Генетические предикторы выживаемости и развития MACE в остром периоде инфекции, вызванной SARS-COV-2, у пациентов высокого кардиоваскулярного риска
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Gusev E., Sarapultsev A., Solomatina L., Chereshnev V. SARS-CoV-2-specific immune response and the pathogenesis of COVID-19. J. Mol. Sci. 2022;23(3):1716. DOI: 10.3390/ijms23031716
- Щербак С.Г., Камилова Т.А., Голота А.С., Вологжанин Д.А. Факторы риска тяжелого течения и летального исхода COVID-19. Физическая и реабилитационная медицина, медицинская реабилитация. 2022;4(1):14–36. Sсherbak S.G., Kamilova T.A., Golota A.S., Vologzhanin D.A. Risk factors of the severe course and fatal outcome in COVID-19. Physical and Rehabilitation Medicine, Medical Rehabilitation. 2022;4(1):14–36. (in Russian). DOI: 36425/rehab104997
- Gao Y.D., Ding M., Dong X., Zhang J.J. et al. Risk factors of severe and critically ill COVID-19 patients: a review. Allergy. 2021;76(2):428–55 DOI: 1111/all.14657
- Guo T., Fan Y., Chen M., Wu X. et al. Cardiovascular Implications of fatal outcomes of patients with coronavirus disease 2019 (COVID-19). JAMA Cardiol. 2020;5(7):1–8. DOI: 10.1001/jamacardio.2020.1017
- Kenney A.D., Dowdle J.A., Bozzacco L., McMichael T.M. et al. Human genetic determinants of viral diseases. Annu. Rev. Genet. 2017;51:241–63. DOI: 10.1146/annurev-genet-120116-023425
- Horowitz J.E., Kosmicki J.A., Damask A., Sharma D. et al. Genome-wide analysis in 756,646 individuals provides first genetic evidence that ACE2 expression influences COVID-19 risk and yields genetic risk scores predictive of severe disease. Nat. Genet. 2022;54(4):382–92. DOI: 10.1038/s41588-021-01006-7
- Вологжанин Д.А., Голота А.С., Камилова Т.А., Шнейдер О.В. и др. Генетика COVID-19. Клиническая практика. 2021;12(1):41–52. Vologzhanin D.A., Golota A.S., Kamilova T.A., Shneider O.V. et al. Genetics of COVID-19. Journal of Clinical Practice. 2021;12(1):41–52. (in Russian). DOI: 10.17816/clinpract64972
- Шпагина Л.А., Козик В.А., Максимов В.Н., Шпагин И.С. и др. Оценка ассоциации полиморфизма гена АСЕ с острым коронарным синдромом у пациентов, перенесших новую коронавирусную инфекцию. Российский кардиологический журнал. 2023;28(10):5503. Shpagina L.A., Kozik V.A., Maksimov V.N., Shpagin I.S. et al. Assessment of the association of ACE gene polymorphism with acute coronary syndrome in patients after a coronavirus disease 2019. Russian Journal of Cardiology. 2023;28(10):5503. (in Russian). DOI: 10.15829/1560-4071-2023-5503
- Богданов Д.С., Черкашин Д.В., Улятовский В.А., Шуленин К.С. и др. Влияние фактора возраста и полиморфизма генов АСЕ и PAI-1 на тяжесть течения новой коронавирусной инфекции (SARS-CoV-2). Трансляционная медицина. 2023;10(6):549– Bogdanov D.S., Cherkashin D.V., Ulyatovsky V.A., Shulenin K.S. et al. Influence of the age factor and АСE and PAI-1 gene polymorphism on the severity of the new coronavirus infection (SARS-CoV-2). Translational Medicine. 2023;10(6):549–56. (in Russian) DOI: 10.18705/2311-4495-2023-10-6-549-556
- Трофимов В.А., Черакшева Д.А. Роль полиморфизмов гена ACE INS/DEL I>D в ишемическом инсульте и COVID-19. Вестник науки. 2023;5(62):915– Trofimov V.A., Cheraksheva D.A. The role of ACE INS/DEL I>D gene polymorphisms in ischemic stroke and COVID-19. Bulletin of Science. 2023;5(62):915–27. (in Russian). DOI: 10.24412/2712-8849-2023-562-915-927
- Verma S., Abbas M., Verma S., Khan F.H. et al. Impact of I/D polymorphism of angiotensin-converting enzyme 1 (ACE1) gene on the severity of COVID-19 patients. Genet. Evol. 2021;91:104801. DOI:10.1016/j.meegid.2021.104801
- Gómez J., Albaiceta G.M., García-Clemente M., López-Larrea C. et al. Angiotensin-converting enzymes (ACE, ACE2) gene variants and COVID-19 outcome. Gene. 2020;762:145102. DOI: 10.1016/j.gene.2020.145102
- Staessen J.A., Ginocchio G., Wang J.G., Saavedra A. et al. Genetic variability in the renin-angiotensin system: prevalence of alleles and genotypes. J. Cardiovasc. Risk. 1997;4(5–6):401–22
- Rigat B., Hubert C., Alhenc-Gelas F., Cambien F. et al. An insertion/deletion polymorphism in the angiotensin I-converting enzyme gene accounting for half the variance of serum enzyme levels. Clin. Invest. 1990;86(4):1343–6. DOI: 10.1172/JCI114844
- Fountain J.H., Kaur J., Lappin S.L. Physiology, renin angiotensin system. In: StatPearls [Internet]. StatPearls Publishing; 2023.
- Pati A., Mahto H., Padhi S., Panda A.K. ACE deletion allele is associated with susceptibility to SARS-CoV-2 infection and mortality rate: an epidemiological study in the Asian population. Chim. Acta. 2020;510:455–8. DOI: 10.1016/j.cca.2020.08.008
- Yamamoto N., Ariumi Y., Nishida N., Yamamoto R. et al. SARS-CoV-2 infections and COVID-19 mortalities strongly correlate with ACE1 I/D genotype. Gene. 2020;758:144944. DOI: 10.1016/j.gene.2020.144944
- Calabrese C., Annunziata A., Coppola A., Pafundi P.C. et ACE gene I/D polymorphism and acute pulmonary embolism in COVID19 pneumonia: a potential predisposing role. Front. Med. (Lausanne). 2021;7:631148. DOI: 10.3389/fmed.2020.631148
- Lv C., Wang Y., Wang J., Zhang H. et al. Association of Interleukin-10 gene polymorphisms with ankylosing spondylitis. Invest. Med. 2011;34(6):E370. DOI: 10.25011/cim.v34i6.15898
- Miteva L.D., Stanilov N.S., Deliysky T.S., Stanilova S.A. Significance of -1082A/G polymorphism of IL10 gene for progression of colorectal cancer and IL-10 expression. Tumour Biol. 2014;35(12):1265–64. DOI: 1007/s13277-014-2589-2
- Fiorentino D.F., Zlotnik A., Mosmann T.R., Howard M. et al. IL-10 inhibits cytokine production by activated macrophages. J. Immunol. 1991;147(11):3815–22
- Batur L.K., Hekim N. Correlations of IL-6, IL-6R, IL-10 and IL-17 gene polymorphisms with the prevalence of COVID-2019 infection and its mortality rate. Preprint (Version 1). Research Square. 2020. URL: https://www.researchgate.net/publication/345429720_Correlations_of_IL-6_IL-6R_IL-10_and_IL-17_gene_polymorphisms_with_the_prevalence_of_COVID-2019_infection_and_its_mortality_rate (дата обращения: 17.11.2023 г.). DOI: 10.21203/rs.3.rs-82662/v1
- Gallagher P.M., Lowe G., Fitzgerald T., Bella A. et al. Association of IL-10 polymorphism with severity of illness in community acquired pneumonia. Thorax. 2003;58(2):154– DOI: 10.1136/thorax.58.2.154
- Boiardi L., Casali B., Farnetti E., Pipitone N. et al. Interleukin-10 promoter polymorphisms in giant cell arteritis. Arthritis Rheum. 2006;54(12):4011–7. DOI: 10.1002/art.22218
- Scarpelli D., Cardellini M., Andreozzi F., Laratta E. et al. Variants of the interleukin-10 promoter gene are associated with obesity and insulin resistance but not type 2 diabetes in Caucasian Italian subjects. Diabetes. 2006;55(5):1529–33. DOI: 10.2337/db06-0047
- Satta Y., Mayer W.E., Klein J. HLA-DRB intron 1 sequences: implications for the evolution of HLA-DRB genes and haplotypes. Hum. Immunol. 1996;51(1):1– DOI: 10.1016/s0198-8859(96)00155-3
- Dobrijević Z., Gligorijević N., Šunderić M., Penezić A. et al. The association of human leucocyte antigen (HLA) alleles with COVID-19 severity: a systematic review and meta-analysis. Rev. Med. Virol. 2023;33(1):e12:2378. DOI: 10.1002/rmv.2378
Введение. Несмотря на то, что вирус SARS-CoV-2 является высоко контагиозным, клинические проявления заболевания, вызванного им, могут иметь существенные различия: от малосимптомного течения до крайне тяжелых форм с развитием летального исхода. Очевидно, что наблюдаемая полиморфность развития инфекции, вызванной SARS-CoV-2, обусловлена также генетическими факторами. К ним относят однонуклеотидные полиморфизмы генов, участвующих в этапах патогенеза инфекции: от проникновения вируса в клетки-мишени, экспрессии его РНК до ответа организма-хозяина. Изучение генетических предикторов, обуславливающих изменение восприимчивости к вирусу SARS-CoV-2 и различия в степени тяжести течения инфекции, поможет лучше понять патогенез этого заболевания и дать представление о перспективных направления терапии и профилактики.
Цель исследования. Изучить взаимосвязь генетических биомаркеров с тяжестью течения инфекции, вызванной SARS-CoV-2, кардиоваскулярными осложнениями и риском летального исхода в раннем периоде заболевания.
Дизайн. Одноцентровое ретроспективное исследование.
Материалы и методы. В исследование были включены 164 пациента (90 мужчин и 74 женщины) с инфекцией, вызванной SARS-CoV-2. Все пациенты относились к категории высокого и очень высокого кардиоваскулярного риска. Сопутствующая соматическая патология: артериальная гипертензия — у 164 (100%), ишемическая болезнь сердца — у 80 (48,9%), алиментарное ожирение — у 100 (61%), предиабет — у 52 (31,74%), хроническая болезнь почек — у 34 (20,7%) пациентов. На первом этапе исследования оценивалась взаимосвязь генетических биомаркеров с тяжестью течения заболевания, на втором — с кардиоваскулярными осложнениями, на третьем — с наступлением летального исхода.
Результаты. В группе пациентов с тяжелым течением заболевания, достоверно чаще встречался вариант DD полиморфизма гена ACE Alu I/D, rs4646994 (p = 0,004), вариант GG полиморфизма гена IL-10 1082 G/A, rs1800896 (p = 0,043), аллель *11 HLA-DRB1 (p = 0,015). Генетическими предикторами развития кардиоваскулярных осложнений явились генотип DD гена ACE (rs4646994) (p = 0,038), аллеля *3 HLA-DRB1 (p = 0,041), реже встречался аллель *13 HLA-DRB1 (p = 0,047). При поиске корреляции между выбранными генетическими биомаркерами и летальным исходом был выявлен только негативный вклад варианта DD полиморфизма ACE Alu I/D, rs4646994 (p = 0,015). Анализ выживаемости показал, что при варианте DD полиморфизма ACE Alu I/D, rs4646994 медиана выживаемости была ниже, чем при варианте II (13 (9–15) суток и 21 (12–н/о) сутки соответственно (p = 0,03)) и варианте ID (31 (14–н/о) сутки (p < 0,0001)). Выживаемость пациентов при гетерозиготном варианте полиморфизма MTRR –66 A/G, rs1801394 составила 11,5 (9–16) суток, при варианте AA — 7 (3–н/о), а при варианте GG — 6 (4–14), p = 0,013. При носительстве аллеля *16 HLA DRB1 выживаемость была всего 5,5 (2–н/о) суток против 22 (17–н/о) суток у пациентов без него, p = 0,04.
Заключение. К предикторам повышенного риска тяжелого течения инфекции, вызванной SARS-CoV-2, следует относить вариант DD полиморфизма гена ACE Alu I/D, rs4646994, вариант GG полиморфизма гена IL-10 1082 G/A, rs1800896 и аллель *11 HLA-DRB1. Негативное влияние варианта DD полиморфизма гена ACE Alu I/D, rs4646994, аллеля *3 HLA-DRB1 и протективное влияние аллеля *13 HLA-DRB1 доказано в отношении общего риска больших кардиоваскулярных осложнений. С повышенным риском ранней внутригоспитальной летальности пациентов коррелируют носительство аллеля *16 HLA-DRB1 и вариант DD полиморфизма гена ACE Alu I/D, rs4646994. В то же время гетерозиготный вариант полиморфизма MTRR –66 A/G, rs1801394 является протекторным биомаркером и ассоциирован с лучшей выживаемостью.
Ключевые слова: вирус SARS-CoV-2, генетические биомаркеры, кардиоваскулярные осложнения, кардиоваскулярный риск, летальность, новая коронавирусная инфекция
Скачать PDFТюрюпов М.С., Шуленин К.С., Свёклина Т.С., Кутелев Г.Г., Шуленин Д.К., Аланичев А.Е., Черкашин Д.В. Генетические предикторы выживаемости и развития MACE в остром периоде инфекции, вызванной SARS-COV-2, у пациентов высокого кардиоваскулярного риска. Вестник терапевта. 2024. № 2 (63). DOI: 10.31550/2712-8601-VT-2024-2-2. URL: https://journaltherapy.ru/statyi/geneticheskie-prediktory-vyzhivaemosti-i-razvitiya-mace-v-ostrom-periode-infekcii-vyzvannoj-sars-cov-2-u-pacientov-vysokogo-kardiovaskulyarnogo-riska/ (дата обращения: дд.мм.гггг)
Тюрюпов Марк Сергеевич — слушатель ординатуры 2-го года по специальности «Терапия» Военно-медицинской академии им. С.М. Кирова. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. eLIBRARY.RU SPIN: 2886-7181. https://orcid.org/0000-0002-8366-0594. E-mail: mark.tfyuryupov@icloud.com
Шуленин Константин Сергеевич — д. м. н., доцент, профессор кафедры военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 198013, Россия, г. Санкт-Петербург, Загородный пр-т, д. 47. eLIBRARY.RU SPIN: 8476-1052. https://orcid.org/0000-0002-3141-7111. E-mail: shulenink@mail.ru
Свёклина Татьяна Сергеевна — к. м. н., доцент, доцент кафедры пропедевтики внутренних болезней Военно-медицинской академии им. С.М. Кирова. 191015, Россия, г. Санкт-Петербург, Суворовский пр-т, д. 63. eLIBRARY.RU SPIN: 3561-6503. https://orcid.org/0000-0001-9546-7049. E-mail: sveklina@rambler.ru
Кутелев Геннадий Геннадьевич (автор для переписки) — д. м. н., старший преподаватель кафедры военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 198013, Россия, г. Санкт-Петербург, Загородный пр-т, д. 47. eLIBRARY.RU SPIN: 5139-8511. https://orcid.org/0000-0002-6489-9938. E-mail: gena08@yandex.ru
Шуленин Дмитрий Константинович — студент 5-го курса факультета подготовки гражданских врачей Военно-медицинской академии им. С.М. Кирова. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. eLIBRARY.RU SPIN: 8476-1052. https://orcid.org/0009-0000-2393-9879. E-mail: shulenink@mail.ru
Аланичев Андрей Евгеньевич — к. м. н., доцент кафедры военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 198013, Россия, г. Санкт-Петербург, Загородный пр-т, д. 47. eLIBRARY.RU SPIN: 6223-7758. https://orcid.org/0000-0002-4135-5815. E-mail: alanichevae80@mail.ru
Черкашин Дмитрий Викторович — д. м. н., профессор, начальник кафедры военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 198013, Россия, г. Санкт-Петербург, Загородный пр-т, д. 47. eLIBRARY.RU SPIN: 2781-9507. https://orcid.org/0000-0003-1363-6860. E-mail: cherkashin_dmitr@mail.ru
Genetic predictorsof survival and development of mace in the acute covid-19 in patients with high cardiovascular risk
M.S. Tyuryupov, K.S. Shulenin, T.S. Svyoklina, G.G. Kutelev, D.K. Shulenin, A.E. Alanichev, D.V. Cherkashin
S.M. Kirov Military Medical Academy; 6 Academician Lebedev Str., St. Petersburg, Russian Federation 194044
Resume
Introduction. Despite the fact that the SARS-CoV-2 virus is highly contagious, the clinical manifestations of the disease caused by it can have significant differences: from a low-symptom course to extremely severe forms with the development of a fatal outcome. It is obvious that the observed polymorphism of the development of infection caused by SARS-CoV-2 is due, among other things, to genetic factors. These include single-nucleotide polymorphisms of genes involved in the stages of the pathogenesis of infection: from the penetration of the virus into target cells, the expression of its RNA to the response of the host organism. The study of genetic predictors that cause changes in susceptibility to the SARS-CoV-2 virus and differences in the severity of infection will help to better understand the pathogenesis of this disease and give an idea of promising areas of therapy and prevention.
Aim. To study the relationship of genetic biomarkers with the severity of infection caused by SARS-CoV-2, cardiovascular complications and the risk of death in the early period of the disease.
Design. A single-center retrospective study.
Materials and methods. The study included 164 patients (90 men, 74 women) with infection caused by SARS-CoV-2. All patients were classified as high and very high cardiovascular risk. Concomitant somatic pathology: arterial hypertension in 164 (100%), coronary heart disease in 80 (48.9%), alimentary obesity in 100 (61%), prediabetes in 52 (31.74%), chronic kidney disease in 34 (20.7%) patients. At the first stage of the study, the relationship of genetic biomarkers with the severity of the disease was evaluated, at the second — with cardiovascular complications, and at the third — with the onset of death.
Results. In the group of patients with severe disease, variant DD of ACE Alu I/D gene polymorphism, rs4646994 (p = 0.004), variant GG of IL-10 polymorphism 1082 G/A, rs1800896 (p = 0.043), allele *11 HLA-DRB1 (p = 0.015) were significantly more common. The genetic predictors of the development of cardiovascular complications were the genotype DD of the ACE gene (rs4646994) (p = 0.038), the allele *3 HLA-DRB1 (p = 0.041), the allele *13 HLA-DRB1 (p = 0.047) was less common. When searching for a correlation between the selected genetic biomarkers and mortality, only a negative contribution of the ACE Alu I/D polymorphism variant DD, rs4646994 (p = 0.015) was revealed. The survival analysis showed that in the DD variant of the ACE Alu polymorphism I/D, rs4646994, the median survival rate is lower than in the II variant (13 (9–15) days and 21 (12–n/o) days, respectively (p = 0.03)), and lower than in the ID (31 variant (14–n/ o) day (p < 0.0001)). The survival rate of patients with the heterozygous variant of the polymorphism MTRR –66 A/G, rs1801394 was 11.5 (9–16) days, with variant AA — 7 (3–n/o), and with variant GG — 6 (4–14), p = 0.013. With the *16 HLA DRB1 allele, survival was only 5.5 (2–n/o) days versus 22 (17–n/o) days in patients without it, p = 0.04.
Conclusion. Predictors of an increased risk of severe infection caused by SARS-CoV-2 include the DD variant of the ACE Alu I/D gene polymorphism, rs4646994, the GG variant of the IL-10 1082 G/A gene polymorphism, rs1800896 and the *11 HLA-DRB1 allele. The negative effect of the DD variant of the polymorphism of the ACE Alu I/D gene, rs4646994, the *3 HLA-DRB1 allele and the protective effect of the *13 HLA-DRB1 allele have been proven in relation to the overall risk of major cardiovascular complications. The carriage of the *16 HLA-DRB1 allele and the DD variant of the ACE Alu I/D gene polymorphism, rs4646994, correlate with an increased risk of early hospital mortality in patients. At the same time, the heterozygous variant of the MTRR –66 A/G polymorphism, rs1801394, is a protective biomarker and is associated with better survival.
Key words: COVID-19, SARS-CoV-2 virus, mortality, cardiovascular complications, cardiovascular risk, genetic biomarkers.
М.С. Тюрюпов, К.С. Шуленин, Т.С. Свёклина, Г.Г. Кутелев, Д.К. Шуленин, А.Е. Аланичев, Д.В. Черкашин
ФГБВОУ ВО «Военно-медицинская академия имени С.М. Кирова» Министерства обороны Российской Федерации; Россия, г. Санкт-Петербург
Пандемия новой коронавирусной инфекции (НКИ), вызванная вирусом SARS-CoV-2, унесла миллионы жизней, создав беспрецедентные проблемы мировой экономике и здравоохранению. Несмотря на то, что вирус SARS-CoV-2 является высоко контагиозным, клинические проявления заболевания, вызванного им, могут иметь существенные различия: от малосимптомного течения до крайне тяжелых форм с развитием летального исхода [1]. К основным факторам, влияющим на течение НКИ, относят возраст и пол пациента, а также сопутствующие соматические заболевания [2]. Их воздействие на тяжесть течения и летальность в остром периоде инфекции, вызванной SARS-CoV-2, неоднократно подтверждалось в крупных метаанализах [3]. С другой стороны, было доказано негативное влияние самой НКИ на течение соматической патологии. Так, к наиболее частым осложнениям острого периода инфекции, вызванной SARS-CoV-2, особенно у полиморбидных пациентов, относятся кардиоваскулярные (острое повреждение миокарда, нарушения сердечного ритма, артериальные и венозные тромбозы). Их развитие объясняется как прямым, так и опосредованным повреждением кардиомиоцитов и эндотелиоцитов, а также нарушениями в системе гемостаза [4]. Тем не менее, наличие указанных выше клинических факторов не всегда может объяснить развитие неблагоприятного исхода.
Поэтому особый интерес представляет изучение молекулярных предикторов осложненного течения НКИ. Однако простое сравнение уровней тех или иных цитокинов с риском развития осложнений не является в полной мере правильным, поскольку экспрессия белков может меняться под действием различных факторов. В этой связи поиск более надежных немодифицируемых предикторов направлен в сторону геномных биомаркеров. Генетические детерминанты выраженности ответа и чувствительности к вирусным инфекциям — плодотворное поле для деятельности ученых в течение нескольких последних десятилетий. В настоящее время уже определен ряд геномных биомаркеров для инфекций, вызванных вирусом гриппа, иммунодефицита человека, респираторным синцитиальным вирусом, гепатита С, гепатита В и некоторыми другими [5].
Очевидно, что наблюдаемая полиморфность течения НКИ обусловлена также генетическими факторами, изучению которых в последнее время уделяется все большее внимание [6]. На данный момент проведены полногеномные исследования в различных этнических популяциях, в которых были выявлены потенциальные генетические биомаркеры, связанные с повышенным риском инфицирования и тяжелого течения НКИ. К ним относят однонуклеотидные полиморфизмы генов, участвующих в этапах патогенеза инфекции, вызванной SARS-CoV-2: от проникновения вируса в клетки-мишени, экспрессии его РНК до ответа организма-хозяина [7]. Исследования, выполненные в Российской Федерации в 2022–2023 годах, показали ассоциацию полиморфизмов генов системы регуляции артериального давления (гена, ответственного за экспрессию рецепторов ангиотензинпревращающего фермента 2 типа) с развитием тяжелого течения, летального исхода и неблагоприятных сердечно-сосудистых событий в остром периоде НКИ [8–10].
Тем не менее, все же остро ощущается нехватка исследований, связанных с генетикой человека. Именно изучение генетических предикторов, обуславливающих изменение восприимчивости к вирусу SARS-CoV-2 и различия в степени тяжести течения НКИ, поможет лучше понять патогенез этого заболевания и дать представление о перспективных направлениях терапии и профилактики [5].
Цель исследования — изучить взаимосвязь генетических биомаркеров с тяжестью течения инфекции, вызванной SARS-CoV-2, кардиоваскулярными осложнениями и риском летального исхода в раннем периоде заболевания.
Материалы и методы
В исследование были включены 164 пациента с НКИ, проходившие лечение в Военно-медицинской академии им. С.М. Кирова с мая 2020 по февраль 2022 года. Медиана возраста больных составила 67 (57–74) лет; распределение по полу — 90 (54,9%) мужчин и 74 (45,1%) женщины. Сопутствующая соматическая патология: артериальная гипертензия — у 164 (100%), ишемическая болезнь сердца — у 80 (48,9%), алиментарное ожирение — у 100 (61%), предиабет (нарушение толерантности к глюкозе и/или нарушенная гликемия натощак) — у 52 (31,7%), хроническая болезнь почек (ХБП) — у 34 (20,7%) человек. Все пациенты относились с категории высокого и очень высокого кардиоваскулярного риска.
Работа проводилась в рамках исследования, одобренного локальным этическим комитетом Военно-медицинской академии им. С.М. Кирова (протокол № 271 от 22.11.2022 г.). Всеми пациентами было подписано информированное добровольное согласие на медицинское вмешательство, обработку персональных данных и участие в исследовании.
Исследование последовательно проходило в 3 этапа. На первом этапе пациенты были разделены на две группы в зависимости от тяжести течения инфекции, вызванной SARS-CoV-2. В первую группу (n = 53; 32%) вошли пациенты с легким и среднетяжелым течением заболевания, во вторую (n = 111; 68%) — с тяжелым и крайне тяжелым. Это позволило провести сопоставление тяжести течения НКИ с результатами генетического типирования врожденного иммунитета (лейкоцитарного человеческого антигена 2 класса (HLA-DRB1) — у 148 пациентов, толл-подобных рецепторов 3 типа (TLR3 –412 L/F) — у 71 пациента), воспалительных цитокинов (IL-6 (–174 G/C, rs1800795) — у 164 пациентов, IL-1b (–511 T/C, –1473 G/C) — у 71 пациента, IL-10 (–1082 G/A, rs1800896) — у 70 пациентов, фактора некроза опухолей α (TNF –308 G/A) — у 71 пациента), системы регуляции артериального давления (ангиотензинпревращающего фермента (АПФ) (ACE Alu I/D, rs4646994) — у 133 пациентов, ангиотензина 2 (–235 M/T) — у 66 пациентов), системы гемостаза (ингибитора активатора плазминогена 1 типа (SERPINE 1 (PAI-1) –675 5G/4G) — у 71 пациента), 13 фактора свертывания (F13A1 –35 V/L) — у 66 пациентов, интегрин-бета 3 (ITGB3 –33 L/P) — у 38 пациентов), фолатного цикла (метилентетрагидрофолатредуктазы (MTHFR –677 C/T, rs1801133) — у 65 пациентов, метионин-синтаза-редуктазы (MTRR –66 A/G, rs1801394) — у 66 пациентов), липидного обмена (липазы C (LIPC –250 G/A, rs2070895) — у 87 пациентов, липопротеинлипазы (LPL –447 C/T, rs328) — у 76 пациентов) и индукторов апоптоза — атаксии-телеангиэктазии мутаций (ATM –185 Asp/Asn, rs1801516) — у 90 пациентов.
На втором этапе оценивалась взаимосвязь выбранных генетических биомаркеров с риском развития кардиоваскулярных осложнений в остром периоде НКИ. Для этого была введена комбинированная конечная точка, которая включала в себя развитие тромбоза легочной артерии, инфаркта миокарда, фибрилляции предсердий, острого нарушения мозгового кровообращения, острого тромбоза мезентериальных артерий и артерий нижних конечностей — MACE (major adverse cardiovascular events). В соответствие с ее достижением пациенты были разделены на две группы: достигшие (MACE+) (n = 91; 55,5%) и не достигшие комбинированной конечной точки (MACE–) (n = 73; 44,5%). На завершающем этапе был проведен поиск генетических маркеров летального исхода и предикторов выживаемости в остром периоде НКИ. Для этого также сформировали две группы пациентов: умершие в остром периоде (n = 92; 56%) и выжившие (n = 72; 44%). Все выделенные группы на трех этапах исследования были однородны по полу, возрасту и коморбидной патологии (табл. 1).
Таблица 1. Сравнительная клиническая характеристика пациентов, включенных в группы на этапах исследования
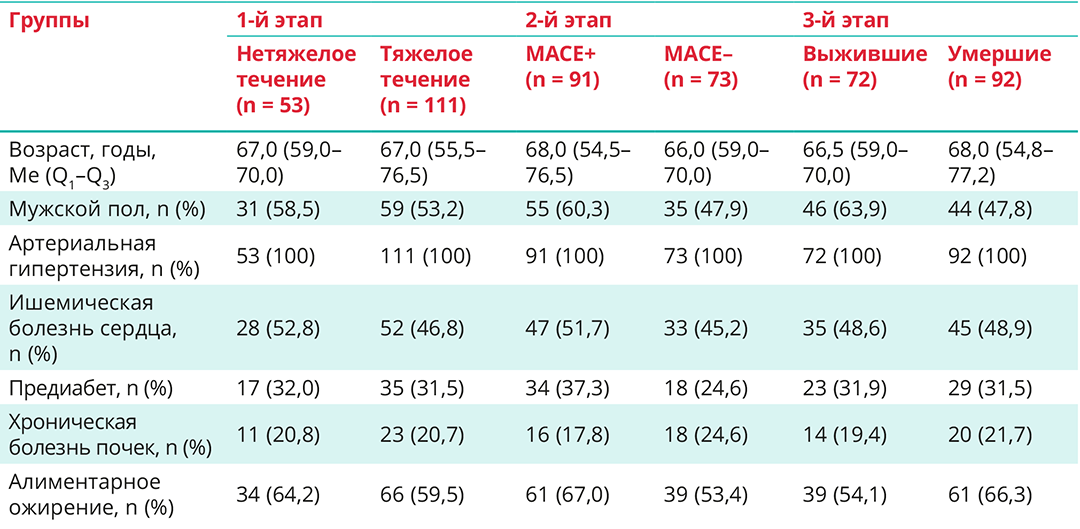
Примечание: все различия в группах недостоверны.
Для определения генетических полиморфизмов использовалась периферическая кровь пациентов, которую забирали в пробирки ЭДТА при выписке. У умерших анализ генетических полиморфизмов осуществлялся с использованием секционного материала — селезенки. Выделение ДНК проводили с использованием набора «ГС-генетика», а амплификацию ДНК — на приборе «ДТ-Прайм» (ООО «ДНК-технология», Россия).
Статистическая обработка данных производились в статистическом пакете R, версия 4.3.1. При описании данных для числовых переменных, распределенных нормально, использовалось среднее и стандартное отклонение M (SD), для негауссовских переменных — медиана и межквартильный размах Me (Q1–Q3). Для номинальных и порядковых данных в описательной статистике использовалось количество вхождений каждого значения и доли каждого значения по отношению ко всей выборке n (m%). Поиск отличий осуществлялся методом проверки статистических гипотез. Для нормальных выборок использовался критерий Стьюдента, для негауссовских — критерий Манна — Уитни. Номинальные и порядковые выборки сравнивались при помощи критерия χ2, при малых выборках (хотя бы одно из ожидаемых меньше 10) — точного критерия Фишера. Анализ выживаемости проводился методом Каплана — Мейера, при этом кривые выживаемости для различных подгрупп сравнивались при помощи логрангового критерия. Во всех случаях проверки гипотез различие признавалось статистически значимым при p < 0,05. Соотношение частот аллелей и генотипов проверялось на соответствие уравнению Харди — Вайберга.
Результаты
Было установлено, что у пациентов высокого кардиоваскулярного риска имеет место корреляция тяжести течения инфекции, вызванной SARS-CoV-2, с однонуклеотидными полиморфизмами генов ACE и IL-10, а также с носительством аллеля *11 HLA—DRB1. Распределение генотипов соответствовало уравнению Харди — Вайберга для гена IL-10 1082 G/A, rs1800896 (p = 0,63). Было установлено несоответствие уравнению Харди — Вайберга для гена ACE Alu I/D, rs4646994 за счет превалирования обоих гомозиготных генотипов над гетерозиготными (p < 0,01). Однако при оценке частот встречаемости аллелей выявлена корреляция их со средними значениями в Европе: аллель I — 46%, аллель D — 54% [13]. В группе пациентов с тяжелым течением заболевания статистически значимо чаще встречались вариант DD полиморфизма гена ACE Alu I/D, rs4646994 (48,0% против 12,9%, p = 0,004), вариант GG полиморфизма гена IL-10 1082 G/A, rs1800896 (41,2% против 15,8%), аллель *11 HLA—DRB1 (33,3% против 13,5%, p = 0,015). Указанные генетические биомаркеры можно с уверенностью назвать предикторами, достоверно повышающими вероятность тяжелого течения НКИ (табл. 2).
Таблица 2. Генетические предикторы тяжести течения инфекции, вызванной SARS-CoV-2, у пациентов высокого кардиоваскулярного риска, n (%)
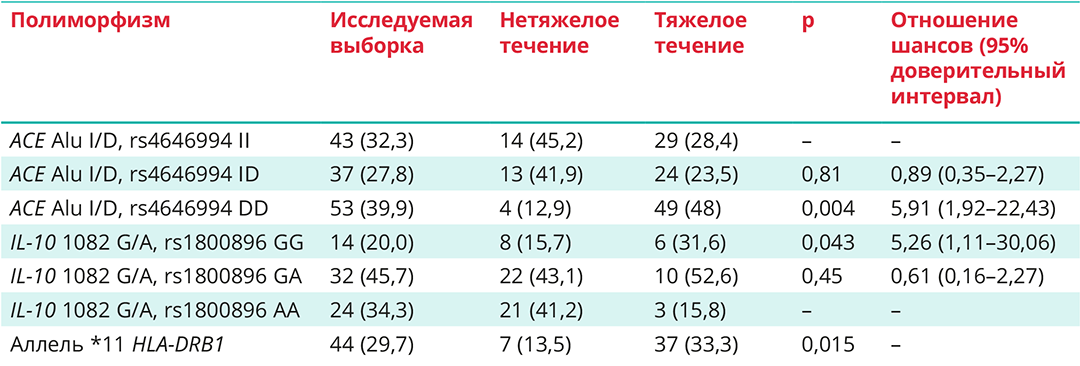
При оценке распределения полиморфизмов в группах пациентов, достигших комбинированной конечной точки MACE, было отмечено увеличение встречаемости генотипа DD гена ACE (rs4646994) (45,5% против 28,9%, p = 0,038) и аллеля *3 HLA-DRB1 (16,7% против 7,1 %, p = 0,041), а также более редкая встречаемость аллеля *13 HLA-DRB1 (16,7% против 31,4%, p = 0,047) (табл. 3).
Таблица 3. Генетические предикторы общего риска больших кардиоваскулярных осложнений в остром периоде инфекции, вызванной SARS-CoV-2, n (%)
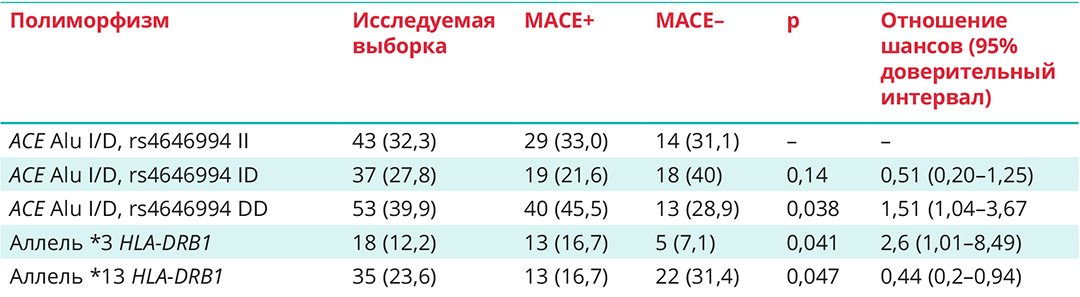
Поиск корреляций между выбранными генетическими биомаркерами и летальным исходом выявил только негативный вклад варианта DD полиморфизма ACE Alu I/D, rs4646994. Так, в группе умерших в раннем периоде инфекции, вызванной SARS-CoV-2, пациентов он встречался значимо чаще (50,6% против 18,2%, p = 0,015) (табл. 4).
Таблица 4. Распределение полиморфизма гена ACE Alu I/D, rs646994, n (%)
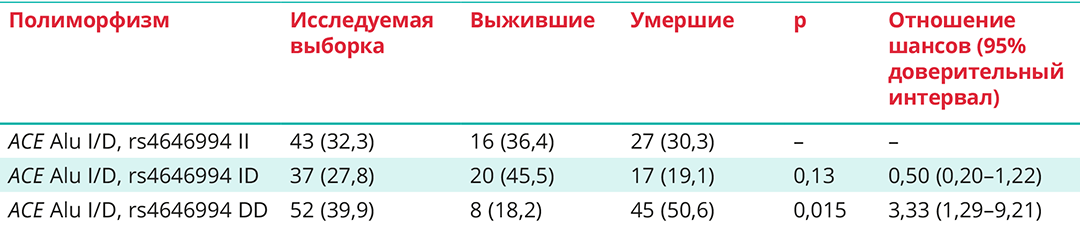
Анализ выживаемости пациентов показал, что при варианте DD полиморфизма ACE Alu I/D, rs4646994 медиана выживаемости ниже, чем при варианте II (13 (9–15) суток и 21 (12–н/о) сутки соответственно (p = 0,03)) и варианте ID (31 (14–н/о) сутки (p < 0,0001)). Значимых различий выживаемости между носителями генотипов II и ID не наблюдалось, p = 0,07 (рис. 1).
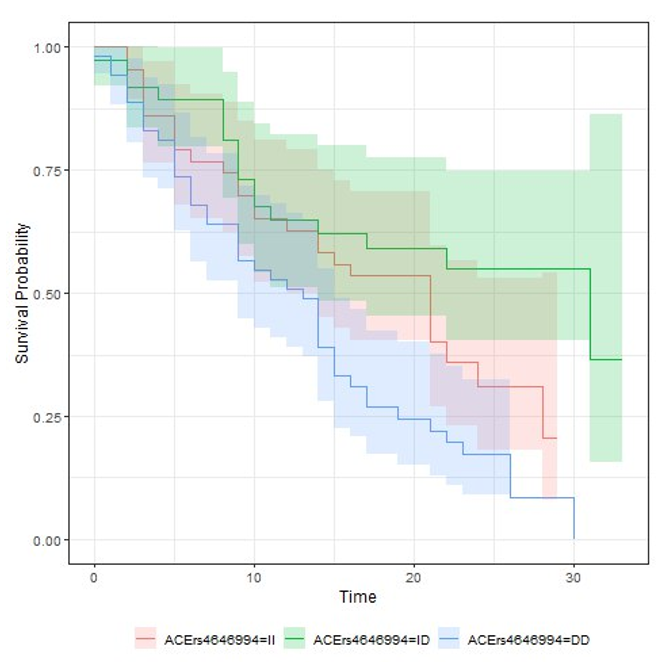
Рисунок 1. Выживаемость пациентов в остром периоде инфекции, вызванной SARS-CoV-2, при различных вариантах полиморфизма ACE Alu I/D, rs4646994
Необходимо отметить, что при оценке выживаемости нами были выявлены различия по аллельным вариантам генов, которые не показали сильной статистической связи на предыдущих этапах анализа. Так, выживаемость пациентов при гетерозиготном варианте полиморфизма MTRR –66 A/G, rs1801394 оказалась выше, чем при обоих гомозиготных вариантах. Его можно отнести к генетическим биомаркерам с протекторным эффектом. Медианная выживаемость при этом варианте составила 11,5 (9–16) суток, при варианте AA — 7 (3–н/о), а при варианте GG — 6 (4–14), p = 0,013 (рис. 2).
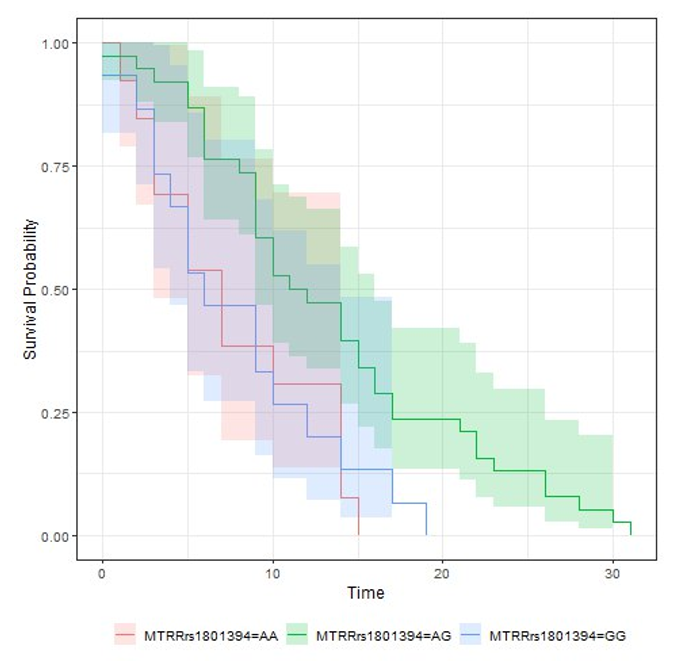
Рисунок 2. Выживаемость пациентов в остром периоде инфекции, вызванной SARS-CoV-2, при различных вариантах полиморфизма гена MTRR –66 A/G, rs1801394
Это же было справедливо и в отношении гена HLA—DRB1. Нами установлено, что носительство аллеля *16 класса ассоциировано с низкой выживаемостью и наступлением летального исхода в более ранние сроки. Медианная выживаемость при носительстве этого варианта составила всего 5,5 (2–н/о) суток против 22 (17–н/о) суток у пациентов без данного аллеля, p = 0,04 (рис. 3).
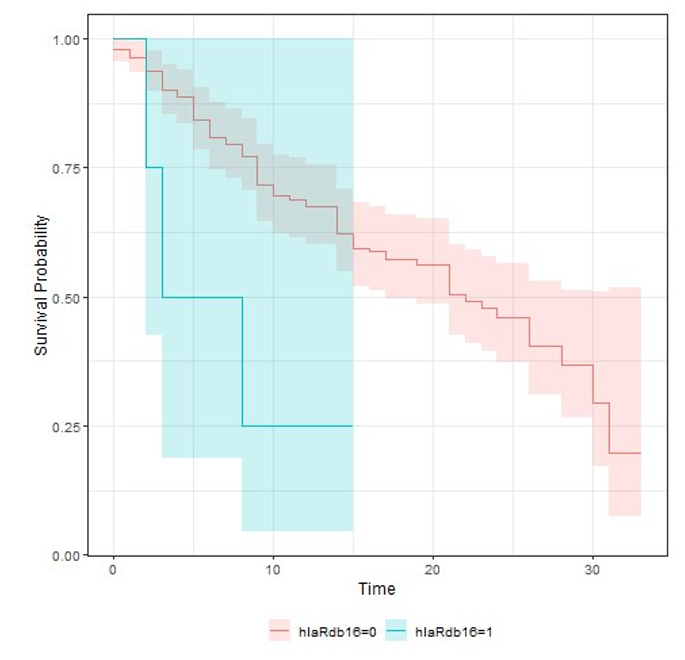
Рисунок 3. Выживаемость пациентов в остром периоде инфекции, вызванной SARS-CoV-2, при наличии и отсутствии аллеля *16 HLA DRB1
Обсуждение
Нами было установлено, что вариант DD гена ACE Alu I/D, rs4646994 достоверно чаще ассоциирован с тяжелым течением НКИ (отношение шансов (ОШ) = 5,91 при 95% доверительном интервале (ДИ) — 1,92–22,43). Аналогичные данные приводят авторы из Индии, определившие в своем исследовании, что носительство генотипа DD гена ACE rs4646994 повышает риск тяжелого течения инфекции, вызванной SARS-CoV-2, в 3 раза (ОШ = 3,69 при 95% ДИ — 1,61–8,43) [11]. J. Gomez и соавт., в свою очередь, показали, что связь варианта DD полиморфизма ACE Alu I/D, rs4646994 с тяжестью течения НКИ усиливается именно у пациентов с АГ [12]. Анализ большинства европейских данных продемонстрировал почти равное распределение аллелей I и D гена ACE, что наблюдалось и в нашем исследовании [13].
Объяснить такую связь можно более высокой экспрессией АПФ у гомозигот по данному аллелю [14]. Хорошо известно, что вирус SARS-CoV-2 проникает в клетку с помощью АПФ2-рецептора [1], который за счет протеолиза ангиотензина II нивелирует его негативное действие [15]. Таким образом, одновременная избыточная экспрессия АПФ и истощение его основной ингибирующей системы (АПФ2-рецепторов) приводят к повышению активности ангиотензина II, что сопровождается более высокой интенсивностью воспалительного процесса, меньшей адаптацией к гипоксии и развитию мультисистемного оксидативного стресса.
Кроме того, полученные нами данные свидетельствуют об ассоциации варианта DD гена ACE Alu I/D, rs646994 с повышенной летальностью в раннем периоде инфекции, вызванной SARS-CoV-2. Это также находит свое подтверждение у других авторов. В исследовании Д.С. Богданова продемонстрирована выраженная корреляция генотипа DD гена ACE Alu I/D, rs4646994 с 6-кратным повышением риска летального исхода у носителей этого генотипа (ОШ = 6,08 при 95% ДИ — 2,97–12,43) [9]. A. Pati и соавт. показали увеличение смертности у пациентов с вариантом DD в 8 раз по сравнению с носителями варианта II [16]. Аналогичные данные приводит N. Yamamoto с соавт. [17]. Ассоциация гомозиготного носительства аллеля D гена ACE Alu I/D, rs4646994 с повышенный риском развития кардиоваскулярных и тромботических осложнений также может быть объяснена высокой экспрессией АПФ. C. Calabrese с соавт. на выборке из 68 пациентов установили достоверную зависимость риска развития тромботических осложнений при НКИ с наличием варианта DD гена ACE Alu I/D, rs646994 ID (72% против 46,5%, р = 0,048) [18]. Схожие данные приводят Л.А. Шпагина и соавт., выявившие ассоциацию генотипа DD этого гена с развитием острого коронарного синдрома у пациентов с инфекцией, вызванной SARS-CoV-2, в анамнезе (26% против 16%, p = 0,044) [8].
В нашем исследовании одним из ведущих предикторов тяжелого течения НКИ показал себя также вариант GG полиморфизма гена IL-10 1082 G/A, rs1800896. Аллель G полиморфизма IL-10 1082 G/A, rs1800896 независимо ассоциирован с большим уровнем экспрессии ИЛ-10 [19, 20], являющегося универсальным противоспалительным цитокином [21]. В результате неограниченной экспрессии ИЛ-10 нарушается адекватный иммунный ответ организма-хозяина, что может приводить к более активному прогрессированию инфекционного процесса и более выраженной агрессии возбудителя. В этом ключе представляется логичным ассоциация гомозиготного носительства данного аллеля с тяжелым течением и смертностью от инфекционных заболеваний. Это справедливо и в отношении инфекции, вызванной SARS-CoV-2, при которой была убедительно доказана корреляция варианта GG полиморфизма гена IL-10 1082 G/A, rs1800896 с большей летальностью [22]. Кроме того, имеются данные и об ассоциации гомозиготного носительства этого аллеля с тяжелым течением внебольничной пневмонии [23]. В общей популяции, по данным авторов, распределение генотипов следующее: GG встречается в 42–43% случаев, AG — в 45–46%, GG — в 11–13% [24, 25]. Исследуемая нами выборка статистически значимо не отличалась по распределению полиморфизмов от общей популяции.
Человеческие лейкоцитарные антигены II класса расположены на антигенпрезентирующих клетках: макрофагах, B-лимфоцитах, дендритных клетках. В частности, белок, кодируемый геном HLA—DRB1, играет центральную роль в иммунной системе, презентуя T-хелперам пептиды, полученные из чужеродных белков [26]. Однако в настоящее время существуют противоречивые данные в отношении ассоциации тех или иных аллелей данного гена с тяжестью течения инфекции, вызванной SARS-CoV-2. В нашем исследовании показано, что носительство аллеля *11 HLA—DRB1 ассоциировано с более тяжелым течением НКИ. Тем не менее, в крупном метаанализе [27], напротив, отмечено протективное влияние данного аллеля. Вероятно, это связано с его большей встречаемостью в исследуемой выборке в сравнении с общей популяцией. Данный вопрос, безусловно, требует более детальной оценки и дальнейших исследований.
Заключение
В рамках нашего исследования были получены новые данные, указывающие на существенную роль некоторых генетических биомаркеров в неблагоприятном течении и исходе НКИ у пациентов высокого кардиоваскулярного риска. К предикторам повышенного риска тяжелого течения инфекции, вызванной SARS-CoV-2, следует относить вариант DD полиморфизма гена ACE Alu I/D, rs4646994, вариант GG полиморфизма гена IL-10 1082 G/A, rs1800896 и аллель *11 HLA—DRB1. Негативное влияние варианта DD полиморфизма гена ACE Alu I/D, rs4646994, аллеля *3 HLA—DRB1 и протективное влияние аллеля *13 HLA—DRB1 доказано в отношении общего риска больших кардиоваскулярных осложнений. С высоким риском ранней внутригоспитальной летальности пациентов коррелируют носительство аллеля *16 HLA—DRB1 и вариант DD полиморфизма гена ACE Alu I/D, rs4646994. В то же время гетерозиготный вариант полиморфизма MTRR –66 A/G, rs1801394 является протекторным биомаркером и ассоциирован с лучшей выживаемостью. Таким образом, можно рассматривать выявленные генетические биомаркеры в качестве потенциальных факторов риска и антириска неблагоприятного течения НКИ. Их определение может быть полезным в стратификации риска пациентов с кардиоваскулярной патологией.
Предыдущая статья
Т.С. Ринчинова1, О.В. Серебрякова1, А.П. Фёдорова1, Д.П. Иванов
Следующая статья
Д.С. Евдокимов, С.А. Болдуева, Е.Д. Реснянская, С.А. Винничук ФГБОУ ВО «Северо-Западный государст...