Патоморфологические особенности миокарда у пациентов с вирусной инфекцией COVID-19
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Чазова И.Е., Миронова О.Ю. COVID-19 и сердечно-сосудистые заболевания. Терапевтический архив. 2020;92(9):4–7. Chazova I.E., Mironova O.I. COVID-19 and cardiovascular diseases. Therapeutic Archive. 2020;92(9):4–7. (in Russian). DOI: 10.26442/00403660.2020.09.000742
- Sandoval Y., Januzzi J.L. Jr, Jaffe A.S. Cardiac troponin for assessment of myocardial injury in COVID-19: JACC review topic of the week. J. Am. Coll. Cardiol. 2020;76(10):1244–58. DOI:10.1016/j.jacc.2020.06.068
- Bangalore S., Sharma A., Slotwiner A., Yatskar L. et al. ST-segment elevation in patients with Covid-19 — a case series. N. Engl. J. Med. 2020;382(25):2478–80. DOI:10.1056/NEJMc2009020
- Stefanini G.G., Montorfano M., Trabattoni D., Andreini D. et al. ST-elevation myocardial infarction in patients with COVID-19: clinical and angiographic outcomes. Circulation. 2020;141(25):2113–6. DOI: 10.1161/CIRCULATIONAHA.120.047525
- Angeli F., Spanevello A., De Ponti R., Visca D. et al. Electrocardiographic features of patients with COVID-19 pneumonia. Eur. J. Intern. Med. 2020;78:101–6. DOI: 10.1016/j.ejim.2020.06.015
- Tutor A., Unis G., Ruiz B., Bolaji O.A. et al. Spectrum of suspected cardiomyopathy due to COVID-19: a case series. Curr. Probl. Cardiol. 2021;46(10):100926. DOI:10.1016/j.cpcardiol.2021.100926
- Haslbauer J.D., Tzankov A., Mertz K.D., Schwab N. et al. Characterisation of cardiac pathology in 23 autopsies of lethal COVID-19. J. Pathol. Clin. Res. 2021;7(4):326–37. DOI: 10.1002/cjp2.212
- Shi S., Qin M., Cai Y., Liu T. et al. Characteristics and clinical significance of myocardial injury in patients with severe coronavirus disease 2019. Eur. Heart J. 2020;41(22):2070–9. DOI: 10.1093/eurheartj/ehaa408
- Болдуева С. А., Евдокимов Д. С., Евдокимова Л. С., Хомуло А. Д. и др. Дифференциальная диагностика острого повреждения миокарда: разбор клинического случая и обсуждение проблемы. Российский кардиологический журнал. 2020;25(11):137–42. Boldueva S.A., Evdokimov D.S., Evdokimova L.S., Khomulo A.D. et al. Differential diagnosis of acute myocardial injury: a case report and discussion. Russian Journal of Cardiology. 2020;25(11):137–42. (in Russian). DOI:10.15829/1560-4071-2020-4046
- Чаулин А.М., Карслян Л.С., Дупляков Д.В. Некоронарогенные причины повышения тропонинов в клинической практике. Клиническая практика. 2019;10(4):81–93. Chaulin AM, Karslyan LS, Duplyakov DV. Non-coronarogenic causes of increased cardiac troponins in clinical practice. Journal of Clinical Practice. 2019;10(4):81–93. (in Russian). DOI: 10.17816/ clinpract16309
- Wang Y., Shu H., Liu H., Li X. et al. The peak levels of highly sensitive troponin I predicts in-hospital mortality in COVID-19 patients with cardiac injury: a retrospective study. Eur. Heart J. Acute Cardiovasc. Care. 2021;10(1):6–15. DOI: 10.1093/ehjacc/zuaa019
- Bellan M., Patti G., Hayden E., Azzolina D. et al. Fatality rate and predictors of mortality in an Italian cohort of hospitalized COVID-19 patients. Sci. Rep. 2020;10(1):20731. DOI: 10.1038/s41598-020-77698-4
- Биличенко Т.Н. Эпидемиология новой коронавирусной инфекции (COVID-19). Академия медицины и спорта. 2020;1(2):14–20. Bilichenko T.N. Epidemiology of Coronavirus disease 2019 (COVID-19). Academy of Medicine and Sports. 2020;1(2):14–20. (in Russian). DOI: 10.15829/2712-7567-2020-2-15
- Мареев В.Ю., Беграмбекова Ю.Л., Мареев Ю.В. Как оценивать результаты лечения больных с новой коронавирусной инфекцией (COVID-19)? Шкала Оценки Клинического Состояния (ШОКС–КОВИД). Кардиология. 2020;60(11):35–41. Mareev V.Yu., Begrambekova Yu.L., Mareev Yu.V. How evaluate results of treatment in patients with COVID-19? Symptomatic Hospital and Outpatient Clinical Scale for COVID-19 (SHOCS–COVID). 2020;60(11):35–41. (in Russian). DOI: 10.18087/cardio.2020.11.n1439
- Зайратьянц О.В., ред. Патологическая анатомия COVID-19: Атлас. М.: ГБУ «НИИОЗММ ДЗМ»; 2020. 140 с. Zayratyants O.V., ed. Pathological anatomy of COVID-19: Atlas. M.: GBU "NIIOZMM DZM"; 2020. 140 p. (in Russian)
- Бубнова М.Г., Аронов Д.М. COVID-19 и сердечно-сосудистые заболевания: от эпидемиологии до реабилитации. Пульмонология. 2020;30(5):688–99. Bubnova M.G., Aronov D.M. COVID-19 and cardiovascular diseases: from epidemiology to rehabilitation. Pulmonologiya. 2020;30(5):688–99. (in Russian). DOI: 10.18093/0869-0189-2020-30-5-688-699
- Unudurthi S.D., Luthra P., Bose R.J.C., McCarthy J.R. et al. Cardiac inflammation in COVID-19: lessons from heart failure. Life Sci. 2020;260:118482. DOI: 10.1016/j.lfs.2020.118482
- Hooper J.E., Padera R.F., Dolhnikoff M., Saldiva P.H. et al. A postmortem portrait of the coronavirus disease 2019 (COVID-19) pandemic: a large multi-institutional autopsy survey study. Arch. Pathol. Lab. Med. 2021;145(5):529–35. DOI: 10.5858/arpa.2020-0786-SA
- Guzik T.J., Mohiddin S.A., Dimarco A., Patel V. et al. COVID-19 and the cardiovascular system: implications for risk assessment, diagnosis, and treatment options. Cardiovasc. Res. 2020;116(10):1666–87. DOI: 10.1093/cvr/cvaa106
- Потешкина Н.Г., Лысенко М.А., Ковалевская Е.А., Фомина Д.С. и соавторы. Кардиальное повреждение у пациентов с коронавирусной инфекцией COVID-19. Артериальная гипертензия. 2020;26(3):277–87. Poteshkina N.G., Lysenko M.A., Kovalevskaya E.A., Fomina D.S. et al. Cardiac damage in patients with COVID-19 coronavirus infection. Arterial Hypertension. 2020;26(3):277– (in Russian). DOI: 10.18705/1607-419X-2020-26-3-277-287
- Коган Е.А., Березовский Ю.С., Проценко Д.Д., Багдасарян Т. Р. и др. Патологическая анатомия инфекции, вызванной SARS-CoV-2. Судебная медицина. 2020;6(2):8–30. Kogan E.A., Berezovsky Yu.S., Protsenko D.D., Bagdasaryan T.R. et al. Pathological anatomy of infection caused by SARS-CoV-2. Russian Journal of Forensic Medicine. 2020;6(2):8–30. (in Russian). DOI: 19048/2411-8729-2020-6-2-8-30
- Митрофанова Л.Б., Макаров И.А., Рунов А.Л., Вонский М.С. и др. Клинико- морфологическое и молекулярно-биологическое исследование миокарда у пациентов с COVID-19. Российский кардиологический журнал. 2022;27(7):4810. Mitrofanova L.B., Makarov I.A., Runov A.L., Vonsky M.S. et al. Clinical, morphological and molecular biological examination of the myocardium in COVID-19 patients. Russian Journal of Cardiology. 2022;27(7):4810. (in Russian). DOI: 10.15829/1560-4071-2022-4810
- Varga Z., Flammer A.J., Steiger P., Haberecker M. et al. Endothelial cell infection and endotheliitis in COVID-19. Lancet. 2020;395(10234):1417–8. DOI: 10.1016/S0140-6736(20)30937-5
- Giustino G., Pinney S.P., Lala A., Reddy V.Y. et al. Coronavirus and cardiovascular disease, myocardial injury, and arrhythmia: JACC focus seminar. J. Am. Coll. Cardiol. 2020;76(17):2011–23. DOI: 10.1016/j.jacc.2020.08.059
- Fox S.E., Li G., Akmatbekov A., Harbert J.L. et al. Unexpected features of cardiac pathology in COVID-19 infection. Circulation. 2020;142(11):1123–5. DOI: 10.1161/CIRCULATIONAHA.120.049465
Коронавирусная инфекция 2019 года (COVID-19) является причиной высокой смертности во всем мире. Несмотря на то, что повреждение миокарда было продемонстрировано у пациентов с COVID-19 в критическом состоянии, его механизм, а также морфологические изменения миокарда при этом остаются малоизученными.
Цель исследования — изучение морфологии миокарда по данным аутопсии у пациентов с установленной инфекцией COVID-19 в зависимости от уровня тропонина за время госпитализации.
Дизайн. Ретроспективное нерандомизированное когортное исследование.
Материалы и методы. Были проанализированы истории болезни 66 умерших пациентов с диагнозом коронавирусная инфекция, находившихся на лечении в клинике ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России с 01.05.2020 г. по 31.07.2020 г. В зависимости от уровня тропонина Т, определенного прижизненно, исследуемые были разделены на две группы. Первую группу (TnT+) составили 28 пациентов, у которых прижизненно было зафиксировано повышение тропонина Т более 100,000 пг/мл (референсное значение в нашей лаборатории), во вторую (TnT–) вошли 16 человек, у которых значимого увеличения уровня тропонина Т не отмечалось. У 22 пациентов тропонин не определялся, и они были включены в общую группу умерших. Анализировались клинические проявления COVID-19 (симптомы, данные объективного осмотра, объем поражения легких по заключению компьютерной томографии, выраженность дыхательной недостаточности), лабораторные показатели, наличие сопутствующей патологии, а также результаты аутопсии. Вскрытие производилось по стандартному протоколу, с гистологическим исследованием микропрепаратов легких, миокарда, печени, почек, поджелудочной железы и селезенки.
Результаты. Сравнительный анализ групп TnT+ и TnT– показал, что у пациентов с повышенным уровнем тропонина чаще развивались ДВС-синдром (в 9 и 1 случае соответственно (p = 0,05)), тромбоэмболия легочной артерии (6 и 0 соответственно (p = 0,05)), а также обнаруживались тромбозы других локализаций (6 и 0 соответственно (p = 0,05)). Кроме того, в группе TnT+ за время госпитализации на фоне пневмонии COVID-19 впервые развивался пароксизм фибрилляции предсердий. При макроскопическом исследовании миокарда всех умерших пациентов определена высокая распространенность гипертрофии (в 56 (84,8%) случаях) и дилатации (у 31 (46,9%) человека) левого желудочка. Микроскопическое исследование выявило периваскулярный фиброз у 51 (77,3%) пациента, а межмышечный — у 38 (57,6%), интерстициальный отек диагностирован у 40 (60,6%) человек. Признаки поражения сосудов среднего калибра и микроциркуляторного русла с наличием стаза, микротромбозами интрамуральных сосудов миокарда определялись у 10 (15,1%) человек. При сравнении результатов аутопсии миокарда у больных с признаками острого повреждения миокарда (группа TnT+) и без такового (группа TnT–) различий выявлено не было. Вместе с тем в группе TnT+ чаще встречались признаки эндотелиита (p = 0,48), сопровождавшегося микротромбозами и кровоизлияниями в миокард, однако различия не были статистически значимыми (p = 0,13 и p = 0,64 соответственно), что, возможно, обусловлено небольшой выборкой пациентов.
Заключение. Поскольку сравниваемые группы статистически значимо не различались по результатам гистологического исследования миокарда, какой субстрат определяет повышение тропонинов при остром повреждении миокарда, остается до конца неясным. Требуется проведение дальнейших исследований с применением современных диагностических методов.
Ключевые слова: COVID-19, аутопсия, повреждение миокарда, эндотелиит
Скачать PDFЕвдокимов Д.С., Болдуева С.А., Реснянская Е.Д., Винничук С.А. Патоморфологические особенности миокарда у пациентов с вирусной инфекцией COVID-19. Вестник терапевта. 2024. № 2 (63). DOI: 10.31550/2712-8601-VT-2024-2-3. URL: https://journaltherapy.ru/statyi/patomorfologicheskie-osobennosti-miokarda-u-pacientov-s-virusnoj-infekciej-covid-19/ (дата обращения: дд.мм.гггг)
Евдокимов Дмитрий Сергеевич (автор для переписки) — аспирант кафедры факультетской терапии ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России. 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41. eLIBRARY.RU SPIN: 5260-0063. https://orcid.org/0000-0002-3107-1691. E-mail: kasabian244@gmail.com
Болдуева Светлана Афанасьевна — д. м. н., профессор, заведующая кафедрой факультетской терапии ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России. 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41. eLIBRARY.RU SPIN: 3716-3375. https://orcid.org/0000-0002-1898-084Х. E-mail: svetlanaboldueva@mail.ru
Реснянская Екатерина Денисовна — студентка 4-го курса ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России. 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41. eLIBRARY.RU SPIN: 7271-3560. https://orcid.org/0000-0001-7889-3679. E-mail: katerina.resn_7@mail.ru
Винничук Сергей Анатольевич — к. м. н., доцент кафедры патологической анатомии ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России. 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41. eLIBRARY.RU SPIN: 6448-9110. https://orcid.org/0000-0002-9590-6678. E-mail: Sergei.Vinnichuk@szgmu.ru
Pathomorphological features of the myocardia in patients with COVID-19
D.S. Evdokimov, S.A.Boldueva, E.D. Resnyanskaya, S.A. Vinnichuk
I.I. Mechnikov North-Western State Medical University; 41 Kirochnaya Str., St. Petersburg, Russian Federation 191015
Summary
Coronavirus disease 2019 (COVID-19) is responsible for high mortality rates worldwide. Although myocardial injury has been demonstrated in critically ill COVID-19 patients, the mechanism of injury as well as morphological changes remain poorly understood. The purpose of the study was to study the morphology of the myocardium according to autopsy data in patients with established COVID-19 infection depending on the troponin level during hospitalization.
Aim. To study autopsy myocardial morphology in patients with established COVID-19 infection, depending on the level of troponin during hospitalization.
Design. Retrospective non-randomized cohort study.
Materials and methods. The medical histories of 66 deceased patients diagnosed with coronavirus infection who were treated at the clinic of I.I. Mechnikov North-Western State Medical University from 05/01/2020 to 07/31/2020. Depending on the level of troponin T taken intravitally, the patients were divided into two groups: the first group — TnT+, which included patients who had an intravitally recorded increase in troponin T of more than 100,000 pg/ml (reference value in our laboratory), and the second group TnT–, it included individuals who did not have a significant increase in troponin T levels. In 22 patients, troponin was not determined, and they were included in the general group of deceased. Clinical manifestations of COVID-19 were analyzed (symptoms, physical examination data, volume of lung damage according to computed tomography, severity of respiratory failure), laboratory parameters, the presence of concomitant pathology, and autopsy results. The autopsy was performed according to a standard protocol, with histological examination of microslides of the lungs, myocardium, liver, kidneys, pancreas and spleen.
Results. A comparative analysis of the TnT+ and TnT– groups showed that patients with elevated troponin levels more often developed disseminated intravascular coagulation (9 and 1, respectively (p = 0.05)), pulmonary embolism (6 and 0, respectively (p = 0, 05)), and thrombosis of other localizations was also detected (6 and 0, respectively (p = 0.05)). In addition, in the TnT+ group, paroxysm of atrial fibrillation developed for the first time during hospitalization against the background of COVID-19 pneumonia. A macroscopic examination of the myocardium of all deceased patients revealed a high prevalence of hypertrophy (56 (84.8%) people) and dilatation (31 (46.9%) people) of the left ventricle. Microscopic examination revealed perivascular fibrosis in 51 (77.3%) patients, intermuscular fibrosis in 38 (57.6%), interstitial edema was diagnosed in 40 (60.6%) people. Signs of damage to medium-sized vessels and microvasculature with the presence of stasis, microthrombosis of intramural myocardial vessels were determined in 10 (15.1%) people. When comparing the results of myocardial autopsy in patients with signs of acute myocardial injury (TnT+ group) and without it (TnT– group), no differences were found. At the same time, in the TnT+ group, signs of endothelitis were more common (p = 0.48), accompanied by microthrombosis and hemorrhages into the myocardium, but the differences were not statistically significant (p = 0.13 and p = 0.64, respectively), which may be due to a small sample of patients.
Conclusion. Which substrate determines the increase in troponins in acute myocardial injury remains unclear, since the compared groups did not differ significantly according to the results of histological examination of the myocardium. Further research using modern diagnostic methods is required.
Key words: myocardial injury, covid-19, autopsy, endotheliitis.
Д.С. Евдокимов, С.А. Болдуева, Е.Д. Реснянская, С.А. Винничук
ФГБОУ ВО «Северо-Западный государственный медицинский университет имени И.И. Мечникова» Министерства здравоохранения Российской Федерации; Россия, г. Санкт-Петербург
Новая коронавирусная инфекция COVID-19 является системным заболеванием и помимо легких поражает другие органы, в том числе и сердечно-сосудистую систему, вовлечение которой существенно ухудшает прогноз заболевания [1]. В литературе описан широкий спектр сердечно-сосудистых осложнений, связанных с COVID-19: острое повреждение миокарда (ОПМ), инфаркт миокарда (ИМ) [2], миокардит, тромбоэмболия легочной артерии (ТЭЛА), различные нарушения ритма и другие [3–7].
Особый интерес для клиницистов представляет понятие ОПМ, которое появилось совсем недавно. Ранее считалось, что ОПМ свойственно конкретным заболеваниям сердца, таким как ИМ, миокардит, эндокардит и т. д. Признаком повреждения миокарда, как известно, является повышение уровня кардиоспецифичных тропонинов выше 99-го перцентиля верхнего референсного предела [8]. Однако, как показывают данные клинической практики, оно не всегда свидетельствует о наличии конкретной патологии сердца и может развиваться на фоне других заболеваний и состояний, например, хронической болезни почек (ХБП), сепсиса, тяжелой дыхательной недостаточности и других [9]. Это представление было сформулировано в Четвертом универсальном определении ИМ 2018 года1.
Решение вопроса о том, является ли повышение кардиоспецифичных тропонинов признаком той или иной нозологической формы заболевания сердца или неспецифическим, определяется совокупностью клинических проявлений и результатов инструментального обследования у каждого конкретного больного. Например, при ИМ это симптомы ишемии миокарда, изменения ЭКГ и данные визуализирующих методов исследования. Повреждение миокарда может быть острым, о чем свидетельствует недавно обнаруженный динамический рост и/или снижение уровня кардиоспецифичных тропонинов, и хроническим — при выявлении их постоянно повышенных показателей2.
Таким образом, ОПМ, возникающее на фоне несердечной патологии, не является самостоятельным нозологическим диагнозом, однако его определение в клинической практике помогает избежать гипердиагностики ИМ. Кроме того, важность выделения понятия ОМП обусловлена тем обстоятельством, что повышение тропонина существенно влияет на прогноз любого основного заболевания, будь то сепсис, ТЭЛА, тяжелая пневмония или другие [10]. Сказанное в полной мере касается и коронавирусной инфекции, при которой, как выявили многие исследования, показатели госпитальной летальности существенно выше у больных, имевших увеличение уровня кардиоспецифичных тропонинов; а встречается этот феномен примерно у 20–30% пациентов, госпитализированных по поводу COVID-19 [8, 11].
Целью настоящего исследования было изучение морфологии миокарда по данным аутопсии у пациентов с установленной инфекцией COVID-19 в зависимости от уровня тропонина за время госпитализации.
Материалы и методы
Ретроспективно были проанализированы истории болезни 66 умерших пациентов, находившихся на лечении в клинике ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России с 01.05.2020 г. по 31.07.2020 г. Диагноз коронавирусной инфекции у всех пациентов был верифицирован по результатам полимеразной цепной реакции на наличие РНК SARS-CoV-2 при заборе материала из носоглотки и ротоглотки, образца бронхоальвеолярного лаважа либо на основании исследования аутопсийного материала.
В зависимости от наличия информации об уровне высокочувствительного тропонина Т были сформированы две группы исследования: группа TnT+, состоявшая из 28 пациентов, у которых прижизненно было зафиксировано повышение тропонина Т более 100,000 пг/мл (референсное значение в нашей лаборатории), и группа TnT–, включившая 16 человек, у которых увеличения уровня тропонина Т не отмечалось. У 22 пациентов тропонин не определялся, и они были включены в общую группу умерших.
Анализировалась следующая информация: клинические проявления COVID-19 (симптомы, данные объективного осмотра, объем поражения легких по заключению компьютерной томографии, выраженность дыхательной недостаточности), лабораторные показатели, наличие сопутствующей патологии, а также результаты аутопсии. Патологоанатомическое исследование проводилось с соблюдением всех предусмотренных мер безопасности, с применением средств индивидуальной защиты. Вскрытие производилось по стандартному протоколу, с гистологическим исследованием микропрепаратов легких, миокарда, печени, почек, поджелудочной железы и селезенки. Образцы тканей для гистологического исследования фиксировались в 10%-ном растворе нейтрального формалина в течение 24 часов. После формирования гистологических блоков на микротоме «Thermo Scientific HM 325» изготавливались гистологические срезы толщиной 3–5 мкм. Для оценки использовалась гистологическая окраска гематоксилином и эозином и световая микроскопия на микроскопе «Micros MC 20» с увеличением ×100 и ×400, а также поляризационная микроскопия.
Статистическую обработку полученных данных осуществляли c использованием программы Statistica 10. Средние величины описаны в виде среднего и стандартного отклонения (M ± SD) либо медианы и квартильного размаха (Me [Q1–Q3]). Для сопоставления частот в группах применяли критерий хи-квадрат. Статистическую значимость различий оценивали с помощью U-теста Манна—Уитни. Критерием статистической достоверности получаемых выводов считали общепринятую в медицине величину р < 0,05.
Результаты
Из 850 пациентов, госпитализированных в центр COVID-19 ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России за период исследования, умерло 66 человек, или 7,8%. Такой уровень летальности сопоставим с данными других авторов [12–14].
Средний возраст умерших составил 72,9 ± 12,4 года, 30 (45,5%) пациентов были мужского пола. Средний срок госпитализации до момента наступления смерти — 12,5 ± 10,6 суток, при этом в отделении реанимации и интенсивной терапии больные находились 8,5 ± 8,3 суток. Терапия всем пациентам проводилась согласно текущим рекомендациям по профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19) Минздрава России3,4.
Среди хронических неинфекционных заболеваний у пациентов с COVID-19 чаще всего встречалась артериальная гипертензия (АГ), хроническая сердечная недостаточность (ХСН), ХБП, сахарный диабет 2-го типа, постинфарктный кардиосклероз (табл.1), что соответствует представленным в литературе данным [17]5.
При сравнении анализируемых групп между ними были выявлены статистически значимые различия по частоте встречаемости ХБП в анамнезе, уровню индекса массы тела, а также по объему поражения легких согласно результатам компьютерной томографии; по остальным анализируемым параметрам группы не различались (табл. 1).
Таблица 1. Характеристика пациентов исследуемых групп при поступлении
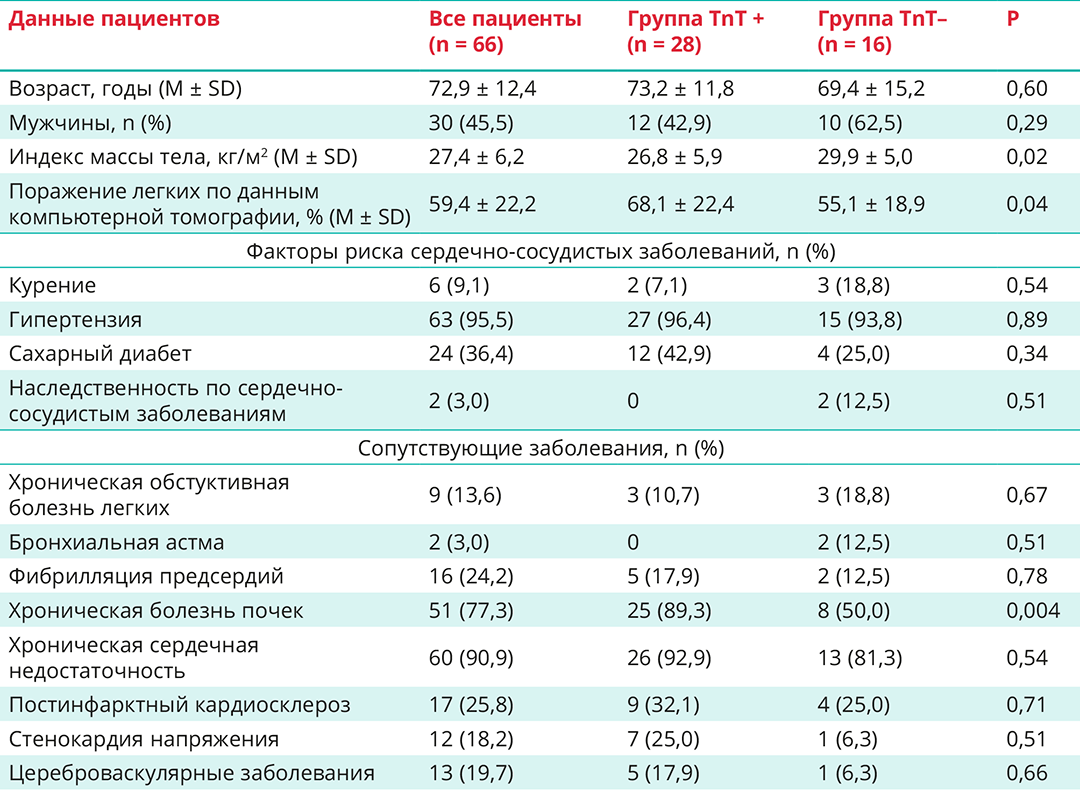
Исходно исследуемые группы не различались по уровню анализируемых лабораторных показателей, однако при анализе максимальных значений было выявлено статистически значимое различие по максимальному показателю тропонина и Д-димера (табл. 2).
Таблица 2. Лабораторные показатели пациентов с COVID-19 при поступлении и их максимальные значения за период госпитализации, Me [Q1–Q3]

По данным патологоанатомического исследования непосредственной причиной смерти у подавляющего большинства (60 (90,9%)) пациентов был острый респираторный дистресс-синдром (ОРДС), морфологические признаки которого соответствовали приведенным в литературе [15]. Другой наиболее частой причиной летальности была острая сердечная недостаточность — у 6 (9,1%) больных.
Среди осложнений, развившихся за время госпитализации, наиболее часто отмечались внутригоспитальная бактериальная пневмония, ДВС-синдром, у каждого пятого пациента — сепсис, тромбозы различной локализации (табл. 3). Тромбы при аутопсии находили в полости правого предсердия, левого желудочка, в ушке левого предсердия, в мелких сосудах легких, в венах малого таза, в приносящих артериолах почек, мелких ветвях брыжеечной артерии; при этом у одного из умерших тромбоз привел к инфаркту тонкой кишки на протяжении 40 см. У 10 пациентов (15,1%) была ТЭЛА артерий мелкого и среднего калибра.
Сравнительный анализ групп TnT+ и TnT– показал, что у пациентов с повышенным уровнем тропонина чаще развивались ДВС-синдром, ТЭЛА, а также обнаруживались тромбозы других локализаций. Помимо этого, в группе TnT+ за время госпитализации на фоне пневмонии COVID-19 впервые развивался пароксизм фибрилляции предсердий (табл. 3).
Таблица 3. Осложнения в исследуемых группах за время госпитализации, n (%)
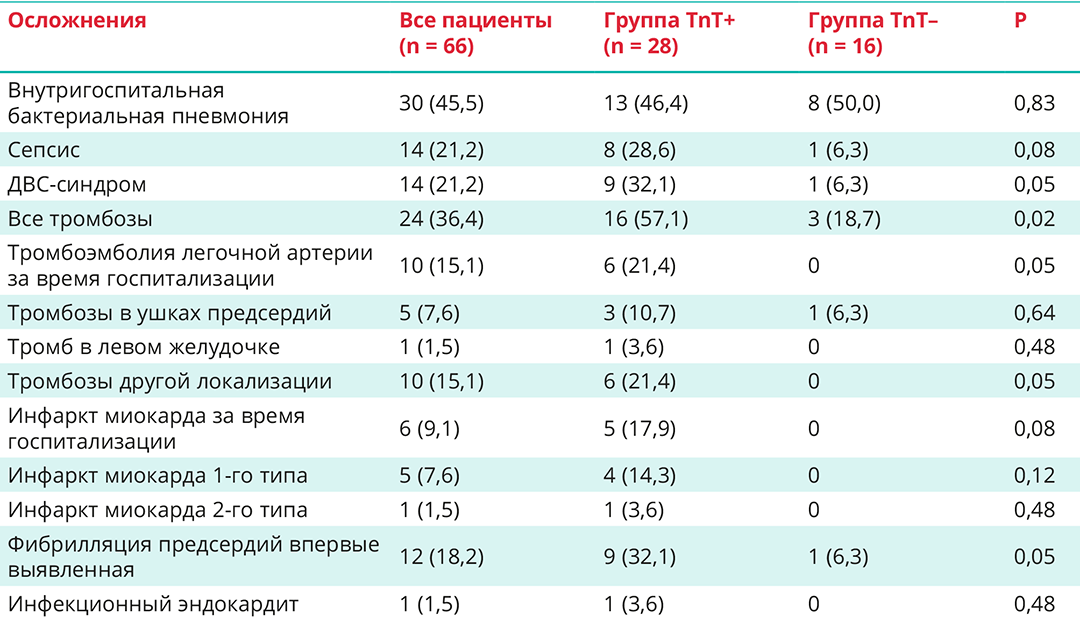
Примечание: у одного пациента инфаркт миокарда был выявлен посмертно, кардиоспецифичные тропонины не исследовались.
При макроскопическом исследовании миокарда выявлена высокая распространенность гипертрофии (у 56 (84,8%) человек) и дилатации (в 31 (46,9%) случае) левого желудочка. Гемодинамически значимый стеноз (стеноз более 75% просвета сосуда) коронарных артерий встречался у 16 (24,2%) пациентов. Микроскопическое исследование выявило периваскулярный фиброз у 51 (77,3%) пациента, а межмышечный — у 38 (57,6%), интерстициальный отек диагностирован у 40 (60,6%) человек. Признаки поражения сосудов среднего калибра и микроциркуляторного русла с наличием стаза, микротромбозами интрамуральных сосудов миокарда определялись у 10 (15,1%) человек (табл. 4). Как уже упоминалось выше, у 5 пациентов были микроскопические признаки острого ИМ с наличием гранулоцитарной инфильтрации, а у 1 — признаки инфекционного эндокардита с микроабсцессами эндокарда. Убедительных признаков миокардита, перикардита у исследуемых больных не наблюдалось.
Таблица 4. Макроскопические и микроскопические данные аутопсии миокарда в исследуемых группах
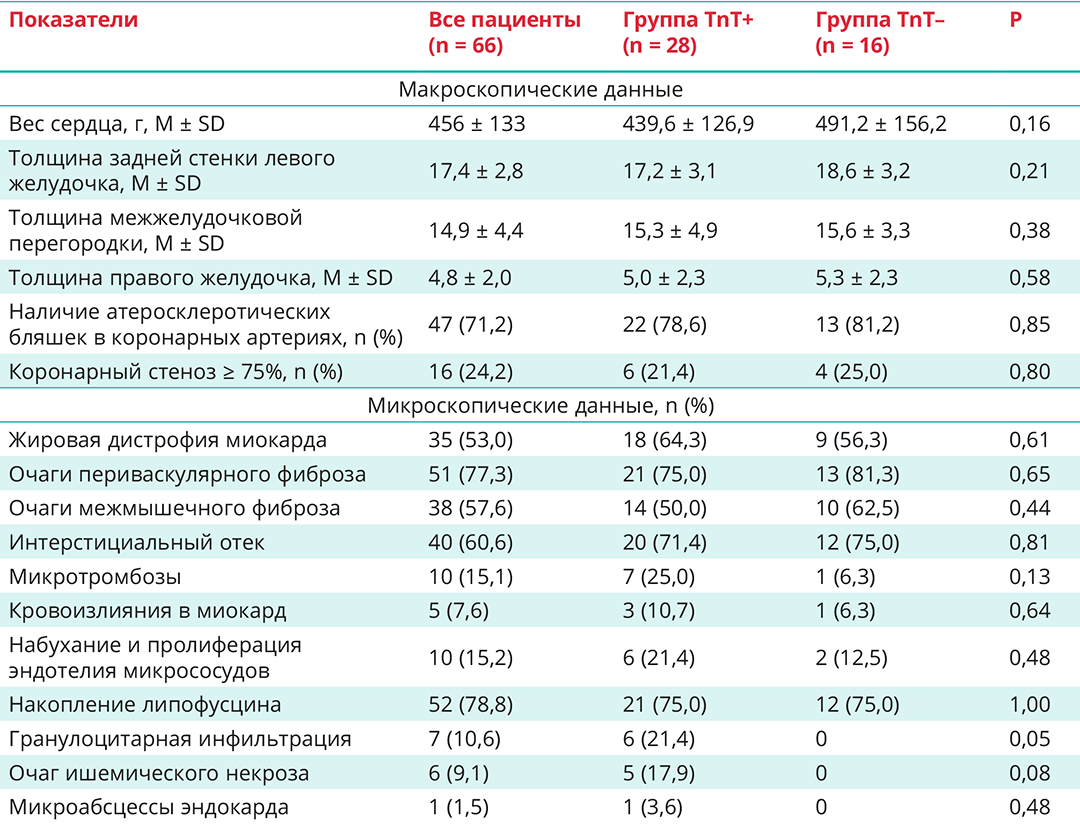
Примечание: у одного пациента инфаркт миокарда был выявлен посмертно, кардиоспецифичные тропонины не исследовались.
При сравнении результатов аутопсии миокарда у больных с признаками ОПМ (группа TnT+) и без такового (группа TnT–) статистически значимых различий выявлено не было (табл. 4). Вместе с тем в группе TnT+ чаще встречались микротромбозы и кровоизлияния в миокард, а также набухание и пролиферация эндотелия микрососудов, очаговая гранулоцитарная инфильтрация миокарда.
Обсуждение
Согласно полученным данным, у 63 (95,5%) пациентов, включенных в исследование, были выявлены сопутствующие сердечно-сосудистые заболевания (АГ, ишемическая болезнь сердца (ИБС), ХСН). Из 44 человек, у которых прижизненно исследовались тропонины, в 28 (63,6%) случаях диагностировано ОПМ (тропонин Т > 99-го перцентиля верхней границы нормы). Еще в одном случае тропонин не определялся, однако по данным аутопсии обнаружен острый инфаркт миокарда (ОИМ). Эти данные в настоящее время хорошо известны и соответствуют информации отечественных и зарубежных авторов [8, 16]6. Повреждение миокарда при коронавирусной инфекции объясняется различными механизмами: непосредственном повреждающим действием вируса на сосуды и миокард, провоспалительным статусом, цитокиновым штормом, гипоксией в связи с ОРДС, гиперактивацией симпатоадреналовой системы, а также прокоагулянтным статусом с развитием микротромбозов [17, 18].
В настоящем исследовании ОПМ морфологически было представлено ОИМ у 9,1% из всех умерших (у 5 больных из группы TnT+ и у 1 пациента, которому тропонин не исследовался), при этом в 5 случаях установлен ОИМ 1-го типа, в одном — 2-го типа. Как известно, одной из причин ИМ 1-го типа при COVID-19 у пациентов с ИБС в анамнезе может быть дестабилизация бляшек, связанная с системным воспалением, гипоксией и цитокиновым штормом [19]. Для возникновения ИМ 2-го типа у пациентов с вирусной инфекцией COVID-19 так же, как и для ОПМ, имеется множество причин: гипоксемия, анемия, воспаление, микротромбоваскулиты, гемодинамические нарушения и другие [20].
Повреждение миокарда в настоящем исследовании наблюдалось также при инфекционном эндокардите у одного пациента с умеренным повышением тропонина (максимально до 160 пг/мл.). Проявлений миокардита и перикардита у исследуемых больных, как указывалось, не было.
Вместе с тем информации о характере поражения миокарда у пациентов с повышением тропонинов (если не брать во внимание такие очевидные причины, как ОИМ, миокардит, инфекционный эндокардит), включая результаты аутопсий, по данным литературы, очень мало. Описываются такие признаки, как тромбоваскулиты, инфильтрация гранулоцитами и моноцитами, мелкоочаговые некротические изменения [21–24]. В связи с этим представляло интерес изучить характер повреждения миокарда у пациентов с коронавирусной инфекцией по данным аутопсии.
У 22 пациентов в группе TnT+ специфических морфологических признаков, характерных для самостоятельного заболевания миокарда, найдено не было. Мы прицельно сравнили характер морфологических изменений миокарда у пациентов группп TnT+ и TnT–, однако достоверные различия не были выявлены. В обеих группах обращали на себя внимание такие признаки, как периваскулярный/межмышечный фиброз, дистрофия и накопление липофусцина, обусловленные, вероятно, наличием хронических ишемических расстройств. Тем не менее, следует выделить такие признаки, как гранулоцитарная инфильтрация миокарда, микротромбозы в микрососудистом русле и кровоизлияния в миокард, а также выраженная пролиферация эндотелия микрососудов, которые встречались почти у каждого четвертого пациента в группе TnT+ в отличие от больных сравниваемой группы. Эти изменения в микрососудистом русле в последнее время называют эндотелиитом, который объясняет поражение не только миокарда, но и микрососудов других органов [22, 23, 25]. Они описаны в недавней работе Л.Б. Митрофановой и соавт., представляющей результаты гистохимического и иммунологического анализов аутопсийного материала [22].
К сожалению, в связи с эпидемиологической обстановкой и большой нагрузкой на патологоанатомическую службу в период проведения работы нам не удалось выполнить иммуногистохимическое исследование, электронную микроскопию полученного материала, идентификация вирусного генома также не проводилась. Вероятно, именно эти методы позволили бы выявить нарушения в ультраструктуре миокарда при его повреждении, обусловленном коронавирусной инфекцией, что подчеркивает важность более широкого использования иммуногистохимических, молекулярно-генетических и электронномикроскопических методов изучения аутопсийного материала.
Можно ли связать повышение тропонина с явлениями эндотелиита? На наш взгляд, да. В норме определенная часть внутриклеточного тропонина находится в связанном состоянии с миофиламентами, другая же свободно располагается в цитозоле клетки. Повышение содержания тропонина в крови, таким образом, может быть связано не только с некрозом кардиомиоцитов, сопровождающимся разрывом миофиламентов, но и с утечкой цитозольного тропонинового пула из-за повышения проницаемости сарколеммы при эндотелиите, возникающем за счет действия эндотоксинов, цитокинов, а также активных радикалов кислорода [11].
Заключение
Поскольку сравниваемые группы статистически значимо не различались по результатам гистологического исследования миокарда, какой субстрат определяет повышение тропонинов при ОПМ, остается до конца неясным. Отмечено, что в группе TnT+ чаще встречались признаки эндотелиита, сопровождавшегося микротромбозами и кровоизлияниями в миокард, однако различия не были статистически значимыми, что, возможно, обусловлено небольшой выборкой пациентов. Требуется проведение дальнейших исследований с применением современных диагностических методов.
1 Thygesen K., Alpert J.S., Jaffe A.S., Chaitman B.R. et al. Fourth Universal Definition of Myocardial Infarction (2018). Circulation. 2018;138(20):e618–51. DOI: 10.1161/CIR.0000000000000617
2 Там же
3 Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)». Версия 6 (28.04.2020). URL: https://www.arfpoint.ru/wp-content/uploads/2020/04/28042020_mr_covid-19_v6.pdf (дата обращения: 17.05.2024)
4 Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)». Версия 7 (03.06.2020). URL: https://nasci.ru/?id=12809&download=1 (дата обращения: 17.05.2024)
5 Арутюнов Г.П., Тарловская Е.И., Арутюнов А.Г., Беленков Ю.Н. и др. Международный регистр «Анализ динамики коморбидных заболеваний у пациентов, перенесших инфицирование SARS-CoV-2 (AКТИВ SARS-CoV-2)»: анализ 1000 пациентов. Российский кардиологический журнал. 2020;25(11):4165. DOI: 10.15829/1560-4071-2020-4165
6 Там же
Предыдущая статья
М.С. Тюрюпов, К.С. Шуленин, Т.С. Свёклина, Г.Г. Кутелев, Д.К. Шуленин, А.Е. Аланичев, Д.В. Черкашин ...
Следующая статья
С.С. Байрамова1, О.В. Цыганкова1, 2, К.Ю. Николаев1, О.В. Тимощенко...