Метаболические аспекты жировой болезни поджелудочной железы
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- междольковый жир — наличие клеток, накапливающих липиды, между дольками ПЖ;
- липидные капли внутри ацинарных или островковых клеток ПЖ;
- трансдифференцировка ацинарных клеток ПЖ в адипоциты;
- замещение мертвых ацинарных клеток ПЖ жировой тканью [1].
- 1А (35% пациентов) — накопление жировой ткани преимущественно в головке ПЖ;
- 1В (35% пациентов) — накопление жировой ткани в головке и теле ПЖ;
- 2А (12% пациентов) — накопление жировой ткани в головке, теле и крючковидном отростке ПЖ;
- 2B (18%) — предполагает жировую инфильтрацию всех частей ПЖ, но с сохранением перибилиарной области.
- Литература
- Petrov M.S., Taylor R. Intra-pancreatic fat deposition: bringing hidden fat to the fore. Nat. Rev. Gastroenterol. Hepatol. 2022;19(3):153–68. DOI: 10.1038/s41575-021-00551-0
- Ogilvie R.F. The islands of Langerhans in 19 cases of obesity. J. Pathol. Bacteriol. 1933;12(3):473–81. DOI:1002/path.1700370314
- Olsen T.S. Lipomatosis of the pancreas in autopsy material and its relation to age and overweight. Acta Pathol. Microbiol. Scand. A. 1978;86A:367–73. DOI: 10.1111/j.1699-0463.1978.tb02058.x
- Sotoudehmanesh R., Tahmasbi A., Sadeghi A., Hosseini H. et al. The prevalence of nonalcoholic fatty pancreas by endoscopic ultrasonography. Pancreas. 2019;48(9):1220–4. DOI: 10.1097/MPA.0000000000001396
- Dite P., Blaho M., Bojkova M., Jabandziev P. et al. Nonalcoholic fatty pancreas disease: clinical consequences. Dig. Dis. 2020;38(2):143–9. DOI: 10.1159/000505366
- Pham Y.H., Bingham B.A., Bell C.S., Greenfield S.A. et al. Prevalence of pancreatic steatosis at a pediatric tertiary care center. South. Med. J. 2016;109(3):196–8. DOI: 10.14423/SMJ.0000000000000432
- Mahyoub M.A., Elhoumed M., Maqul A.H, Almezgagi M. et al. Fatty infiltration of the pancreas: a systematic concept analysis. Front. Med. (Lausanne). 2023;10:1227188. DOI: 10.3389/fmed.2023.1227188
- Wong V.W., Wong G.L., Yeung D.K., Abrigo J.M. et al. Fatty pancreas, insulin resistance, and b-cell function: a population study using fat-water magnetic resonance imaging. Am. J. Gastroenterol. 2014;109(4):589–97. DOI: 10.1038/ajg.2014.1
- Caldart F., de Pretis N., Luchini C., Ciccocioppo R. et al. Pancreatic steatosis and metabolic pancreatic disease: a new entity? Intern. Emerg. Med. 2023;18(8):2199–208. DOI: 10.1007/s11739-023-03364-y
- Fraulob J.C., Ogg-Diamantino R., Fernandes-Santos C., Trindade M. et al. A mouse model of metabolic syndrome: insulin resistance, fatty liver and non-alcoholic fatty pancreas disease (NAFPD) in C57BL/6 mice fed a high fat diet. J. Clin. Biochem. Nutr. 2010;46(3):212–23. DOI: 3164/jcbn.09-83
- Zhang X., Cui Y., Fang L., Li F. Chronic high-fat diets induce oxide injuries and fibrogenesis of pancreatic cells in rats. Pancreas. 2008;37(3):e31–8. DOI: 10.1097/MPA.0b013e3181744b50
- Pinnick K.E., Collins S.C., Londos C., Gauguier D. et al. Pancreatic ectopic fat is characterized by adipocyte infiltration and altered lipid composition. Obesity (Silver Spring). 2008;16(3):522–30. DOI: 10.1038/oby.2007.110
- Sakai N.S., Taylor S.A., Chouhan M.D. Obesity, metabolic disease and the pancreas — quantitative imaging of pancreatic fat. Br. J. Radiol. 2018;91: 20180267. DOI: 10.1259/bjr.20180267
- Zhu S.J., Ding Z. Association between gut microbiota and seven gastrointestinal diseases: a Mendelian randomized study. J. Gene Med. 2024;26(1):e3623. DOI: 10.1002/jgm.3623
- Ефимова О.В., Григорьева И.Н., Тов Н.Л., Суворова Т.С. и др. Липиды, печень и поджелудочная железа на перекрестке эпидемий метаболического синдрома и ожирения. Атеросклероз. 2020;16(4):77–84. Efimova O.V., Grigorieva I.N., Tov N.L., Suvorova T.S. et al. Lipids, liver and pancreas at the crossroads of the epidemics of metabolic syndrome and obesity. Atherosclerosis. 2020;16(4):77–84. (in Russian). DOI: 10.15372/ATER20200410
- Sepe P.S., Ohri A., Sanaka S., Berzin T.M. et al. A prospective evaluation of fatty pancreas by using EUS. Gastrointest. Endosc. 2011;73(5):987–93. DOI: 10.1016/j.gie.2011.01.015
- Singh R.G., Yoon H.D., Poppitt S.D., Plank L.D. et al. Ectopic fat accumulation in the pancreas and its biomarkers: a systematic review and meta-analysis. Diabetes Metab. Res. Rev. 2017;33:e2918. DOI: 10.1002/dmrr.2918
- Wang C.Y., Ou H.Y., Chen M.F., Chang T.C. et al. Enigmatic ectopic fat: prevalence of nonalcoholic fatty pancreas disease and its associated factors in a Chinese population. J. Am. Heart Assoc. 2014;3(1):e000297. DOI: 1161/JAHA.113.000297
- Chan T.T., Tse Y.K., Lui R.N., Wong G. et al. Fatty pancreas is independently associated with subsequent diabetes mellitus development: a 10-year prospective cohort study. Clin. Gastroenterol. Hepatol. 2022;20(9):2014–2022.e4. DOI: 10.1016/j.cgh.2021.09.027
- Taylor R., Holman R.R. Normal weight individuals who develop type 2 diabetes: the personal fat threshold. Clin. Sci. (Lond.). 2015;128(7):405–10. DOI: 10.1042/CS20140553
- Lee J.S., Kim S.H., Jun D., Korantzis I. et al. Clinical implications of fatty pancreas: correlations between fatty pancreas and metabolic syndrome. World J. Gastroenterol. 2009;15(15):1869–75. DOI: 3748/wjg.15.1869
- Kul S., Karadeniz A., Dursun İ., Sahin S. et al. Non-alcoholic fatty pancreas disease is associated with increased epicardial adipose tissue and aortic intima-media thickness. Acta Cardiol. Sin. 2019;35(2):118–25. DOI: 6515/ACS.201903_35(2).20181009A
- Sahin S., Yerlikaya M.G., Ozderya A., Cavusoglu I.G. et al. Non-alcoholic fatty pancreas disease is associated with SYNTAX score in acute coronary syndrome. Acta Cardiol. Sin. 2022;38(6):683–90. DOI: 10.6515/ACS.202211_38(6).20220424A
- Sun P.T., DU X.C., Wang R.D., Sun Y. et al. Zhongguo Yi Xue Ke Xue Yuan Xue Bao. 2020;42(2):172–7. (in Chinese). DOI: 10.3881/j.issn.1000-503X.11524
- Lee E.H., Kim J.Y., Yang H.R. Ectopic pancreatic fat as a risk factor for hypertension in children and adolescents with nonalcoholic fatty liver disease. J. Clin. Hypertens. 2021;23(8):1506–15. DOI: 10.1111/jch.14326
- Romana B.S., Chela H., Dailey F.E., Nassir F. et al. Non-alcoholic fatty pancreas disease (NAFPD): a silent spectator or the fifth component of metabolic syndrome? A literature review. Endocr. Metab. Immune Disord. Drug Targets. 2018;18(6):547–54. DOI: 10.2174/1871530318666180328111302
- Пиманов С.И. Стеатоз поджелудочной железы — «белое пятно» панкреатологии. Медицинский совет. 2014;11:22–6. Pimanov S.I. Pancreatic steatosis — a "white spot" of pancreatology. Medical Council. 2014;11:22–6. (in Russian)
- Wagner R., Eckstein S.S., Yamazaki H., Gerst F. et al. Metabolic implications of pancreatic fat accumulation. Nat. Rev. Endocrinol. 2022;18(1):43–54. DOI: 10.1038/s41574-021-00573-3
- Rugivarodom M., Geeratragool T., Pausawasdi N., Charatcharoenwitthaya P. Fatty pancreas: linking pancreas pathophysiology to nonalcoholic fatty liver disease. J. Clin. Transl. Hepatol. 2022;10(6):1229– DOI: 10.14218/JCTH.2022.00085
- Rossi A.P., Fantin F., Zamboni G.A., Mazzali G. et al. Effect of moderate weight loss on hepatic, pancreatic and visceral lipids in obese subjects. Nutr. Diabetes. 2012;2(3):e32. DOI: 10.1038/nutd.2012.5
- Jiang Y., Spurny M., Schübel R., Nonnenmacher T. et al. Changes in pancreatic fat content following diet-induced weight loss. Nutrients. 2019;11(4):912. DOI: 10.3390/nu11040912
- Gepner Y., Shelef I., Schwarzfuchs D., Zelicha H. et al. Effect of distinct lifestyle interventions on mobilization of fat storage pools: central magnetic resonance imaging randomized controlled trial. Circulation. 2018;137:1143–57. DOI: 10.1161/CIRCULATIONAHA.117.030501
- Heiskanen M.A., Motiani K.K., Mari A., Saunavaara et al. Exercise training decreases pancreatic fat content and improves beta cell function regardless of baseline glucose tolerance: a randomised controlled trial. Diabetologia. 2018;61(S1):1817–28. DOI: 10.1007/s00125-018-4627-x
- Salman A.A., Salman M.A., Said M., El Sherbiny M. et al. Improvement of pancreatic steatosis and indices of insulin resistance after metabolic surgery. Front. Med. (Lausanne). 2022;9:894465. DOI: 10.3389/fmed.2022.894465
- Pinte L., Balaban D.V., Băicuş C., Jinga M. Non-alcoholic fatty pancreas disease — practices for clinicians. Rom. J. Intern. Med. 2019;57(3):209– DOI: 10.2478/rjim-2019-0005
- Gao Y., Hou L., Wang Y., Guo S. et al. Octreotide alleviates pancreatic damage caused by paraquat in rats by reducing inflammatory responses and oxidative stress. Environ. Toxicol. Pharmacol. 2020;80:103456. DOI: 10.1016/j.etap.2020.103456
- Ramkissoon R., Gardner T.B. Pancreatic steatosis: an emerging clinical entity. Am. J. 2019;114(11):1726–34. DOI: 10.14309/ajg.0000000000000262
Цель обзора. Актуализировать представление о неалкогольной жировой болезни поджелудочной железы как важного компонента развития и поддержания метаболического синдрома, представить современные данные о связи данной патологии с сердечно-сосудистыми рисками, обозначить подходы к диагностике и лечению.
Основные положения. Метаболический синдром является одной из наиболее распространенных патологий, существенно увеличивающих сердечно-сосудистые риски. Известно, что избыточное накопление липидов в поджелудочной железе у пациентов с метаболическим синдромом неизбежно влечет за собой нарушение функционирования бета-клеток. Тем не менее, термин, характеризующий собой метаболическую дисфункцию поджелудочной железы на фоне ее стеатоза, введен в обращение сравнительно недавно. Таким образом, неалкогольная жировая болезнь поджелудочной железы приобретает свои дефиниции, отличающие ее от традиционного морфологического подхода, заключающегося в большей степени в оценке содержания доли жировой ткани, но не в связи с компонентами метаболического синдрома. Известно, что у пациентов с неалкогольной жировой болезнью поджелудочной железы чаще встречается сахарный диабет 2-го типа, артериальная гипертензия и атеросклероз. Вероятно, патогенез ее развития также тесно связан с неалкогольной жировой болезнью печени.
Заключение. Неалкогольная жировая болезнь поджелудочной железы, являясь одним из ключевых механизмов метаболической дисфункции, требует дальнейшего исследования с целью определения профилактической и лечебной тактики.
Ключевые слова: инсулинорезистентность, метаболический синдром, неалкогольная жировая болезнь поджелудочной железы, стеатоз поджелудочной железы
Скачать PDFМозгунова В.С., Семикова Г.В., Волкова А.Р., Халимов Ю.Ш. Метаболические аспекты жировой болезни поджелудочной железы. Вестник терапевта. 2024. № 1 (62). DOI: 10.31550/2712-8601-VT-2024-1-1. URL: https://journaltherapy.ru/statyi/metabolicheskie-aspekty-zhirovoj-bolezni-podzheludochnoj-zhelezy/ (дата обращения: дд.мм.гггг)
Мозгунова Валентина Сергеевна — ассистент кафедры терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6-8. http://orcid.org/0000-0002-0841-3438. E-mail: sidelnikovavalya@mail.ru
Семикова Галина Владимировна (автор для переписки) — к. м. н., ассистент кафедры терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6-8. eLIBRARY.RU SPIN: 4534-0974. http://orcid.org/0000-0003-0791-4705. E-mail: Semikovagv@yandex.ru
Волкова Анна Ральфовна — д. м. н., профессор кафедры терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6-8. eLIBRARY.RU SPIN: 4007-1288. http://orcid.org/0000-0002-5189-9365. E-mail: volkovaa@mail.ru
Халимов Юрий Шавкатович — д. м. н., профессор, заведующий кафедрой терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6-8. eLIBRARY.RU SPIN: 7315-6746. http://orcid.org/0000-0002-7755-7275. E-mail: yushkha@gmail.com
Metabolic aspects of fatty pancreatic disease
V.S. Mozgunova, G.V. Semikova, Y.Sh. Khalimov, A.R. Volkova
Pavlov First Saint Petersburg State Medical University; 6–8 L’va Tolstogo Str., Saint Petersburg, Russian Federation 197022
Abstract
Aim. To update the understanding of non-alcoholic fatty pancreatic disease as an important component of the development and maintenance of metabolic syndrome, to present current data on the connection of this pathology with cardiovascular risks, and to outline approaches to diagnosis and treatment.
Key points. Metabolic syndrome is one of the most common pathologies that significantly increases cardiovascular risks. It is known that excessive accumulation of lipids in the pancreas in patients with metabolic syndrome inevitably entails impaired functioning of beta cells. However, the term characterizing metabolic dysfunction of the pancreas against the background of its steatosis was introduced into circulation relatively recently. Thus, non-alcoholic fatty pancreatic disease acquires its own definitions that distinguish it from the traditional morphological approach, which consists more in assessing the content of the proportion of adipose tissue, but not the connection with the components of the metabolic syndrome. It is known that patients with non-alcoholic fatty pancreatic disease are more likely to have type 2 diabetes mellitus, arterial hypertension and atherosclerosis. Probably, the pathogenesis of its development is also closely related to non-alcoholic fatty liver disease.
Conclusion. Non-alcoholic fatty pancreatic disease, being one of the key mechanisms of metabolic dysfunction, requires further research in order to determine preventive and therapeutic tactics.
Key words: insulin resistance, non-alcoholic fatty pancreatic disease, pancreatic steatosis, metabolic syndrome.
В.С. Мозгунова, Г.В. Семикова, А.Р. Волкова, Ю.Ш. Халимов
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения Российской Федерации; Россия, г. Санкт-Петербург
Метаболический синдром (МС) — одна из наиболее часто встречающихся патологий в практике врача терапевтической специальности. Компоненты МС хорошо известны: абдоминальное ожирение, инсулинорезистентность, нарушения углеводного обмена, артериальная гипертензия и дислипидемия. Каждый из этих факторов сам по себе способен увеличивать сердечно-сосудистый риск, однако сочетание их приводит к взаимному усугублению патологических состояний, что может драматически ускорить развитие сердечно-сосудистых катастроф.
С учетом того, что ни один орган не способен избежать негативного влияния МС, в последние годы особое внимание уделяется метаболическому состоянию отдельных систем организма в условиях инсулинорезистентности и дислипидемии. В частности, известно, что неалкогольная жировая болезнь печени (НАЖБП) является частым спутником МС; более того, наличие НАЖБП ухудшает течение нарушений углеводного обмена и способно усугублять инсулинорезистентность. С другой стороны, специфической перестройке подвергается и поджелудочная железа (ПЖ), однако данные относительно места жировой инфильтрации ПЖ в патогенезе МС в настоящее время достаточно ограничены. Отчасти это может быть связано с отсутствием четкого понимания морфологических и клинических последствий панкреатической жировой эктопии.
Цель данного обзора заключается в формулировке определения неалкогольной жировой болезни поджелудочной железы (НАЖБПЖ), представлении современных литературных данных о ее эпидемиологии, патогенезе и связи с компонентами МС, диагностических подходах и перспективах лечения данного состояния.
Дефиниции
В норме жировая ткань составляет 3–5,5% (или 10–15 г) от веса ПЖ. Жир, содержащийся в ПЖ, состоит в основном из триглицеридов, свободных жирных кислот и общего холестерина [1]. Избыточное накопление липидов в ПЖ не является строго специфическим отражением метаболических заболеваний и нередко становится следствием токсических влияний (как правило, избыточного употребления алкоголя), вирусных и некоторых других заболеваний.
Первые данные относительно накопления жировой ткани в ПЖ были представлены результатами аутопсийных исследований в первой половине прошлого века. В 1926 году J.H. Schaefer описал корреляцию между массой ПЖ и массой тела, а в 1933 году R.F. Ogilvie отметил, что у лиц с ожирением по сравнению с худыми содержание жира в ткани ПЖ почти в два раза выше [2]. Последующие аутопсийные исследования позволили связать накопление жира в ПЖ с пожилым возрастом; кроме того, была выявлена связь этого патологического состояния с нарушениями углеводного обмена и тяжелым генерализованным атеросклерозом.
В 1978 году T.S. Olsen обратил внимание на неоднородность распределения жировой ткани в ПЖ у лиц в зависимости от возраста и выраженности ожирения, на основании чего им была разработана классификация стеатоза ПЖ, которой врачи-морфологи пользуются и в настоящее время [3]. Жировая инфильтрация ПЖ определяется как сочетание следующих характеристик:
Встречающиеся в литературе термины «стеатоз ПЖ», «жировая инфильтрация ПЖ», «липоматоз ПЖ» отражают в основном морфологические изменения, однако не указывают на патогенез этого состояния у пациентов с МС. Таким образом, назрела клиническая необходимость создания термина, который был бы способен описать патологическое состояние ПЖ, не связанное с фактом употребления алкоголя, но возникающее вследствие избыточного отложения липидов в ее паренхиме на фоне ряда метаболических нарушений (инсулинорезистентности, ожирения, нарушения углеводного обмена). По аналогии с НАЖБП, отражающей избыточное накопление липидов в паренхиме печени у пациентов, специалистами был предложен термин «НАЖБПЖ», который в настоящее время определяется как эктопия жировой ткани в ПЖ на фоне ожирения и МС, а неалкогольный стеатопанкреатит (по аналогии с неалкогольным стеатогепатитом) — как воспаление ПЖ, обусловленное накоплением в ней жировой ткани.
Эпидемиология и факторы риска
В связи с относительно новым понятием НАЖБПЖ точно оценить эпидемиологические данные затруднительно. Сведения о ее распространенности в различных исследованиях варьируют от 12,9 до 41% среди взрослого населения [4, 5]. В эпидемиологическом исследовании Y.H. Pham и соавт. частота НАЖБПЖ составила 8% у детей без ожирения и 19% — у детей с ожирением, при этом выявлялась ее связь с развитием НАЖБП [6].
Многие работы, в которых оценивается распространенность НАЖБПЖ, также содержат сведения и о НАЖБП у обследованных пациентов. Так, отмечено, что НАЖБПЖ выявляется у 50–80% больных с неалкогольным стеатогепатитом [7]. В ряде исследований было выявлено, что содержание жира в ПЖ у мужчин выше, чем у женщин. При этом у мужчин НАЖБПЖ чаще всего выявляется в возрасте 40–49 лет, а у женщин — после наступления менопаузы [8, 9].
К факторам риска НАЖБПЖ относят общее и висцеральное ожирение, наличие ожирения у матери, высокожировую диету. В связи со значимым вкладом НАЖБП в патогенез инсулинорезистентности ее также можно считать фактором риска развития НАЖБПЖ. Поскольку и в экспериментах на животных, и в реальной клинической практике при ожирении выявляются оба состояния, установить степень их взаимного влияния затруднительно, несомненна лишь их негативная взаимодополняющая роль в патогенезе МС [10].
Патогенез
У большинства пациентов развитие НАЖБПЖ тесно ассоциировано с ожирением. Накопление липидов в адипоцитах подкожной жировой клетчатки приводит к их гипертрофии, при этом цитокиновый профиль адипоцитов приобретает высокой провоспалительный потенциал за счет гиперэкспрессии фактора некроза опухоли-α (ФНО-α), С-реактивного белка, интерлейкина-6 и др. на фоне значительного снижения секреции адипонектина (адипоцитокина с противовоспалительной активностью). Локальное воспаление, апоптоз и некроз подкожных адипоцитов, нарушение васкуляризации подкожной жировой клетчатки приводят к тому, что накопление липидов смещается в висцеральные депо — в частности, в междольковое пространство ПЖ. В экспериментах на животных установлено, что высокожировая диета приводит к междольковому накоплению липидов, повышению активности воспалительных и фибротических процессов в ПЖ, а также развитию инсулинорезистентности [11]. Так, в работе K.E. Pinnick и соавт. крысам назначалась высокожировая диета в течение 15 недель. После выведения животных из эксперимента и исследования внутренних органов было установлено, что жировая инфильтрация в ПЖ была выражена в 5 раз сильнее, чем в печени [12]. Нельзя исключить, что ткань ПЖ более чувствительна к высокожировому питанию, чем ткань печени применительно к грызунам, хотя аналогичные результаты еще не установлены на человеческой популяции.
Жировая ткань, локализованная висцерально (в том числе интраорганно, как в случае НАЖБПЖ и НАЖБП), существенно отличается от подкожных жировых депо. В частности, секреторный профиль висцеральной жировой ткани имеет провоспалительную активность, доля иммунных клеток в ней выше, а окислительный стресс более выражен. Таким образом, локальный уровень ФНО-α, интерлейкина-6 и моноцитарного хемотаксического белка-1 в ткани ПЖ возрастает, что приводит к постоянному рекрутированию макрофагов в инфильтрированную дисфункциональным жиром ПЖ [13]. Активированные макрофаги секретируют интерлейкин-1β и миелопероксидазу, приводя к поддержанию и усугублению воспалительной реакции. Указанные компоненты патогенеза отражены на рисунке 1.
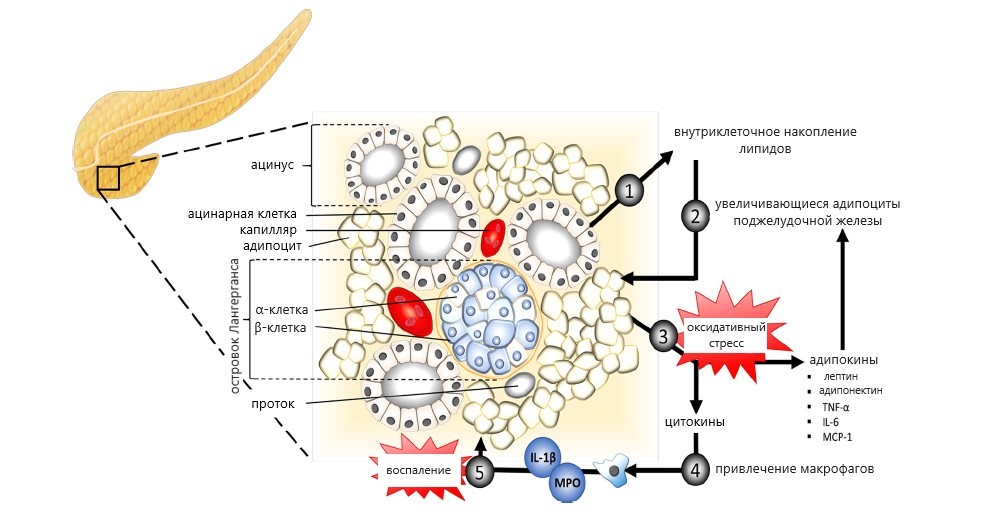
Рис. 1. Патофизиологические механизмы неалкогольной жировой болезни поджелудочной железы (адаптировано из N.S. Sakai и соавт., 2018 [13])
Примечание: MCP-1 — моноцитарный хемотаксический белок-1; TNF-α — фактор некроза опухоли-α; IL-6 — интерлейкин-6; IL-1β — интерлейкин-1β; MPO — миелопероксидаза.
Интрапанкреатический жир, кроме того, играет важную роль в развитии панкреатита: липазы, выделяемые ацинарными клетками на фоне их повреждения, усиливают выраженность интрапанкреатического липолиза, в паренхиме ПЖ увеличивается содержание свободных жирных кислот, особенно ненасыщенных, что оказывает прямое токсическое действие на ацинарные клетки («липолитический поток»), приводя к ацинарному некрозу.
В последние годы большое внимание уделяется влиянию микробиома кишечника на метаболическое здоровье. В работе M. Signoretti и соавт. отмечается связь между активностью воспалительных процессов в ПЖ и микробным составом кишки, однако авторы делают акцент на течении хронического панкреатита, отмечая, что данные относительно связи стеатоза ПЖ и микробиома кишки освещены в литературе достаточно скудно [14].
Связь с компонентами метаболического синдрома и сердечно-сосудистыми заболеваниями
Как было указано выше, развитие НАЖБПЖ тесно взаимосвязано с процессами инсулинорезистентности и липотоксичности, типичными для МС. Распространенность MC среди пациентов с НАЖБПЖ составляет 59,2–76,9%. НАЖБПЖ также ассоциирована с гипергликемией, и, по данным ряда исследователей, может выявляться у трети больных с сахарным диабетом (СД) 2-го типа [15]. В исследовании P.S. Sepe и соавт. при обследовании 250 пациентов МС расценивался как важный фактор риска развития НАЖБПЖ, а ожирение и НАЖБП были независимо взаимосвязаны с частотой развития НАЖБПЖ. При этом у больных с признаками НАЖБПЖ вероятность развития МС была более чем в три раза выше, чем у пациентов без них (относительный риск (ОР) — 3,13, p = 0,004). Кроме того, в работе было установлено, что каждый дополнительный фактор МС (индекс массы тела > 30 кг/м2, СД 2-го типа, артериальная гипертензия или гиперлипидемия) увеличивает риск развития стеатоза ПЖ на 37% [16].
По данным метаанализа R.G. Singh и соавт. (n = 20000), у лиц с признаками стеатоза ПЖ наблюдалась значительно более высокая распространенность МС, чем у пациентов без него, а также большее количество его лабораторных маркеров. В частности, согласно ряду исследований со схожим дизайном, представленных в указанном метаанализе, у 43,4% пациентов со стеатозом ПЖ был выявлен МС (265 случаев из 611), в то время как у лиц без него признаки МС выявлялись лишь в 17,5% случаев (у 361 пациента из 2057). Наличие стеатоза ПЖ было ассоциировано с развитием МС с ОР — 2,37 (95% доверительный интервал (ДИ) = 2,07–2,71; р < 0,001) [17].
В условиях повышенного питания (особенно богатого простыми углеводами и жирами) достаточно быстро формируется НАЖБПЖ, вследствие которой существенно усугубляются механизмы, формирующие и поддерживающие течение МС. Известно, что при повышенном накоплении триглицеридов функциональная активность β-клеток снижается, а их склонность к апоптозу несколько увеличивается. Подвергшиеся апоптозу β-клетки замещаются участками фиброза и адипоцитами, что, в свою очередь, также поддерживает локальный воспалительный процесс. В настоящее время активно изучаются отрицательные паракринные эффекты интрапанкреатических адипоцитов. Таким образом, риск НАЖБПЖ при инсулинорезистентности и гипергликемии повышается, а ее наличие способствует усугублению нарушений углеводного обмена (рис. 2).
Вероятно, патогенез развития СД 2-го типа у пациентов с НАЖБПЖ не исчерпывается печеночным метаболизмом липидов, поскольку не у всех пациентов с НАЖБПЖ и СД 2-го типа выявляются признаки НАЖБП. Судя по всему, НАЖБПЖ может участвовать в патогенезе СД 2-го типа независимо от НАЖБП, роль которой в нарушениях углеводного обмена достаточно хорошо изучена. Склонность к гипергликемии у пациентов с НАЖБПЖ не всегда зависит от развития периферической инсулинорезистентности и может быть обусловлена нарушением функции β-клеток на фоне накопления липидов в эндокринной части ПЖ, при этом вследствие пока не вполне ясных причин развития НАЖБП у таких пациентов не происходит. Считается, что данный процесс играет решающую роль в патогенезе СД 2-го типа. С другой стороны, у больных с сочетанием НАЖБП и НАЖБПЖ инсулинорезистентность практически всегда выражена в большей степени, чем у пациентов только с НАЖБП. Нельзя исключить, что и в тканях печени, и в тканях ПЖ существуют многообразные механизмы (вероятно, генетически обусловленные), которые предопределяют некий критический порог накопления липидов, при превышении которого выраженность метаболических нарушений начинает прогрессивно увеличиваться. Можно предположить, что устойчивость организма к развитию нарушений углеводного обмена детерминирована не только и не столько его индивидуальными показателями периферической инсулинорезистентности, сколько устойчивостью главных метаболических центров — печени и ПЖ — к тканевому накоплению липидов и последующему хроническому воспалению.
Поперечное исследование C.Y. Wang и соавт., выполненное на китайской популяции (n = 8097), выявило большую распространенность СД 2-го типа у больных с НАЖБПЖ по сравнению с пациентами без нее (12,6 и 5,2% соответственно, р < 0,001). НАЖБП в данной работе также значительно чаще встречалась у пациентов с НАЖБПЖ, чем без нее (67,2 и 35,1% соответственно, р < 0,001) [18]. Тем не менее, ряд исследований не выявили разницы в содержании жира в тканях ПЖ у пациентов с СД 2-го типа и без него, однако авторы обзора отмечают, что отсутствие значимых различий касается именно человеческой популяции и может быть связано с разными способами подсчетов содержания жира по косвенным методикам визуализации, и не оспаривают данные экспериментальных моделей, где количество жира оценивалось морфологически.
Таким образом, складывается представление о существенном вкладе НАЖБПЖ в развитие нарушений углеводного обмена. Данная точка зрения подтверждается результатами 10-летнего проспективного исследования T.T. Chan и соавт. (n = 631). Примечателен тот факт, что СД 2-го типа был критерием невключения, то есть исследователи намеренно исключили факт влияния исходной гипергликемии на формирование стеатоза ПЖ. Исходно признаки НАЖБПЖ выявлялись у 93 (14,7%) пациентов. Показано, что у больных с НАЖБПЖ частота СД 2-го типа была значительно выше, чем у лиц без нее (33,3 против 10,4%; p < 0,001). В ходе длительного наблюдения было выявлено, что в группе пациентов с НАЖБПЖ СД 2-го типа развивался чаще, чем в группе сравнения (33,3 и 10,4%; р < 0,001). У пациентов с НАЖБПЖ также чаще развивалась артериальная гипертензия (37,7 и 22,7% соответственно; р = 0,003) и дислипидемии (37,7 и 14,6%; р < 0,001). В основном СД 2-го типа возникал у пациентов с сочетанием НАЖБП и НАЖБПЖ (р < 0,001), при этом НАЖБПЖ была его независимым предиктором развития (скорректированное ОР — 1,81; 95% ДИ = 1,10–3,00; р = 0,020), но не гипертензии или дислипидемии. Согласно расчетам авторов исследования, повышение содержания жира в ПЖ на 1% увеличивало риск развития СД 2-го типа на 7% (скорректированное ОР — 1,07; 95% ДИ = 1,01–1,13; р = 0,016) [19].
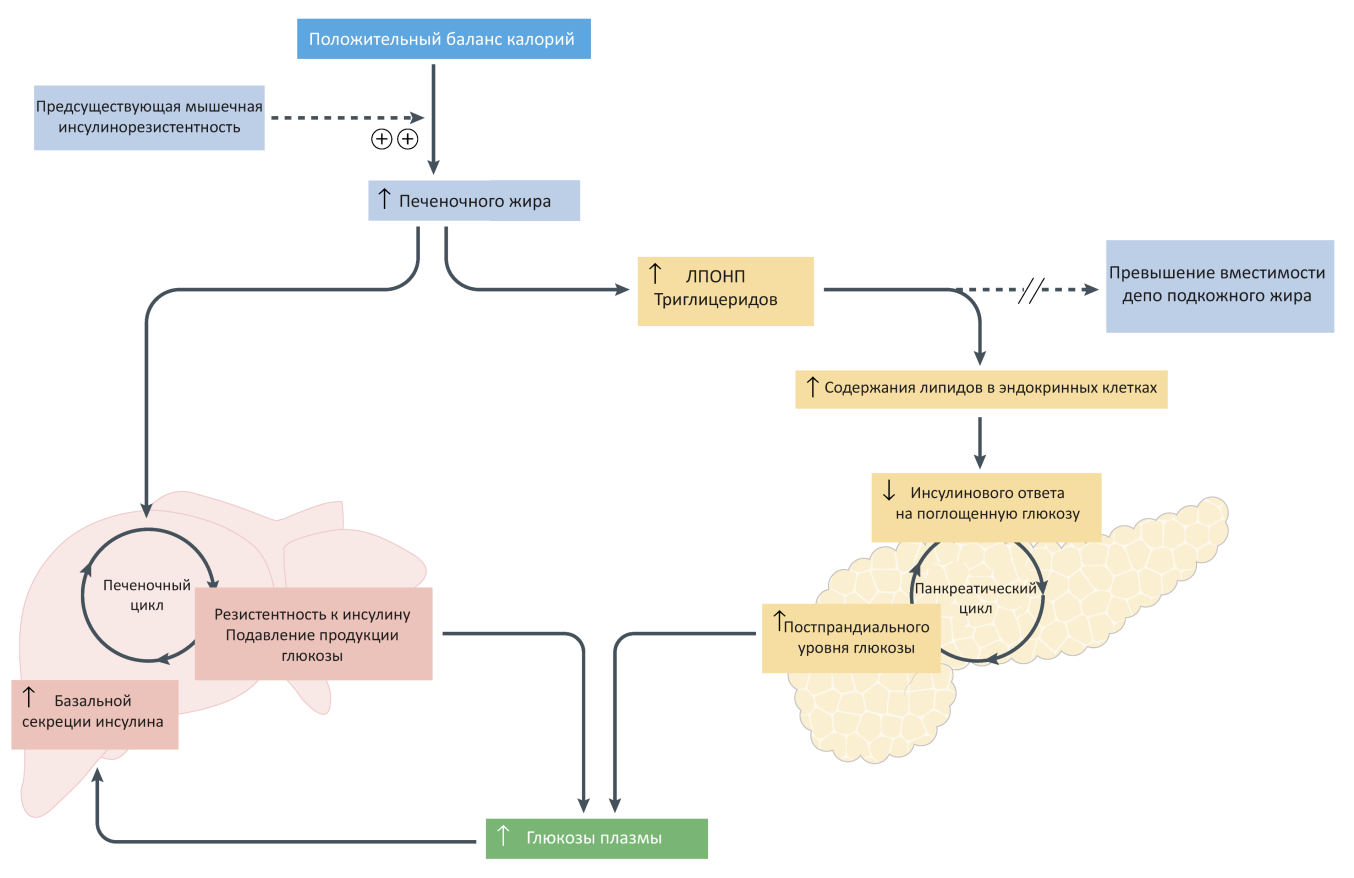
Рис. 2. Роль избыточного внутрипанкреатического отложения жира в развитии сахарного диабета 2-го типа (адаптировано из R. Taylor и соавт., 2015 [20])
Активно изучается взаимное влияние НАЖБП и компонентов НАЖБПЖ. Так, в исследовании J.S. Lee и соавт. среди пациентов с ультразвуковыми признаками стеатоза ПЖ в 68% случаев была выявлена НАЖБП, при этом у больных с НАЖБП признаки стеатоза ПЖ выявлялись в 97% случаев. Авторы пришли к заключению о том, что стеатоз ПЖ является более ранним проявлением МС, чем НАЖБП [21].
Связь НАЖБПЖ с компонентами МС имеет важное клиническое значение, поскольку в литературе появляются данные об ассоциации избыточного панкреатического жира и тяжести сердечно-сосудистых заболеваний. Нельзя исключить, что основным «действующим лицом» является именно комплекс метаболических нарушений, формирующийся у больных с висцеральным ожирением, однако нужно помнить и о категории пациентов, имеющих признаки стеатоза ПЖ без выявленных компонентов МС. Так, в работе S. Kul и соавт. (n = 93, из них 44 больных с НАЖБПЖ, 49 – без нее) толщина эпикардиальной жировой ткани у пациентов с НАЖБПЖ была существенно выше: 6,09 ± 1,52 мм и 3,87 ± 1,31 мм соответственно; p < 0,001. У лиц с НАЖБПЖ также выявлена намного большая толщина комплекса интима-медиа аорты: 1,12 (0,60–1,90) мм и 0,93 (0,50–1,44) мм соответственно; p < 0,001 [22].
Существуют данные, что выраженность НАЖБПЖ может быть связана с атеросклерозом коронарных артерий у пациентов с СД 2-го типа. Согласно результатам исследования S. Sahin и соавт. (n = 99), которое было посвящено изучению связи НАЖБПЖ и острого коронарного синдрома, у пациентов с НАЖБПЖ по сравнению с контрольной группой отмечены значительно более высокие показатели SXscore (ангиографического расчетного показателя, отражающего риск сердечно-сосудистой смерти): 12,3 ± 6,4 и 8,2 ± 4,3; р < 0,001 [23].
Попытка оценить вклад НАЖБПЖ в развитие атеросклероза у пациентов с СД 2-го типа была предпринята P. Sun: из 173 пациентов у большинства (71,7%) по данным коронароангиографии выявлялись стенозы легкой и средней степени, у 12,7% — стенозы тяжелой степени, у остальных не было значимых изменений коронарного русла. У всех пациентов оценивалась выраженность стеатоза ПЖ по отношению плотности ПЖ и селезенки по данным компьютерной томографии (КТ) (с помощью индекса Р/S). Согласно результатам исследования, индекс Р/S у больных с тяжелым коронарным атеросклерозом был значительно выше, чем у обследованных с легким и средним атеросклерозом или без него. Более того, авторы утверждают, что индекс P/S может служить независимым прогностическим фактором развития тяжелого стеноза коронарных артерий (ОР — 0,062; 95% ДИ = 0,008–0,487; р = 0,008) [24].
Данные относительно взаимного влияния НАЖБПЖ и артериальной гипертензии несколько противоречивы. Более того, ряд исследователей указывают на то, что артериальная гипертензия сама по себе способствует накоплению липидов в тканях ПЖ: вазоконстрикция у пациентов с артериальной гипертензией влечет за собой развитие гипоперфузии, что приводит к тканевой гипоксии. Как известно, в условиях гипоксии усиливаются процессы апоптоза, накопление липидов и фиброз (что хорошо иллюстрирует жировая дистрофия печени на фоне хронической сердечной недостаточности). Следовательно, гипертензия может способствовать стойкой тканевой гипоксии, приводящей к накоплению липидов и дисфункции островков ПЖ. В упомянутом ранее метаанализе R.G. Singh и соавт. наличие НАЖБПЖ увеличивало риск развития артериальной гипертензии на 67% [17]. В ретроспективном исследовании E.H. Lee и соавт. (n = 65, дети с НАЖБП) при наличии признаков НАЖБП вероятность возникновения артериальной гипертензии повышалась в 1,28 раза по сравнению с показателями детей без НАЖБПЖ (отношение шансов — 1,28; 95% ДИ = 1,01–1,62; р < 0,001) [25]. Тем не менее, в исследовании P.S. Sepe наличие артериальной гипертензии было фактором риска НАЖБПЖ, но ее значимого влияния на течение и риск развития артериальной гипертензии выявлено не было [16].
Диагностика
НАЖБПЖ, в отличие от НАЖБП, в настоящее время не рубрифицируется как отдельное заболевание в связи с тем, что диагностические критерии пока еще уточняются. Тем не менее, если исходить из определения, ключевым компонентом выявления данного состояния является подтверждение жировой инфильтрации ПЖ (с учетом сбора анамнеза относительно эпизодов хронической алкоголизации и наличия некоторых наследственных заболеваний).
В связи с этим основную роль в выявлении НАЖБП играют различные методы визуализации ПЖ, позволяющие количественно определить в ней долю жировой ткани. Методы, доступные в условиях реальной клинической практики, включают в себя ультразвуковое исследование (УЗИ) (в том числе эластографию ПЖ), КТ, магнитно-резонансную томографию (МРТ), в более редких случаях может использоваться магнитно-резонансная спектроскопия.
УЗИ в стандартном виде (согласно трансабдоминальному протоколу) в большинстве случаев не дает достаточной информации о состоянии ПЖ, поскольку у многих пациентов визуализация затруднена в связи с конституциональными особенностями, а ПЖ может быть перекрыта содержащим газ желудком или петлями пневматизированного кишечника. В свою очередь, эндоскопическое УЗИ позволяет разместить датчик в непосредственной близости от ПЖ, что существенно улучшает визуализацию органа. Стеатоз ПЖ проявляется диффузным повышением эхогенности, структура ПЖ при этом обычно однородная, размеры в пределах нормы или слегка превышают ее, контуры ровные, часто нечеткие. Стоит отметить, что при фиброзе ПЖ изменения носят схожий характер, и поскольку УЗИ не способно четко ответить на вопрос, за счет какой ткани повышена эхогенность ПЖ, данный метод не может быть рекомендован для скрининга НАЖБПЖ.
Эластография позволяет измерить биомеханические свойства тканей (в частности, их жесткость и эластичность). Глубокое расположение ПЖ затрудняет использование временной эластографии, но перспективным считается применение точечной эластографии сдвиговой волной под контролем стандартного УЗИ.
Имеющиеся на сегодняшний день данные относительно эластографических характеристик ткани ПЖ при стеатозе несколько противоречивы. По результатам КТ, позволяющей оценить плотность ПЖ при панкреостеатозе, данный показатель снижается, достигая значений, характерных для селезенки. Пороговые значение КТ-плотности, которые могут быть использованы в диагностике стеатоза ПЖ, в настоящее время не определены. Таким образом, это перспективное направление для дальнейшей работы в связи с высокой частотой назначения КТ органов брюшной полости.
МРТ также является значимым методом оценки состава ПЖ, поскольку позволяет не только точно определять размеры органа и гомогенные изменения структуры железы, характерные для стеатоза, но и оценивать признаки повышенного содержания в ней липидов. Примеры МР-томограмм представлены на рисунке 3. В настоящий момент критерии МР-диагностики стеатоза ПЖ также продолжают разрабатываться.
Метод протонной магнитно-резонансной спектроскопии позволяет количественно оценить содержание триглицеридов в ПЖ, однако результаты визуализации могут быть «загрязнены» внепанкреатическими структурами (в частности, внепанкреатическим жиром), а само исследование более дорогостоящее и занимает много времени в сравнении с упомянутыми выше методиками [26, 27].
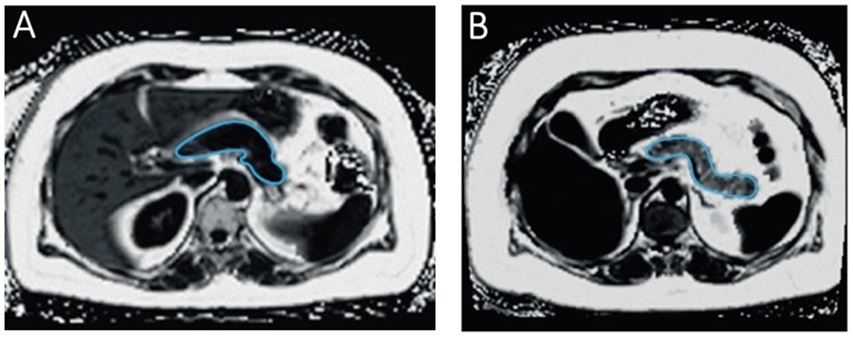
Рис. 3. Магнитно-резонансные томограммы пациентов с различным содержанием жира в поджелудочной железе (адаптировано из R. Wagner и соавт. [28]). Поджелудочная железа очерчена синей линией. А — низкое содержание жира. В — высокое содержание жира
Хотя морфологическое исследование для прижизненной оценки доли жировой ткани в ПЖ рутинно не используется, аутопсийный материал и фрагменты ПЖ, полученные в ходе оперативных вмешательств на ней, позволяют оценить особенности распределения жировой ткани у пациентов с НАЖБПЖ. В частности, показано, что отложение жира в ткани ПЖ, как правило, происходит не внутриклеточно (в отличие от ткани печени при НАЖБП), а межклеточно, что характерно как для эндокринной, так и экзокринной части ПЖ. Морфологические признаки стеатоза ПЖ представлены на рисунке 4.
Распределение жировой ткани в ПЖ может быть равномерным и неравномерным. Неравномерное накопление подразделяют на следующие категории:
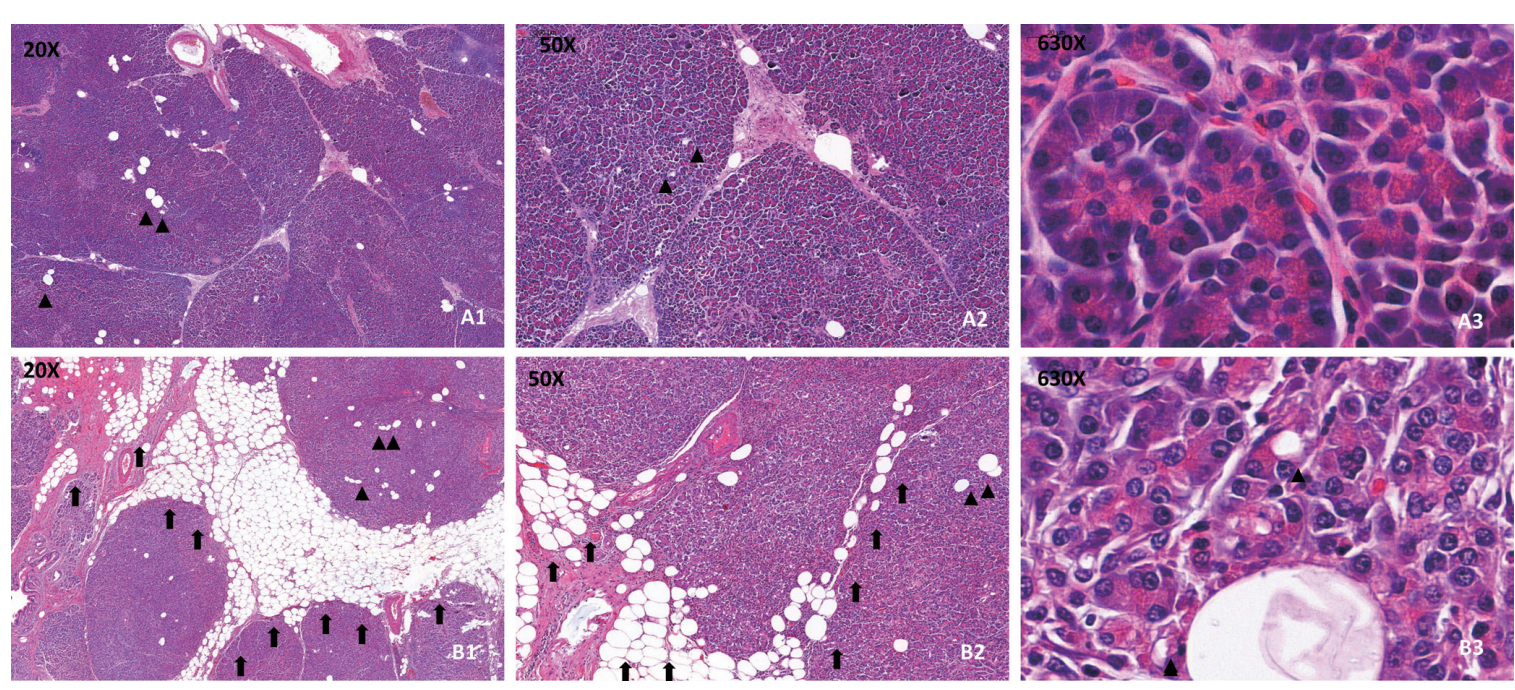
Рис. 4. Гистологическое исследование поджелудочной железы (M. Rugivarodom и соавт., 2022 [29]). Окраска: гематоксилин/эозин. А — здоровая поджелудочная железа: А1, А2 — треугольными указателями отмечены междольковые адипоциты, внутридольковый жир представлен слабо, занимая 3% от объема поджелудочной железы; А3 — сохраненная архитектоника поджелудочной железы. В — стеатоз поджелудочной железы: В1 — стрелками обозначены перипанкреатические адипоциты, треугольными указателями — междольковые адипоциты (стрелка, B2), количество внутридаолькового жира существенно увеличено — до 23% объема поджелудочной железы; В3 — многочисленные липидные капли (белые округлые пятна)
Подходы к лечению
Поскольку НАЖБПЖ является следствием МС, основным подходом к лечению и профилактике этого состояния считается комплекс мероприятий, направленных на снижение или нормализацию массы тела, что приводит к снижению инсулинорезистентности, а также значимой коррекции метаболических нарушений со стороны углеводного и липидного видов обмена.
Согласно результатам исследования A.P. Rossi, снижение массы тела на 8,9% на фоне низкокалорийной диеты у 24 пациентов с ожирением по результатам МРТ способствовало значимому уменьшению доли панкреатического жира [30]. В когортном исследовании HELENA (n = 137) у лиц с ожирением оценивали долю панкреатической жировой ткани по данным МРТ исходно и после 12-недельного периода низкокалорийной диеты. Исходно была установлена положительная корреляция между количеством жировой ткани в ПЖ и висцеральной жировой ткани (r = 0,41, p < 0,001). Кроме того, определено, что снижение массы тела приводит к уменьшению выраженности стеатоза ПЖ [31].
Интересны результаты работы Y. Gepner и соавт. (n = 278, длительность исследования — 18 месяцев), в которой сравнивалось влияние низкожировой и средиземноморской диеты на содержание жира в печени, ПЖ и перикарде у пациентов с абдоминальным ожирением. Так, средиземноморская диета приводила к более значимому (по сравнению с низкожировой) уменьшению содержания жира во всех перечисленных областях, а снижение объема висцеральной жировой ткани независимо улучшало метаболические показатели. Уменьшение доли подкожных жировых депо подобного эффекта в приведенном исследовании не оказало [32].
Влияние физических нагрузок на течение НАЖБПЖ оценивалось в работе М.A. Heiskanen и соавт. (n = 54, возраст участников — 40–55 лет). Особенностью исследования являлось то, что критерием включения был малоподвижный образ жизни; у части обследуемых были выявлены нарушение толерантности к глюкозе или СД 2-го типа (n = 26). У всех пациентов исходно и после двухнедельного периода стандартизированных физических нагрузок оценивали количество панкреатической жировой ткани, показатели секреции инсулина в пероральном глюкозотолерантном тесте, а также поглощение глюкозы и жирных кислот тканью ПЖ с помощью позитронно-эмиссионной томографии. Согласно результатам исследования, у лиц с нарушениями углеводного обмена количество жира в ПЖ было выше по сравнению с пациентами, не имеющими их. Отмечено, что физические нагрузки приводили к снижению панкреатического жира у всех исследуемых. Так, у лиц с нарушением толерантности к глюкозе или СД 2-го типа содержание жировой ткани в ПЖ снизилось с 8,7 (6,0–11,9) % до 6,7 (4,4–9,6) %, а в группе здоровых лиц — с 4,4 (3,0–6,1) % до 3,6 (2,4–5,2) %. У всех пациентов также было выявлено положительное влияние физических нагрузок на показатели секреции инсулина, однако разницы между исходным захватом глюкозы и жирных кислот тканью ПЖ в данной работе не выявлено, что, по мнению авторов, может быть связано с небольшой длительностью исследования и малым размером выборки [33].
Поскольку бариатрические вмешательства способны приводить к ремиссии СД 2-го типа, логично предположить их воздействие и на ткань ПЖ. Известно, что нормализация гликемии после выполнения продольной резекции желудка и гастрошунтирования происходит уже в первые часы после вмешательства в связи с повышением уровня эндогенного глюкагоноподобного пептида-1 и не связана напрямую с изменением в тканях ПЖ. Тем не менее, долгосрочный сахароснижающий эффект бариатрических операций сохраняется далеко не у всех пациентов и может быть связан со степенью стеатоза ПЖ, а утрата положительного метаболического эффекта может быть следствием повторного набора массы тела в послеоперационном периоде. Предполагается, что хирургическое лечение ожирения и метаболических расстройств также приводит к снижению выраженности НАЖБПЖ. Так, в исследовании А.А. Salman (n = 54) после выполнения продольной резекции желудка доля жировой ткани в ПЖ уменьшилась с 26,8 ± 7,2 % до 20,0 ± 7,3 %, а также определялось существенное снижение активности панкреатической липазы плазмы (р < 0,001). Кроме того, была замечена положительная корреляция между процентом общей потери массы тела и уменьшением доли жира в ПЖ (r = 0,295, р = 0,030) [34].
Перспективными направлениями фармакотерапии НАЖБПЖ являются препараты, способствующие преодолению инсулинорезистентности, и другие, использующиеся в лечении СД 2-го типа. В частности, широко известно положительное влияние метформина на липидный обмен, а также его способность уменьшать долю висцеральной жировой ткани. Немаловажным является и снижение выраженности окислительного стресса, наблюдаемое у пациентов, получающих метформин. В экспериментах на животных с СД 2-го типа установлено, что введение тиазолиндионов препятствует воспалению в тканях ПЖ, уменьшает выраженность жировой инфильтрации и фиброза ПЖ. Прием орлистата снижал степень воспаления в тканях ПЖ у мышей с ожирением и стеатозом ПЖ, а совместное применение ситаглиптина и телмисартана в аналогичных экспериментальных моделях было эффективно в лечении стеатоза ПЖ [35]. У крыс с ожирением назначение сандостатина (аналога соматостатина) приводило к замедлению накопления жира в ПЖ, уменьшению инсулинорезистентности и улучшению липидного спектра [36]. Существуют данные, что берберин и коричная кислота способны ингибировать накопление липидов в культурах бета-клеток ПЖ, однако они не были доказаны на моделях ожирения и СД 2-го типа [37].
Возможно, определенный эффект на течение НАЖБПЖ могут оказывать лекарства, направленные на борьбу с дислипидемиями, а также препараты, влияющие на выраженность оксидативного стресса, витаминные препараты и гепатопротекторы (за счет тесной связи НАЖБП и НАЖБПЖ). В настоящее время недостаточно данных относительно влияния фармакологических агентов на течение НАЖБПЖ, специфические средства не разработаны, однако исследования в данном направлении продолжаются.
Заключение
Дисфункция жировой ткани, формирующаяся в условиях МС, приводит к системным изменениям. НАЖБПЖ — сравнительно новое понятие, применяемое для обозначения жирового повреждения ПЖ в условиях метаболического нездоровья, что отличает его от накопления липидов в ПЖ на фоне повторяющейся алкогольной интоксикации, а также вследствие травм, воспалительных процессов и врожденных заболеваний.
В связи с тем, что эктопически расположенная дисфункциональная жировая ткань демонстрирует провоспалительную активность, здоровая ткань ПЖ при НАЖБПЖ подвергается воздействию воспалительных цитокинов и оксидативного стресса, что потенциально способно нарушать функцию как эндокринного, так и экзокринного аппарата ПЖ. Влияние НАЖБПЖ на секрецию инсулина и реализацию другой гормональной активности продолжает изучаться, данные исследований противоречивы и получены на выборках пациентов с различной соматической патологией и исходными антропометрическими параметрами. Тем не менее, не вызывает сомнения тесная связь НАЖБПЖ и других компонентов МС, включая НАЖБП. Таким образом, разработка методов диагностики и подходов к лечению НАЖБПЖ представляется актуальной клинической задачей.
Следующая статья
С.С. Байрамова1, О.В. Цыганкова1, 2, К.Ю. Николаев1, А.А. Старичков...