Опыт успешного лечения рецидивирующего полихондрита тофацитинибом
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Mathian A., Miyara M., Cohen-Aubart F., Haroche J. et al. Relapsing polychondritis: a 2016 update on clinical features, diagnostic tools, treatment and biological drug use. Best Pract. Res. Clin. Rheumatol. 2016; 30(2): 316–33. DOI: 10.1016/j.berh.2016.08.001
- Longo L., Greco A., Rea A., Lo Vasco V.R. et al. Relapsing polychondritis: a clinical update. Autoimmun Rev. 2016; 15(6): 539–43. DOI: 10.1016/j.autrev.2016.02.013
- Sharma A., Gnanapandithan K., Sharma K., Sharma S. Relapsing polychondritis: a review. Clin. Rheumatol. 2013; 32(11): 1575–83. DOI: 10.1007/s10067-013-2328-x
- Letko E., Zafirakis P., Baltatzis S., Voudouri A. et al. Relapsing polychondritis: a clinical review. Semin. Arthritis Rheum. 2002; 31(6): 384–95. DOI: 10.1053/sarh.2002.32586
- Trentham D.E., Le C.H. Relapsing polychondritis. Ann. Intern. Med. 1998; 129(2): 114–22. DOI: 10.1055/s-2002-25303
- Jaksch-Wartenhorst R. Polychondropathia. Wien Arch. F Inn. Med. 1923; 6: 93–100.
- Pearson C.M., Kline H.M., Newcomer V.D. Relapsing polychondritis. N. Engl. J. Med. 1960; 263: 51–8. DOI: 10.1056/NEJM196007142630201
- Черняк В.И., Савельев А.И., Погромов А.П., Меньшикова И.В. и др. Рецидивирующий полихондрит. Клиническая медицина. 2014; 92(11): 22–8. [Chernyak V.I., Savelyev A.I., Pogromov A.P., Menshikova I.V. et al. Relapsing polychondritis. Clinical Medicine. 2014; 92(11): 22–8. (in Russian)]
- Черняк В.И., Савельев А.И., Меньшикова И.В., Погромов А.П. Поражение нервной системы при рецидивирующем полихондрите. Клиническая медицина. 2016; 94(2): 108–13. [Chernyak V.I., Savelyev A.I., Menshikova I.V., Pogromov A.P. Nervous system lesions associated with relapsing polychondritis: analysis of original observations. Clinical Medicine. 2016; 94(2): 108–13. (in Russian)]. DOI 10.18821/0023-2149-2016-94-2-108-113
- Fukuda K., Mizobuchi T., Nakajima I., Kishimoto T. et al. Ocular involvement in relapsing polychondritis. J. Clin. Med. 2021; 10(21): 4970. DOI: 10.3390/JCM10214970
- Dion J., Costedoat-Chalumeau N., Sène D., Cohen-Bittan J. et al. Relapsing polychondritis can be characterized by 3 different clinical phenotypes: analysis of a series of 142 patients. Arthritis Rheumatol. 2016; 68(12): 2992–3001. DOI: 10.1002/art.39790
- File I., Trinn C., Mátyus Z., Ujhelyi L. et al. Relapsing polychondritis with p-ANCA associated vasculitis: which triggers the other? World J. Clin. Cases. 2014; 2(12): 912–7. DOI: 10.12998/wjcc.v2.i12.912
- Pruthi P., Munganda H., Bangia A., Rani U. et al. Leprosy with atypical skin lesions masquerading as relapsing polychondritis. Case Rep. Infect. Dis. 2016; 2016: 7802423. DOI: 10.1155/2016/7802423
- Урсол Н.Б., Тарасюк М.И., Закревская В.А. Клинический случай рецидивирующего полихондрита. Украинский терапевтический журнал. 2015; 44(1): 102–6. [Ursol N.B., Tarasyuk M.I., Zakrevskaya V.A. A clinical case of relapsing polychondritis. Ukrainian Therapeutic Journal. 2015; 44(1): 102–6. (in Russian)]
- Заигрова Н.К., Лазарева О.Ю., Долженкова Е.А. Клинический случай рецидивирующего полихондрита у больного сублейкемическим миелозом. Земский врач. 2015; 25(1): 59–62. [Zaigrova N.K., Lazareva O.Yu., Dolzhenkova E.A. Clinical case of relapsing polychondritis in patient with subleukemic mielosis. Zemsky Doctor. 2015; 25(1): 59–62. (in Russian)]
- Молоткова С.А., Молотков А.О., Литвинова И.А., Базина И.Б. и др. Ревматологические проявления острого миелобластного лейкоза: случай из практики. Вестник Смоленской государственной медицинской академии. 2017; 16(1): 71–6. [Molotkova S.A., Molotkov A.O., Litvinova I.A., Bazina I.B. et al. Rheumatological manifestations of acute nonlymphoblastic leukemia: case in clinical practice. Vestnik of the Smolensk State Medical Academy. 2017; 16(1): 71–6. (in Russian)]
- Hazra N., Dregan A., Charlton J., Gulliford M.C. et al. Incidence and mortality of relapsing polychondritis in the UK: a population-based cohort study. Rheumatology (Oxford). 2015; 54(12): 2181–7. DOI: 10.1093/rheumatology/kev240
- Nakano K., Aritomi T., Ohkubo N., Tanaka Y. Relapsing polychondritis diagnosed by fusion images of gallium-67 uptake on computed tomography and single-photon–emission computed tomography. Arthritis Rheumatol. 2017; 69(12): 2406. DOI: 10.1002/art.40234
- Lei W., Zeng H., Zeng D.X., Zhang B. et al. (18)F-FDG PET-CT: a powerful tool for the diagnosis and treatment of relapsing polychondritis. Br. J. Radiol. 2016; 89(1057): 20150695. DOI: 10.1259/bjr.20150695
- Wang J., Li S., Zeng Y., Chen P. et al. 18F-FDG PET/CT is a valuable tool for relapsing polychondritis diagnose and therapeutic response monitoring. Ann. Nucl. Med. 2014; 28(3): 276–84. DOI: 10.1007/s12149-014-0805-1
- Wang J., Liu X., Pu C., Chen Y. 18F-FDG PET/CT is an ideal imaging modality for the early diagnosis of relapsing polychondritis. Medicine (Baltimore). 2017; 96(30): e7503. DOI: 10.1097/MD.0000000000007503
- Zhou H., Su M., Li L. 18F-FDG PET/CT imaging of relapsing polychondritis: A case report. Medicine (Baltimore). 2016; 95(33): e4496. DOI: 10.1097/MD.0000000000004496
- Ikeda S., Arita M., Ikeo S., Nishiyama A. et al. Chronological assessment of airway lesions in relapsing polychondritis by positron emission tomography. Intern. Med. 2015; 54(9): 1099–102. DOI: 10.2169/internalmedicine.54.3775
- Огнерубов Н.А., Антипова Т.С. Возможности ПЭТ/КТ в диагностике и оценке терапии рецидивирующего полихондрита: случаи из практики. Вестник Тамбовского университета. Серия: Естественные и технические науки. 2017; 22(6–2): 1422–30. [Ognerubov N.A., Antipova T.S. PET/CT capabilities in the diagnostics and estimation of therapy of generalized chondromalacia: practice cases. Tambov University Reports. Series of Natural and Technical Sciences. 2017; 22(6–2): 1422–30. (in Russian)]
- McAdam L.P., O’Hanlan M.A., Bluestone R., Pearson C.M. Relapsing polychondritis: prospective study of 23 patients and a review of the literature. Med. 1976; 55(3): 193–215.
- Damiani J.M., Levine H.L. Relapsing polychondritis — report of ten cases. Laryngoscope. 1979; 89(6 Pt1): 929–46.
- Michet C.J., McKenna C.H., Luthra H.S., O’Fallon W.M. Relapsing polychondritis: Survival and predictive role of early disease manifestations. Ann. Intern. Med. 1986; 104(1): 74–8. DOI: 10.7326/0003-4819-104-1-74
- Thaiss W.M., Nikolaou K., Spengler W., Spira D. et al. Imaging diagnosis in relapsing polychondritis and correlation with clinical and serological data. Skeletal Radiol. 2016; 45(3): 339–46. DOI: 10.1007/s00256-015-2270-x
- Lin D.F., Yang W.Q., Zhang P.P., Lv Q. et al. Clinical and prognostic characteristics of 158 cases of relapsing polychondritis in China and review of the literature. Rheumatol. Int. 2016; 36(7): 1003–9. DOI: 10.1007/s00296-016-3449-8
- Arnaud L., Devilliers H., Peng S.L., Mathian A. et al. The Relapsing Polychondritis Disease Activity Index: development of a disease activity score for relapsing polychondritis. Autoimmun. Rev. 2012; 12(2): 204–9. DOI: 10.1016/j.autrev.2012.06.005
- Horváth A., Páll N., Molnár K., Kováts T. et al. A nationwide study of the epidemiology of relapsing polychondritis. Clin. Epidemiol. 2016; 8: 211–30. DOI: 10.2147/CLEP.S91439
- Kemta Lekpa F., Kraus V.B., Chevalier X. Biologics in relapsing polychondritis: a literature review. Semin. Arthritis Rheum. 2012; 41(5): 712–19. DOI: 10.1016/j.semarthrit.2011.08.006
- Wasano K., Tomisato S., Yamamoto S., Suzuki N. et al. Successful continual intratympanic steroid injection therapy in a patient with refractory sensorineural hearing loss accompanied by relapsing polychondritis. Auris Nasus Larynx. 2017; 44(4): 489–92. DOI: 10.1016/j.anl.2016.07.019
- Martin J., Roenigk H.H., Lynch W., Tingwald F.R. Relapsing polychondritis treated with dapsone. Arch. Dermatol. 1976; 112(9): 1272–4.
- Barranco V.P., Minor D.B., Solomon H. Treatment of relapsing polychondritis with dapsone. Arch. Dermatol. 1976; 112(9): 1286–8.
- Lu P.H., Lin Y.C., Wu Y.H. Relapsing polychondritis complicated with Sweet’s syndrome and normolipemic neutrophilic xanthomatosis successfully treated by dapsone. Int. J. Dermatol. 2011; 50(2): 212–14. DOI: 10.1111/j.1365-4632.2010.04477.x
- Belot A., Collardeau-Frachon S., Bellil D., Descours G. et al. It sounds like a relapsing polychondritis. Lancet Infect. Dis. 2013; 13(7): 638. DOI: 10.1016/S1473-3099(13)70114-2
- Almackenzie M., Alharbi A., Alhassan S., Cook E. et al. Successful treatment of central nervous system vasculitis associated with relapsing polychondritis with cyclophosphamide. Am. J. Med. Sci. 2017; 353(5): 495–7. DOI: 10.1016/j.amjms.2016.11.023
- Sainz-De-La-Maza M., Molina N., Gonzalez-Gonzalez L.A., Doctor P.P. et al. Scleritis associated with relapsing polychondritis. Br. J. Ophthalmol. 2016; 100(9): 1290–4. DOI: 10.1136/bjophthalmol-2015-306902
- Yang C.L., Brinckmann J., Rui H.F., Vehring K.H. et al. Autoantibodies to cartilage collagens in relapsing polychondritis. Arch. Dermatol. Res. 1993; 285(5): 245–9. DOI: 10.1007/BF00371591
- Hansson A.S., Heinegard D., Piette J.C., Burkhardt H. et al. The occurrence of autoantibodies to matrilin 1 reflects a tissue-specific response to cartilage of the respiratory tract in patients with relapsing polychondritis. Arthritis Rheum. 2001; 44(10): 2402–12. DOI: 10.1002/1529-0131(200110)44:10<2402::AID-ART405>3.0.CO;2-L
- Kemta Lekpa F., Chevalier X. Refractory relapsing polychondritis: challenges and solutions. Open Access Rheumatol. Res. Rev. 2018; 10: 1–11. DOI: 10.2147/OARRR.S142892
- Tomomatsu J., Hamano Y., Ando J., Komatsu N. et al. Non-myeloablative allogenic BMT for myelodysplastic syndrome successfully controlled accompanying relapsing polychondritis. Bone Marrow Transplant. 2012; 47(5): 742–3. DOI: 10.1038/bmt.2011.159
- Daikeler T., Kötter I., Tyndall C.B., Apperley J. et al. Haematopoietic stem cell transplantation for vasculitis including Behçet’s disease and polychondritis: a retrospective analysis of patients recorded in the European Bone Marrow Transplantation and European League Against Rheumatism databases and a review. Ann. Rheum. Dis. 2007; 66(2): 202–7. DOI: 10.1136/ard.2006.056630
- Kötter I., Daikeler T., Amberger C., Tyndall A. et al. Autologous stem cell transplantation of treatment-resistant systemic vasculitis — a single center experience and review of the literature. Clin. Nephrol. 2005; 64(6): 485–9. DOI: 10.5414/cnp64485
- Rosen O., Thiel A., Massenkeil G., Hiepe F. et al. Autologous stem-cell transplantation in refractory autoimmune diseases after in vivo immunoablation and ex vivo depletion of mononuclear cells. Arthritis Res. 2000; 2(4): 327–36. DOI: 10.1186/ar107
- Haug M.D., Witt P., Kalbermatten F.D., Rieger U.M. et al. Severe respiratory dysfunction in a patient with relapsing polychondritis: should we treat the saddle nose deformity? J. Plast. Reconstr. Aesthetic Surg. 2009; 62(2): e7–10. DOI: 10.1016/j.bjps.2008.05.012
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации; Россия, г. Москва
2 АО «Европейский Медицинский Центр»; Россия, г. Москва
3 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации; Россия, г. Москва
4 ФГАОУ ВО «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); Россия, г. Москва
Цель статьи: рассмотреть клинический случай успешной терапии рецидивирующего полихондрита с помощью тофацитиниба.
Основные положения. РПХ — редкое аутоиммунное заболевание, требующее постоянной иммуносупрессивной терапии. Глюкокортикостероиды (ГКС) позволяют эффективно снизить активность заболевания, однако их длительное использование приводит к развитию осложнений. В связи с этим необходимы базисные иммуносупрессивные препараты для долгосрочного лечения РПХ и минимизации дозы ГКС. Из-за редкости заболевания выполнение рандомизированных клинических исследований невозможно. Современное понимание подходов к терапии основывается на анализе отдельных наблюдений или серий случаев. В статье представлен первый российский опыт успешного применения игибитора Янус-киназы тофацитиниба для лечения РПХ.
Заключение. Остается большое количество сложностей, связанных с пониманием патофизиологии и ранней диагностикой, оценкой активности и прогноза и, конечно, лечением РПХ. Решению указанных проблем будет способствовать объединение данных из различных центров всего мира. Тогда, возможно, удастся продвинуться вперед к лучшему пониманию механизмов развития, разработке новых диагностических критериев, выявлению прогностических факторов. Необходимо проведение рандомизированных клинических исследований для создания доказательных рекомендаций по лечению.
Ключевые слова: ингибиторы Янус-киназы, преднизолон, рецидивирующий полихондрит, стероид-сберегающая терапия, таргетные синтетические базисные противовоспалительные препараты, тофацитиниб
Скачать PDFМешков А.Д., Жиляев Е.В., Новиков П.И. Опыт успешного лечения рецидивирующего полихондрита тофацитинибом. Вестник терапевта. 2023; 1(56). URL: https://journaltherapy.ru/statyi/opyt-uspeshnogo-lechenija-recidivirujushhego-polihondrita-tofacitinibom/ (дата обращения: дд.мм.гг.)
Мешков Алексей Дмитриевич (автор для переписки) — к. м. н., врач-ревматолог, старший научный сотрудник лаборатории заболеваний костно-мышечной системы Российского геронтологического научно-клинического центра ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. 117997, Россия, г. Москва, ул. Островитянова, д. 1. http://orcid.org/0000-0002-5187-0108. E-mail: alexeymeshkov@mail.ru
Жиляев Евгений Валерьевич — д. м. н., профессор, заместитель главного врача по лечебной работе АО «Европейский Медицинский Центр»; профессор кафедры ревматологии ФГБОУ ДПО РМАНПО Минздрава России; профессор кафедры факультетской терапии имени академика А.И. Нестерова ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. 117997, Россия, г. Москва, ул. Островитянова, д. 1. http://orcid.org/0000-0002-9443-1164. E-mail: zhilyayevev@mail.ru
Новиков Павел Игоревич — к. м. н., врач-ревматолог, заведующий ревматологическим отделением Клиники ревматологии, нефрологии и профпатологии имени Е.М. Тареева Университетской клинической больницы № 3 ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). http://orcid.org/0000-0003-0148-5655. 119021, Россия, г. Москва, ул. Россолимо, д. 11, стр. 1. E-mail: novikov-pavel@mail.ru
Experience of successful treatment of relapsing polychondritis with tofacitinib
A.D. Meshkov1, E.V. Zhilyaev1–3, P.I. Novikov4
1 Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation; 1 Ostrovityanova Str., Moscow, Russian Federation 117997
2 Group of companies “European Medical Center”; 35, Schepkin Str., Moscow, Russian Federation 129090
3 Federal State Budgetary Educational Institution of Further Professional Education “Russian Medical Academy of Continuous Professional Education” of the Ministry of Healthcare of the Russian Federation; 2/1 Barrikadnaya Str., build. 1, Moscow, Russian Federation 125993
4 Federal State Autonomous Educational Institution of Higher Education I.M. Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation (Sechenov University); 11 Rossolimo Str., build. 1, Moscow, Russian Federation 119021
Abstract
Objective of the Paper: To consider a case of successful therapy of relapsing polychondritis (RPH) with tofacitinib.
Key points. RPH is a rare autoimmune disease that requires continuous immunosuppressive therapy. Glucocorticosteroids (GCS) can effectively reduce activity of the disease, but their long-time usage results in drug side-effects; thereby, basic immunosuppressive drugs are needed for long-term treatment of RPH and minimizing the dose of GCS. Due to the rarity of the disease, it is impossible to perform randomized clinical trials. Current understanding of therapy approaches is based on the analysis of individual observations or series of cases. The article presents the first Russian experience of the successful use of the Janus kinase inhibitor tofacitinib for the treatment of RPH.
Conclusion. There remains a large number of complexities associated with understanding of the pathophysiology and early diagnostics, assessment of activity and prognosis, and, of course, the treatment of RPH. The solution of these problems will be facilitated by the integration of data from various centers around the world. Then, perhaps, it will be possible to move forward towards a better understanding of the mechanisms of development, designing of new diagnostic criteria, detection of prognostic factors. Randomized clinical trials are needed to provide evidence-based treatment recommendations.
Keywords: relapsing polychondritis, targeted synthetic disease-modifying antirheumatic drugs, Janus kinase inhibitors, tofacitinib, prednisolone, steroid-sparing therapy.
А.Д. Мешков1, Е.В. Жиляев1–3, П.И. Новиков 4
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации; Россия, г. Москва
2 АО «Европейский Медицинский Центр»; Россия, г. Москва
3 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации; Россия, г. Москва
4 ФГАОУ ВО «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); Россия, г. Москва
Рецидивирующий полихондрит (РПХ) — тяжелое аутоиммунное заболевание, проявляющееся как повторными приступами, так и персистирующим воспалительным процессом с прогрессирующим разрушением хрящевых структур, в частности хондритами ушей, носа, гортани и бронхов, а также суставов. В патологический процесс могут также вовлекаться такие богатые протеогликаном структуры, как глаза, сердце, кровеносные сосуды, внутреннее ухо, кожные покровы. РПХ может быть отдельным заболеванием или сочетаться с другими патологиями [1–5].
В 1923 г. R. Jaksch-Wartenhorst [6] опубликовал первое описание и назвал патологию полихондропатией. В 1960 г. C.M. Pearson и соавт., описав 4 новых и 12 старых клинических случев, предложили название, используемое по настоящее время: рецидивирующий полихондрит. Авторы достаточно четко описали РПХ как интенсивное воспалительное состояние как хрящевой, так и так и других тканей. Они также отметили, что после нескольких воспалительных эпизодов хрящевая ткань может замещаться фиброзной соединительной тканью [7].
Несмотря на все дальнейшие исследования, болезнь и в настоящее время продолжает интриговать ученых и клиницистов из-за редкости, сложного патогенеза, неясной этиологии, клинического полиморфизма, непредсказуемого течения и сложного лечения.
На сегодняшний день описаны всего около 1000 случаев РПХ, что свидетельствует о редкости данного заболевания. Большинство случаев — наблюдение нескольких больных в одном медицинском учреждении, большие группы пациентов крайне редки. Таким образом, реальная распространенность и заболеваемость РПХ неизвестны. Даже в небольшом количестве имеющихся данных наблюдается существенное расхождение.
РПХ распространен повсеместно, задокументированы случаи его развития в различных этнических группах, однако большинство пациентов — европеоиды [1–3]. Семейные случаи встречаются редко. Имеются данные о более частом поражении женщин, однако в других исследованиях не отмечали преобладание того или иного пола. РПХ не влияет на фертильность и развитие беременности. Наиболее часто РПХ возникает на четвертом или пятом десятилетии жизни, однако может дебютировать в любом возрасте [1–5, 8].
Этиология РПХ до сих пор остается неизвестной. Патофизиология неясна, как и причины обострений. На сегодняшний день не выявлены специфические факторы риска в окружающей среде.
РПХ относится к аутоиммунным заболеваниям, так как при нем обнаруживаются аутоантитела, чаще направленные к коллагену 2 типа. Вероятно, РПХ развивается при сочетании генетической предрасположенности, провоцирующих факторов и последующей патологической иммунной реакции [1–5]. Тем не менее эта гипотеза требует подтверждения, и проблема усугубляется тем, что адекватную животную модель РПХ создать не удалось.
Течение РПХ характеризуется чередованием периодов ремиссии и обострений. Клиническая картина крайне многообразна и зачастую требует консультаций врачей различных специальностей, в том числе хирургических. Начало болезни обычно острое и тяжелое. Наиболее частые клинические признаки — хондрит ушных раковин, сопровождающийся болью, эритемой, а также воспаление хрящей носа. Впоследствии могут развиться хондрит реберно-грудинных сочленений, верхних дыхательных путей, склерит и эписклерит, артралгии, а также разнообразные поражения кожи и слизистых. Описаны также поражения нервной системы [9].
Повторные атаки РПХ способны приводить к деструкции хряща и деформации носа, ушей и дыхательных путей. Наиболее опасные осложнения — трахеобронхомаляция и поражение восходящей аорты. Лихорадочный синдром, астения, снижение массы тела или сыпь могут быть в дебюте или при обострении болезни.
Поражение опорно-двигательного аппарата варьирует от простых артралгий до асимметричного мигрирующего неэрозивного артрита крупных и мелких суставов с частым вовлечением грудинно-реберных суставов.
Структуры глаза также являются мишенью воспаления при РПХ, оно отмечается примерно у 50% больных. Чаще всего развиваются склерит/эписклерит, увеит и конъюнктивит. Реже наблюдаются кератит, ретинопатия, нейропатия зрительного нерва, поражение глазодвигательных мышц и воспаление других структур орбиты [10]. Симптомы со стороны органа зрения могут быть одними из первых проявлений РПХ, однако с учетом низкой распространенности РПХ и неспецифичности офтальмологических проявлений данные симптомы сами по себе редко позволяют верифицировать диагноз.
Обычно все описанные симптомы РПХ появляются последовательно с течением времени, а их частота зависит от продолжительности болезни, ее активности и тяжести. Разнообразие клинической картины наряду с редкостью заболевания становится причиной диагностических ошибок, особенно в случае дебюта РПХ с неспецифических проявлений [1–5].
После того, как была проведена дифференциальная диагностика, необходимо исключить наличие ассоциированных аутоиммунных заболеваний [1–5]. Действительно, у трети больных с РПХ выявляются системные васкулиты, другие воспалительные или гематологические болезни. Они могут предшествовать, развиваться позже или одновременно с РПХ [1–5, 11].
Реальную сложность представляют ситуации, когда подозревают сочетание РПХ и васкулита, особенно АНЦА-ассоциированного, или проводится их дифференциальная диагностика. В таких случаях многие симптомы этих двух нозологий могут совпадать [11, 12]. Хондрит возможен при системной красной волчанке, болезни Бехчета и инфекционных заболеваниях. Хондрит ушных раковин описан у пациентов с лепрой [13]. Имеются сообщения о паранеопластическом характере РПХ [14]. Существует связь между РПХ и миелодиспластическими синдромами [15, 16]. Гематологические нарушения наблюдают примерно у 8–40% пациентов с РПХ, наиболее часто у мужчин старше 60 лет [1–5, 11].
Много вопросов возникает при попытках различить поражение почек при сочетании РПХ и других системных заболеваний — системных васкулитов, системной красной волчанки. У 22% пациентов отмечалось поражение почек при РПХ, однако этот вопрос является предметом дискуссии: ряд авторов полагает, что поражение почек в рамках РПХ не наблюдается, и его причиной послужили сочетанные заболевания [11, 12]. Изменения осадка мочи и данные биопсии почки крайне разнообразны.
Разнообразная клиническая картина и рецидивирующий характер болезни зачастую приводят к существенному увеличению сроков диагностики, которые в среднем колеблются от 1,9 до 10 лет, при этом до установления диагноза пациент обычно посещает около 5 врачей [5, 17].
Не существует специфических лабораторных или визуализирующих исследований для диагностики РПХ. Основная цель анализа крови — исключить сопутствующие заболевания и оценить активность болезни. Биопсия хряща не является обязательной для установления диагноза, однако может потребоваться в случае раннего, атипичного или крайне тяжелого течения болезни.
Среди визуализирующих исследований для выявления патологии дыхательных путей можно использовать КТ, МРТ, сцинтиграфию (с технецием-99m или галлием-67) и УЗИ с эффектом Доплера [1–5, 18].
В многочисленных исследованиях продемонстрирована ценность позитронно-эмиссионной томографии (ПЭТ) с фтордезоксиглюкозой для ранней диагностики болезни, выявления субклинического хондрита, оценки активности РПХ и уточнения распространенности поражений, а также выбора места биопсии и контроля эффективности лечения [19–24]. Наличие очагов с повышенным накоплением радиофармпрепарата в хрящевой ткани может стать новым критерием диагностики РПХ [19].
В настоящее время диагноз РПХ устанавливается, в первую очередь, на основании клинических данных. При наличии убедительного симптомокомплекса врач может использовать диагностические критерии McAdam и соавт. [25], Damiani и Levine [26], Michet и соавт. [27]. Критерии McAdam и соавт. [25] требуют выполнения как минимум трех условий из шести следующих:
1) двусторонний артрит ушных раковин;
2) неэрозивный серонегативный полиартрит;
3) хондрит носа;
4) поражение органа зрения;
5) хондрит дыхательных путей;
6) поражение кохлеарного и/или вестибулярного аппарата.
Damiani и Levine [26] расширили данные критерии, которые стали включать один критерий McAdam и соавт. плюс гистологическое подтверждение и/или эффективность глюкокортикоидов или дапсона. Диагноз РПХ основывается в основном на критериях Michet и соавт., для которых не нужна биопсия, однако требуется наличие доказанного хондрита как минимум двух из трех локализаций — поражение хрящей уха, носа или гортани/трахеи — или воспаление одного из этих хрящей плюс два других симптома, в том числе поражение органа зрения, вестибулярные нарушения, серонегативный атрит и снижение слуха [27].
Эти критерии [25–27] должны облегчить работу клиницистов, сталкивающихся с РПХ. Тем не мене у них есть ограничения. Во-первых, данные критерии были разработаны на ограниченном числе пациентов, наблюдавшихся в одном центре: 112 пациентов для критериев Michet и соавт. [27], 23 для критериев McAdam и соавт. [25] и всего 10 для критериев Damiani и Levine [26]. Во-вторых, ни у одного из этих исследований не было специального дизайна для разработки классификационных критериев. В-третьих, критерии не валидированы на независимой когорте. Все это является следствием редкости РПХ, и публикации по нему включают больных преимущественно одного центра. Необходимо, чтобы команды из разных стран, изучающие РПХ, объединили свои базы данных для изучения большего числа пациентов и разработки новых критериеы.
Оценка активности РПХ достаточно трудна. В недавнем исследовании не выявлена связь между клинической активностью, повышением островоспалительных показателей и результатами визуализирующих исследований [28]. У большинства пациентов активность заболевания низкая, но с большим числом обострений. Обычно обострения происходят в той же локализации и сопровождаются дальнейшим поражением хрящевой ткани, что приводит к постепенной инвалидизации или даже потере функции (слуха, зрения, голоса, острым сердечно-сосудистым событиям) вплоть до смертельного исхода.
Факторы неблагоприятного прогноза, выявленные в разных исследованиях, существенно различались [11, 17, 29]. Тяжесть состояния пациентов с РПХ также усиливают осложнения стероидной терапии.
Активность болезни обычно оценивается на основании жалоб и симптомов, повышения уровней островоспалительных маркеров, данных визуализирующих обследованиий — ларингоскопии, сцинтиграфии, КТ или МРТ трахеи. Значение генетических факторов, а также ряда экспериментальных биомаркеров в крови и моче требует уточнения.
В 2012 г. разработан индекс активности РПХ Relapsing Polychondritis Disease Activity Index [30], который является первой консенсусной шкалой для оценки болезни.
Данные свидетельствуют об увеличении общей выживаемости пациентов с РПХ: 5- и 10-летняя выживаемость возросла с 74 и 55% [27] 40 лет назад до 95 и 91% в 2012 г. [29]. Сходные оптимистичные результаты получены и в других исследованиях [17, 31]. Есть основания полагать, что совершенствование хирургических техник позволит уменьшить смертность от РПХ.
На настоящий день не существует клинических рекомендаций по лечению пациентов с РПХ. Редкость заболевания, гетерогенность клинической картины и непредсказуемость обострений частично объясняют сложности с проведением клинических исследований для оценки эффективности и безопасности терапии. Таким образом, в настоящее время используется эмпирический подход к лечению, базирующийся на отдельных наблюдениях [1–5, 32].
Несмотря на отсутствие клинических исследований или валидированных рекомендаций, глюкокортикостероиды (ГКС) являются единственными препаратами, повсеместно используемыми в лечении РПХ [1, 2]. Они показаны для терапии всех проявлений болезни на всех ее стадиях и позволяют добиться ремиссии у некоторых больных. Иногда требуется лечение высокими дозами ГКС или внутривенная пульс-терапия с целью купировании тяжелых обострений, а также в случае угрожающих жизни поражений. В зависимости от локализации поражений возможно использование ингаляционных, топических ГКС или их инъекции в барабанную полость в случае нейросенсорной тугоухости [33].
Обычно дозу ГКС снижают после достижения ремиссии, однако большинство больных нуждаются в постоянной поддерживающей дозе гормональных препаратов.
Стероид-зависимое или резистентное течение болезни, а также наличие угрожающих жизни осложнений — показания для начала приема стероид-сберегающих препаратов [1–5]. К таким препаратам относятся колхицин, дапсон, метотрексат, циклофосфамид, циклоспорин, хлорамбуцил, азатиоприн, микофенолата мофетил, внутривенный иммуноглобулин, миноциклин и лефлуномид, которые оказались эффективными у некоторых больных [3].
Эффективность дапсона [26, 34–36] описана у пациентов без поражения дыхательной или сердечно-сосудистой систем, однако его использование сопряжено с большим числом побочных эффектов [5]. На основании клинических наблюдений в отсутствие контролируемых исследований метотерксат является наиболее эффективным иммунодепрессантом и обладает наиболее выраженным стероид-сберегающим эффектом [5].
Внутривенное введение циклофосфамида и плазмаферез эффективны в случае развития жизнеугрожающих состояний или тяжелых висцеральных поражений, в том числе обструкции дыхательных путей, поражения органа зрения или гломерулонефрита [1, 37–39].
Аутоиммунная природа заболевания стала основным аргументом для использования таргетной биологической терапии у пациентов с РПХ, рефрактерным к стандартным иммунодепрессантам. Повышение экспрессии цитокинов при РПХ (ФНО-α, ИЛ-1, ИЛ-6), особенно при обострении [40, 41], обосновывало применение специфических ингибиторов данных цитокинов. Тем не мене нет клинических исследований, которые могли бы предоставить доказательную базу для использования генно-инженерных биологических препаратов (ГИБП) при РПХ.
С 2000-х годов началась волна публикаций об эффективности ГИБП при РПХ. Многие пациенты получали лечение анакинрой, анти-ФНО-α препаратами (инфликсимабом, этанерцептом, адалимумабом, цертолизумаба пэголом), абатацептом, ритуксимабом и тоцилизумабом. В обзоре литературы [32] авторы обобщают опыт лечения РПХ при помощи ГИБП, говоря о сложностях стандартизации ответа на терапию, ограниченном числе наблюдений, различной продолжительности наблюдения. Представляется важной и идея о том, что в реальности число случаев неэффективности ГИБП выше, поскольку такие случаи публикуются реже. Не найдены предикторы эффективности лечения. Данные по отдельным ГИБП обобщены в таблице.
Таблица. Эффективность генно-инженерных биологический препаратов при рецидивирующем полихондрите (данные 2017 г.) [42], число больных
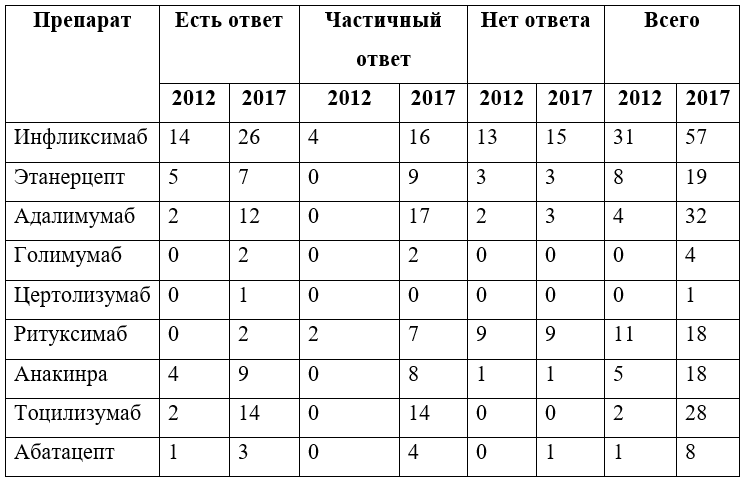
Имеющиеся данные, конечно, требуют обновления. Тем не менее, судя по количеству пациентов, получающих ГИБП, можно заключить, что интерес к биологическим препаратам при РПХ только растет. Число больных, получавших ГИБП при РПХ увеличилось с 62 в 2012 г. до 185 к маю 2017 г. (предварительные данные) [42]. Крайне желательно и даже необходимо собирать и анализировать данные различных клинических центров, имея стандартизованную систему оценки активности болезни и ответа на лечение. Проведение рандомизированных исследований при РПХ все еще представляется маловероятным.
С учетом ограничений, присущих отдельным клиническим наблюдениям, трансплантация органов может оказаться обнадеживающим способом помощи этим больным. Аутологичная трансплантация стволовых клеток или аллогенная трансплантация костного мозга у некоторых пациентов позволили добиться клинического улучшения или полной ремиссии. Трансплантация гематопоэтических клеток может обладать лечебным потенциалом при РПХ [43–46].
Некоторым пациентам требуются инвазивные вмешательства. Пролапс трахеи, ее стриктура или стеноз могут потребовать трахеостомии [3, 5, 11, 25]. В дальнейшем возможно использование техник дилатации трахеи, ее стентирование или реконструктивные операции в случае распространенных поражений. При нейросенсорной тугоухости можно использовать кохлеарные импланты. Седловидную деформацию носа можно исправить с помощью реконструктивных операций с использованием костного трансплантата из гребня подвздошной кости.
Аутоиммунная природа заболевания исключает применение хряща в качестве трансплантата в связи с его ожидаемой деструкцией [47]. В ряде наблюдений описана замена клапанов сердца или вмешательства по поводу аневризмы аорты [3].
Клиническое наблюдение
Приводим клиническое наблюдение пациентки с РПХ, резистентным к различным цитостатическим препаратам, стойкого улучшения у которой удалось добиться после начала лечения тофацитинибом.
Больная Б., 1979 года рождения, считает себя больной с 2012 г. (33 года), когда впервые отметила появление эпизодов носовых кровотечений. В апреле 2013 г. выявлена перфорация носовой перегородки, в сентябре она заметила, что меняется форма носа (седловидная деформация), консультировалась с лор-врачом. Направлена к ревматологу для исключения ревматических причин заболевания.
К этому времени пациентка перенесла непродолжительный артрит межфалангового сустава, по данным рентгенографии кистей рук, без существенных изменений, терапия НПВП дала эффект.
При обследовании выявлено повышение ревматоидного фактора, обсуждалось наличие ревматоидного артрита, однако в это же время впервые развилась инъекция склер (расценена офтальмологами как эписклерит), возникла боль в глазу, в связи с чем больная консультировалась с окулистом. Проводилась локальная терапия ГКС, в том числе инъекции, однако при попытках отмены у пациентки рецидивировали офтальмологические нарушения.
В середине октября появились постоянный кашель, осиплость голоса, лечение у лор-врачей не дало существенного эффекта. Прогрессировала общая слабость, появилась ломота, боли во втором глазу. С начала ноября — повышение температуры до субфебрильных значений. В ноябре впервые заметила снижение слуха. С учетом наличия признаков поражения лор-органов к этому моменту у больной обсуждалось наличие гранулематоза с полиангиитом, однако АНЦА при исследовании оказались в пределах референсных значений, в связи с чем больной рекомендована биопсия слизистой носа, которая оказалась неинформативной.
С этого времени температура тела постоянно была повышенной до 37,6°C, сохранялись выраженные артралгии, осиплость голоса, снижался слух.
Лабораторно отмечались повышение уровня СРБ до 21 мг/л, СОЭ — до 46 мм/ч, легкая анемия (уровень гемоглобина — 107 г/л). С учетом высокой активности болезни и ее прогрессирующего характера с поражением лор-органов и развитием функциональных ограничений (снижения слуха, лихорадки, постоянного кашня и дисфонии, выраженной слабости и болевого синдрома, поражения органа зрения) состояние расценено как локальный вариант гранулематоза с полиангиитом (гранулематоза Вегенера), и, несмотря на отсутствие морфологической или иммунологической верификации диагноза, начато лечение глюкокортикоидами.
С середины декабря 2013 г. пациентка получала преднизолон (ПЗ) в дозе 30 мг/сут, затем присоединен метотрексат с повышением до дозы 15 мг/нед. Ответ на терапию ГКС отмечен в первый же день приема стойко нормализовалась температура тела, постепенно уменьшились суставные боли. Регрессировали и остальные жалобы: прекратился кашель, исчезла осиплость голоса, нормализовался слух.
До апреля 2014 г. состояние пациентки оставалось удовлетворительным, воспалительноая активность отсутствовала (уровень СРБ — 2,4–4,7 мг/л). Постепенно снижалась доза ГКС. Весной 2014 г. больная перенесла несколько эпизодов кашля, осиплости голоса, субфебрилитета, которые вначале рассматривались как неспецифические инфекции, однако после появления постоянного кашля и субфебрилитета обсуждалось обострение васкулита на фоне снижения дозы ГКС.
Впервые пациентка госпитализирована в клинику в мае 2014 г. При поступлении жалобы на постоянный кашель с небольшим количеством мокроты, повышение температуры тела. С учетом поражения верхних дыхательных путей и эффекта глюкокортикоидов в дебюте заболевания диагноз не пересматривался. По результатам обследования выявлена высокая активность заболевания (повышение СОЭ до 53 мм/ч, субфебрилитет, кашель) и отрицательная динамика, по данным КТ (увеличение размеров перфорации в полости носа). АНЦА оставались отрицательными.
В связи с активностью васкулита проведен сеанс пульс-терапии метилпреднизолоном в дозе 500 мг № 3, доза метотрексата увеличена до 20 мг/нед. В результате лечения нормализовалась температура тела, уменьшился кашель, снизилась СОЭ. При выписке доза ПЗ — 7,5 мг/сут.
После выписки больная продолжала рекомендованное лечение. В течение 2014 г. сохранялась «тлеющая» активность болезни, в феврале 2015 г. появились жалобы на геморрагическое отделяемое из полости носа, шум (хрип) при вдохе и выдохе, на одышку в положении лежа и при небольшой физической нагрузке, боли в грудной клетке, а также тошноту. Метотрексат отменен в связи с тошнотой, отсутствием явного влияния на активность болезни и возможной провокацией вторичных инфекционных осложнений. Сохранялся также суставной синдром.
Обращало на себя внимание нетипичное течение предполагавшегося гранулематоза с полианигиитом — поражение верхних дыхательных путей было представлено в основном перфорацией носовой перегородки, дебют болезни с боли в орбитах и гиперемии склер без наличия псевдоопухоли, не отмечались выраженные синуситы, при этом постепенно присоединились боли в области хрящевых частей ребер и признаки поражения трахеи в виде хрипов и явлений трахеобронхиальной дискинезии без подскладочного ларингита.
Наблюдался отчетливый эффект глюкокортикоидов при отсутствии очевидного эффекта метотрексата. Впервые высказано предположение о наличии РПХ с поражением хрящей носа, ребер, трахеи, эписклеритом в дебюте и формированием соответствующих клинических проявлений. Для уточнения диагноза принято решении о выполнении ПЭТ-КТ.
По данным обследования: повышенное накопление радиофармпрепарата умеренной интенсивности в утолщенной и искривленной носовой перегородке, в мышцах и хрящах гортани, в утолщенной трахее, преимущественно в верней и средней трети, по ходу левого главного бронха, а также в проекции бронхопульмональных лимфоузлов с обеих сторон (рис. 1, 2).
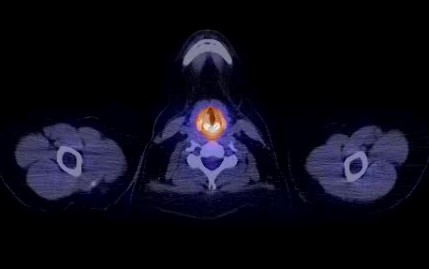
Рис. 1. Поражение хрящей гортани у пациентки с рецидивирующим полихондритом. Здесь и далее иллюстрации авторов
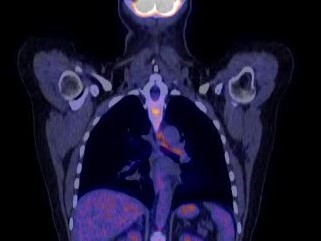
Рис. 2. Поражение левого главного бронха у пациентки с рецидивирующим полихондритом
С учетом стойкого отсутствия АНЦА, локализации воспаления в хрящевых структурах, а также клинических особенностей болезни (инъекция склер в дебюте — вероятный эписклерит, боли в области хрящевых частей ребер) диагноз изменен на РПХ. Доза ПЗ увеличена до 20 мг/сут. После повышения дозы ГКС стойко нормализовалась температура тела, регрессировали артралгии и боли в области ребер, не отмечались признаки поражения органа зрения. Воспалительной активности не было, начато медленное снижение дозы ГКС.
С июля 2015 г. к лечению добавлен азатиоприн в дозе 150 мг/сут, в октябре потребовалась отмена препарата в связи с лейкопенией. Доза ПЗ снижена за лето 2015 г. до 10 мг/сут, что сопровождалось ухудшением самочувствия в виде нарастания одышки, затруднения дыхания, тошноты, слабости. В качестве базисного препарата решено применять дапсон, прием ПЗ продолжен в дозе 10 мг/сут.
С января 2016 г. больная получала дапсон с отчетливым эффектом — удалось снизить дозу ПЗ, отсутствовали клинические признаки активности болезни. Для дальнейшего безопасного снижения дозы ГКС доза дапсона к марту 2016 г. увеличена до 150 мг в сутки, на фоне чего у пациентки появилась бессонница. В апреле 2016 г. — выраженная общая слабость, акроцианоз, повышение пульса до 100–110 в мин, одышка в покое, бледные кожные покровы; лабораторно зафиксированы выраженная лейкопения и анемия. Состояние расценено как осложнение терапии дапсоном, препарат отменен, начато лечение фолиевой кислотой.
В течение 2 недель после отмены дапсона указанные жалобы регрессировали, в анализах — разрешение лейкопении, повышение уровня гемоглобина. Содержание СРБ, СОЭ в норме. С учетом отчетливого клинического эффекта дапсона решено прием данного препарата возобновить, однако дозу уменьшить до 50 мг/сут из-за высокого риска токсичности. К сожалению, редуцированная доза не позволила поддержать ремиссию болезни и продолжить снижение дозы ГКС.
Осенью 2016 г. произошло повышение уровня СРБ до 24,1 мг/л, фибриногена — до 4,53 г/л; рецидивировали клинические проявления активности болезни — боль в проекции хрящевых частей ребер, эпизоды субфебрилитета, наросла осиплость голоса. Сохранялись отделение кровянистых корочек из полости носа, периодически — лающий кашель.
В декабре 2016 г. пациентку повторно госпитализировали, подтверждена высокая активность болезни — отделение корочек из полости носа, субфебрилитет, хондралгии, кашель, а также выраженное повышение СОЭ (47 мм/ч), концентраций СРБ (43,1 мг/л), фибриногена (5,4 г/л). По результатам КТ, зафиксирована отрицательная динамика: увеличение размеров дефекта в перегородке носа, вовлечение новых хрящей в гортани, персистирование патологического процесса в трахее (утолщение стенок). По данным ФВД, впервые выявлено существенное нарушение динамики потока на уровне верхних дыхательных путей, за время наблюдения в клинике сатурация О2 86–94%, впервые зафиксирована дыхательная недостаточность.
Таким образом, несмотря на длительную терапию различными базисными препаратами, отчетливый эффект отмечался только от стероидной терапии, на фоне увеличения дозы ГКС воспалительная активности и жалобы уменьшались, при этом дальнейшее использование средних доз ГКС представлялось сопряженным с высоким риском осложнений. Отчетливого эффекта от базисных препаратов не было.
У пациентки, несмотря на длительную терапию с использованием различных иммунодепрессантов, отмечалось прогрессирование заболевания с разрушением структур гортани и трахеи, тяжелой деформацией носа, нарастанием дыхательной недостаточности и выраженным косметическим дефектом. С целью подавления активности процесса принято решение о терапии препаратами второго ряда, коллегиально в составе консилиума специалистов принято решение начать лечение тофацитинибом.
С апреля 2017 г. больная стала принимать тофацитиниб в дозе 10 мг/сут, переносимость лечения удовлетворительная. Доза ПЗ на момент начала лечения — 15 мг/сут. К июню стала видна отчетливая положительная динамика: температура тела стойко нормализовалась, не отмечались боли в проекции хрящевых частей ребер, осиплость голоса, ломота, кашель был редко. Лабораторно все острофазовые показатели сохранялись стойко в норме(уровень СРБ — 3,4 мг/л, СОЭ — 15 мм/ч). Зафиксировано достижение как клинической, так и лабораторной ремиссии на фоне терапии тофацитинибом, доза ПЗ снижена до 10 мг/сут.
Осенью 2017 г. пациентка продолжала прием тофацитиниба в прежней дозировке, постепенно снижалась доза ПЗ, клинико-лабораторные признаки активности заболевания не выявлялись. По данным КТ гортани, отмечена положительная динамика. К январю 2018 г. стероидная терапия была прекращена полностью, при этом жалобы не рецидивировали, СОЭ, уровни СРБ, фибриногена сохранялись стойко в норме (уровень СРБ — 2,7 мг/л, СОЭ — 11 мм/ч).
Рекомендовано продолжить терапию тофацитинибом, осуществлять динамический контроль лабораторных показателей и данных КТ. В настоящее время (начало 2023 г.) больная продолжает терапию тофацитинибом, доза уменьшена до 5 мг в связи с эпизодами лейкопении (до 3,4 тыс/мкл), сохраняется стойкая ремиссия болезни.
Обсуждение
Данное наблюдение демонстрирует ряд типичных для РПХ особенностей. Обсуждая дебют, необходимо отметить достаточно характерное постепенное появление симптомов заболевания, начиная от длительно скрыто протекающего хондрита носовой перегородки с последующим последовательным присоединением артритов, поражения дыхательных путей, органа зрения. В этом же и состояла трудность диагностики: на момент дебюта заболевания клиническая картина была крайне спутанной. Несмотря на ошибку в диагностике конкретной нозологии, в целом понимание патологического процесса оказалось верным: аутоиммунное заболевание, требующее иммуносупрессивной терапии. При этом, тем не менее, дополнительное внимание стоит уделять вариантам АНЦА-негативных васкулитов, добиваясь морфологической верификации и исключая все гематопролиферативные, инфекционные и другие ревматические заболевания.
Высокая активность заболевания в дебюте, проявлявшаяся лихорадкой и выраженной астенией, поражением органа зрения, несмотря на сомнительные результаты биопсии, диктовала необходимость лечения, которое оказалось высокоэффективным, что, в свою очередь, отодвинуло установление правильного диагноза.
Потребовалось достаточно продолжительное время, чтобы внимание клиницистов привлекли крайне резистентный к различным цитостатикам, рецидивирующий характер «васкулита», а также новые нетипичные жалобы, которые стали ведущими в клинической картине. Пересмотр диагноза позволил объединить в рамках РПХ неэрозивные артриты, поражение грудино-реберных сочленений, трахеи (а не подскладковый стеноз), органа слуха и глаз в дебюте болезни. Стало также понятным отсутствие выраженных синуситов, которые были бы закономерны в случае гранулематоза с полиангиитом.
С учетом инвазивности биопсии и неинформативного ее характера при исследовании в дебюте заболевания решено выполнить ПЭТ-КТ с расчетом выявления воспаленной хрящевой ткани. Диагностический поход оправдал себя, диагноз был подтвержден (см. рис. 1, 2). В целом, как отмечалось выше, прослеживается достаточно оптимистичное отношение к ПЭТ для диагностики и оценки активности РПХ, и в данном наблюдении наш опыт совпал с мнением других авторов [19–22].
Смена диагноза расширила терапевтические возможности, хотя проводившееся ранее лечение не противоречило новому диагнозу. Дапсон оказался достаточно эффективным у данной больной, однако прием терапевтической дозы привел к развитию серьезных побочных эффектов. С учетом накопленных за время лечения глюкокортикоидами побочных эффектов и угрожающего хирургическим вмешательством поражения трахеи стала необходимой стероид-сберегающая терапия.
Выбор препарата обосновывался прерыванием сигнальных путей на раннем этапе, что способствует воздействию ингибиторов Янус-киназы на множество нозологий. Не последнюю роль в выборе средства лечения сыграл научный азарт: на момент назначения препарата ни одного наблюдения использования тофацитиниба не было опубликовано, при подготовке публикации к печати подобные наблюдения также не найдены.
Эффект от проводимой терапии впечатляет: у пациентки удалось купировать большинство симптомов заболевания, связанных с его активностью, полностью прекратить прием глюкокортикоидов, она даже похудела на 8 кг, при этом переносимость лечения была удовлетворительной. Достигнута лабораторная ремиссия, и при КТ гортани отмечена положительная динамика, однако в данной ситуации хочется все же избежать излишнего оптимизма: известны случаи прогрессирования хондрита при клинико-лабораторной ремиссии, а также наблюдения «ускользания» эффекта от длительного лечения. Кроме того, иммуносупрессивная терапия сама по себе сопряжена с более высоким риском инфекционных осложнений.
Таким образом, на сегодняшний день достигнут очевидный результат лечения, однако не вызывает сомнений, что пациентке потребуется продолжительная терапия с постоянной оценкой активности болезни и безопасности лечения.
Заключение
Рецидивирующий полихондрит — редкое заболевание, которое за 100 лет все так же сохраняет множество тайн и вопросов. Остается большое количество сложностей, связанных с пониманием патофизиологии и ранней диагностикой, оценкой активности и прогноза и, конечно, лечением. Решению указанных проблем будет способствовать объединение данных из различных центров всего мира. Тогда, возможно, удастся продвинуться вперед к лучшему пониманию механизмов развития, разработке новых диагностических критериев, прогностических факторов. Более того, необходимо проведение рандомизированных клинических исследований для создания доказательных рекомендаций по лечению.
Предыдущая статья
И.Р. Гайсин ФГБОУ ВО «Ижевская государственная медицинская академия» Министерства здравоохранения...
Следующая статья
Т.М. Максикова, А.Н. Калягин, М.В. Карнакова ФГБОУ ВО «Иркутский государственный медицинский унив...