Взаимосвязь показателей вариабельности гликемии и нарушений сердечного ритма у пациентов с сахарным диабетом 1 типа
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Дедов И.И., Шестакова М.В., Викулова О.К., Железнякова А.В. и др. Сахарный диабет в Российской Федерации: динамика эпидемиологических показателей по данным Федерального регистра сахарного диабета за период 2010–2022 гг. Сахарный диабет. 2023;26(2):104–23. Dedov I.I., Shestakova M.V., Vikulova O.K., Zheleznyakova A.V. et al. Diabetes mellitus in the Russian Federation: dynamics of epidemiological indicators according to the Federal Register of Diabetes Mellitus for the period 2010–2022. Diabetes Mellitus. 2023;26(2):104– (in Russian). DOI: 10.14341/DM13035
- Vinik A.I., Erbas T., Casellini C.M. Diabetic cardiac autonomic neuropathy, inflammation and cardiovascular disease. J. Diabetes Investig. 2013;(4)1:4–18. DOI: 10.1111/jdi.12042
- Торшхоева Х.М., Ткачева О.Н., Подпругина Н.Г., Пироева К.Э. и др. Диабетическая кардиоваскулярная автономная нейропатия. Сахарный диабет. 2004;7(1)38–45. Torshkhoeva K., Tkacheva O., Podprugina N., Piroeva K. et al. Diabeticheskaya kardiovaskulyarnaya avtonomnaya neyropatiya. Diabetes mellitus. 2004;7(1):38–45. (in Russian). DOI: 14341/2072-0351-5900
- Spallone V. Update on the impact, diagnosis and management of cardiovascular autonomic neuropathy in diabetes: what is defined, what is new, and what is unmet. Diabetes Metab. J. 2019;43(1):3– DOI: 10.4093/dmj.2018.0259
- Buse J.B., Ginsberg H.N., Bakris G.L., Clark N.G. et al. Primary prevention of cardiovascular diseases in people with diabetes mellitus: a scientific statement from the American Heart Association and the American Diabetes Association. Diabetes Care. 2007;30(1):162–72. DOI: 10.2337/dc07-9917
- Лаптев Д.Н., Рябыкина Г.В., Корнеева И.Т., Поляков С.Д. Влияние автономной дисфункции на восстановление частоты сердечных сокращений и вариабельности ритма сердца при проведении нагрузочного тестирования у детей и подростков с сахарным диабетом 1-го типа. Проблемы эндокринологии. 2015;61(3):23–9. Laptev D.N., Ryabykina G.V., Korneeva I.T., Polyakov S.D. et al. The influence of autonomous dysfunction on the restoration of the heart rate and cardiac rhythm variability under loading test conditions in the children and adolescents presenting with type 1 diabetes mellitus. Problems of Endocrinology. 2015;61(3):23–9. (in Russian). DOI: 14341/probl201561323-29
- Gardim C.B., de Oliveira B.A., Bernardo A.F., Gomes R.L. et al. Heart rate variability in children with type 1 diabetes mellitus. Rev. Paul. Pediatr. 2014;32(2)279–85. DOI: 10.1590/0103-0582201432215513
- Kusunoki Y., Konishi K., Tsunoda T., Koyama H. Significance of glycemic variability in diabetes mellitus. Intern. 2022;61(3):281–90. DOI: 10.2169/internalmedicine.8424-21
- Климонтов В.В. Влияние вариабельности гликемии на риск развития сердечно-сосудистых осложнений при сахарном диабете. Кардиология. 2018;58(10)80–7. Klimontov Impact of glycemic variability on cardiovascular risk in diabetes. Kardiologiia. 2018;58(10)80–7. (in Russian). DOI: 10.18087/cardio.2018.10.10152
- Saisho Y. Glycemic variability and oxidative stress: a link between diabetes and cardiovascular disease? Int. J. Mol. 2014;15(10)18381–406. DOI: 10.3390/ijms151018381
- Ceriello A., Monnier L., Owens D. Glycaemic variability in diabetes: clinical and therapeutic implications. Lancet Diabetes Endocrinol. 2019;7(3)221–30. DOI: 10.1016/S2213-8587(18)30136-0
- Helleputte S., De Backer T., Lapauw B., Shadid S. et al. The relationship between glycaemic variability and cardiovascular autonomic dysfunction in patients with type 1 diabetes: a systematic review. Diabetes Metab. Res. 2020;36(5):e3301. DOI: 10.1002/dmrr.3301
- Дедов И.И., Шестакова М.В., Майоров А.Ю., Мокрышева Н.Г. и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом (11-й выпуск). Сахарный диабет. 2023;26(2S):1–231. Dedov I.I., Shestakova M.V., Mayorov A.Yu., Mokrysheva N.G., et al. Standards of specialized diabetes care (11th issue). Diabetes Mellitus. 2023;26(2S):1–231. (in Russian). DOI: https://doi.org/10.14341/DM13042
- Семенова Ю.Ф., Климонтов В.В. Референсные значения суточных, дневных и ночных показателей вариабельности гликемии у лиц с нормальной толерантностью к глюкозе. Сахарный диабет. 2022;25(2):104–11. Semenova J.F., Klimontov V.V. Reference values of 24-hour, day-time and nocturnal glucose variability parameters in subjects with normal glucose tolerance. Diabetes mellitus. 2022;25(2):104–11. (in Russian). DOI: 14341/DM12793
- Lachin J.M., Bebu I., Bergenstal R.M., Pop-Busui R. et al. Association of glycemic variability in type 1 diabetes with progression of microvascular outcomes in the diabetes control and complications trial. Diabetes Care. 2017;40(6):777–83. DOI: 10.2337/dc16-2426
- Черникова Н.А., Камынина Л.Л., Аметов А.С. Кардиометаболическая оценка вариабельности гликемии у пациентов с сахарным диабетом 2 типа: роль глюкокардиомониторирования. Кардиология. 2020;60(5):100–6. Chernikova N.A., Kamynina L.L., Ametov A.S. The сardiometabolic assessment of the glycemic variability in patients with diabetes mellitus: the role of the glucocardiomonitoring. Kardiologiia. 2020;60(5):100–6. (in Russian). DOI: 18087/cardio.2020.5.n902
- Andreasen C.R., Andersen A., Hagelqvist P.G., Maytham K. et al. Sustained heart rate-corrected QT prolongation during recovery from hypoglycaemia in people with type 1 diabetes, independently of recovery to hyperglycaemia or euglycaemia. Diabetes Obes. Metab. 2023;25(6)1566–75. DOI: 10.1111/dom.15005
- Валеева Ф.В., Шайдуллина М.Р. Диагностика диабетической автономной кардиальной нейропатии у больных сахарным диабетом 1 типа. Сахарный диабет. 2009;12(4):55–60. Valeeva F.V., Shaydullina M.R. Diagnosis of diabetic autonomous cardioneuropathy in patients with type 1 diabetes mellitus. Diabetes mellitus. 2009;12(4):55–60. (in Russian). DOI: 14341/2072-0351-5706
Цель исследования: изучить показатели вариабельности гликемии (ВГ) и их взаимосвязь с нарушениями сердечного ритма у пациентов с сахарным диабетом (СД) 1 типа по данным глюкокардиомониторирования.
Дизайн: одномоментное поперечное исследование.
Материалы и методы. В исследование вошли 72 пациента с СД 1 типа без ранее диагностированной сердечно-сосудистой патологии. Из них 34 человека получали помповую инсулинотерапию, 38 — множественные инъекции инсулина. Средний возраст больных составил 39,7 ± 15,9 года, средняя длительность СД 1 типа — 15,4 ± 10,8 года.
У пациентов определяли уровень гликированного гемоглобина (HbA1c), по данным непрерывного мониторирования глюкозы (НМГ) рассчитывали индексы ВГ: SD (стандартное отклонение), CONGA (непрерывное частично перекрывающееся изменение гликемии), LI (индекс лабильности гликемии), MAGE (среднюю амплитуду колебаний гликемии), MAG (среднее абсолютное значение гликемии). Одновременно с НМГ осуществлялось холтеровское мониторирование электрокардиограммы: оценивались показатели частоты сердечных сокращений (ЧСС), наличие и время возникновения аритмий, вариабельность корригированного интервала QT (QTс), наличие ишемических изменений.
Произведен корреляционный анализ взаимосвязей между уровнями ВГ и нарушениями ритма сердца.
Результаты. Независимо от вида инсулинотерапии показатели ВГ у пациентов с СД 1 типа были выше референсных значений для здоровых лиц. Целевого уровня HbA1c достигли только 19 (26%) пациентов. У 62 (86%) человек зарегистрированы различные нарушения ритма сердца, у 30 (42%) — снижение циркадного индекса (ЦИ) ЧСС, у 14 (19%) – удлинение интервала QTс. Результаты корреляционного анализа показали, что при увеличении ВГ снижался ЦИ ЧСС и возрастала частота наджелудочковых и желудочковых экстрасистол.
Заключение. Выявленные изменения ритма сердца на фоне увеличения ВГ у пациентов с СД 1 типа указывают на высокий риск формирования сердечно-сосудистой патологии. Строгий гликемический контроль и нормализация ВГ позволят снизить риск возникновения нарушений ритма сердца и развития ДКАН у пациентов с СД 1 типа.
Ключевые слова: вариабельность гликемии, диабетическая кардиоваскулярная автономная нейропатия, сахарный диабет 1 типа, сердечно-сосудистые заболевания
Скачать PDFЧерная М.Е., Корчагина Ж.В., Халимов Ю.Ш., Бутомо М.И., Шихалиев Д.Р., Нерсесян А.А., Лискер А.В., Волкова А.Р. Взаимосвязь показателей вариабельности гликемии и нарушений сердечного ритма у пациентов с сахарным диабетом 1 типа. Вестник терапевта. 2023. № 4 (59). DOI: 10.31550/2712-8601-VT-2023-4-4. URL: https://journaltherapy.ru/statyi/vzaimosvyaz-pokazatelej-variabelnosti-glikemii-i-narushenij-serdechnogo-ritma-u-pacientov-s-saharnym-diabetom-1-tipa/ (дата обращения: дд.мм.гггг)
Черная Мария Евгеньевна (автор для переписки) — ассистент кафедры терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. eLIBRARY SPIN: 7249-268. https://orcid.org/0000-0001-6567-6990. E-mail: Mashaeatworld@gmail.com.
Корчагина Жанна Владиславовна — врач-эндокринолог научно-клинического центра эндокринологии научно-клинического исследовательского центра ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. https://orcid.org/0000-0001-7223-2378. E-mail: fedulova.zhanna@gmail.com
Халимов Юрий Шавкатович — д. м. н., профессор, заслуженный врач РФ, главный эндокринолог Комитета по здравоохранению Правительства Санкт-Петербурга, главный эндокринолог Министерства обороны РФ, заведующий кафедрой терапии факультетской с курсом эндокринологии, кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. eLIBRARY SPIN: 7315-6746. https://orcid.org/0000-0002-7755-7275. E-mail: yushkha@gmail.com.
Бутомо Мария Игоревна — к. м. н., заведующая отделением функциональной диагностики № 1, доцент кафедры функциональной диагностики ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. eLIBRARY SPIN: 9000-8840. https://orcid.org/0000-0003-2506-0862. E-mail: mbutomo@mail.ru.
Шихалиев Джошгун Рагим Оглы — врач отделения функциональной диагностики № 1, ассистент кафедры функциональной диагностики ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. https://orcid.org/0000-0002-8591-7576. E-mail: ftkafedra@mail.ru
Нерсесян Артем Артурович — студент 6-го курса лечебного факультета ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. https://orcid.org/0000-0003-0936-9915. E-mail: Artem_Nersesyan00@mail.ru
Лискер Анна Владимировна — заведующая эндокринологическим отделением научно-клинического центра эндокринологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. eLIBRARY SPIN: 3688-1505. https://orcid.org/0000-0003-4295-1202. E-mail: a.lisker@mail.ru.
Волкова Анна Ральфовна — д. м. н., профессор кафедры терапии факультетской с курсом эндокринологии и кардиологии с клиникой имени академика Г.Ф. Ланга ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8. eLIBRARY SPIN: 4007-1288. https://orcid.org/0000-0002-5189-9365. E-mail: volkovaa@mail.ru.
Correlation of indicators of glycemic variability and cardiac arrhythmias in patients with type 1 diabetes mellitus
M.E. Chernaya, Zh.V. Korchagina, Yu.Sh. Khalimov, M.I. Butomo, D.R. Shikhaliev, A.A. Nersesyan, A.V. Lisker, A.R. Volkova
Pavlov First Saint Petersburg State Medical University; 6–8 L’va Tolstogo Str., Saint Petersburg, Russian Federation 197022
Abstract
Objective: To study indicators of glycemic variability (GV) and their relationship with cardiac arrhythmias in patients with type 1 diabetes mellitus according to glucocardiomonitoring data.
Design: Cross-sectional study.
Materials and methods. The study included 72 patients with type 1 diabetes without previously diagnosed cardiovascular pathology. Of these, 34 patients received insulin pump therapy, 38 received multiple insulin injections. The average age of patients was 39.7 ± 15.9 years, the average duration of type 1 diabetes was 15.4 ± 10.8 years.
The level of glycated hemoglobin (HbA1c) was determined in patients, and according to continuous glucose monitoring (CGM), GV indices were calculated: SD (standard deviation), CONGA (continuous overall net glycemic action), LI (lability index), MAGE (mean amplitude of glycemic excursions), MAG (mean absolute glucose). Simultaneously with CGM, Holter monitoring of the electrocardiogram was carried out: heart rate (HR), the presence and time of occurrence of arrhythmias, variability of the corrected QT interval (QTc), and the presence of ischemic changes were assessed.
A correlation analysis of the relationships between GV levels and heart rhythm disorders was carried out.
Results. Regardless of the type of insulin therapy, GV indicators in patients with type 1 diabetes were higher than the reference values for healthy individuals. Only 19 (26%) patients reached the target HbA1c level. In 62 (86%) people, various heart rhythm disturbances were registered, in 30 (42%) of patients there was a decrease in the circadian index (CI) of heart rate, and in 14 (19%) there was a prolongation of the QTc interval. The results of the correlation analysis showed that with an increase in GV, the HR CI decreased and the frequency of supraventricular and ventricular extrasystoles increased.
Conclusion. The detected changes in heart rhythm against the background of increased GV in patients with type 1 diabetes indicate a high risk of developing a cardiovascular process. Strict glycemic control and normalization of GV can better reduce the risk of cardiac arrhythmia and the development of DCAN in patients with type 1 diabetes.
Keywords: type 1 diabetes mellitus, glycemic variability, cardiovascular disease, diabetic cardiovascular autonomic neuropathy.
М.Е. Черная, Ж.В. Корчагина, Ю.Ш. Халимов, М.И. Бутомо, Д.Р. Шихалиев, А.А. Нерсесян, А.В. Лискер, А.Р. Волкова
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения Российской Федерации; Россия, г. Санкт-Петербург
Сахарный диабет (СД) 1 типа — хроническое социально значимое заболевание, обусловленное развитием абсолютной инсулиновой недостаточности, которое, как правило, диагностируется у людей молодого возраста — детей, подростков, взрослых до 30 лет. В Российской Федерации в последнее время наблюдается рост распространенности СД 1 типа: с 2020 года заболеваемость увеличилась со 146 до 191 человека на 100 тысяч населения, то есть более чем на 30%; к 2023 году на диспансерном учете состоит 277 100 человек [1].
Среди причин смерти пациентов с СД 1 типа первое место занимают сердечно-сосудистые заболевания[1]. По данным Федерального регистра больных СД, в России на 2023 год доля сердечно-сосудистой патологии (ССП) в структуре смертности пациентов с СД 1 типа составила 38,6% [1].
Одним из наиболее часто встречаемых и при этом редко диагностируемых осложнений СД, связанных с ССП, считается диабетическая кардиоваскулярная автономная нейропатия (ДКАН) — форма диабетической автономной нейропатии, которая возникает вследствие повреждения вегетативных нервных волокон, иннервирующих сердце и кровеносные сосуды, что приводит к нарушениям контроля частоты сердечных сокращений (ЧСС) и сосудистого тонуса [2]. По разным данным, ДКАН выявляется у 20–25% больных СД 1 типа и является серьезным фактором риска развития поздних осложнений СД и инвалидизации пациентов, а также увеличивает риск смерти в 4 раза [2, 3].
У пациентов с ДКАН наблюдаются нарушение переносимости физических нагрузок и изменения сердечного ритма, проявляющиеся в виде тахикардии покоя и склонности к аритмиям, ортостатическая гипотензия, безболевая ишемия миокарда, а также снижение вариабельности сердечного ритма (ВСР), что ассоциировано с риском внезапной сердечной смерти [4]. Изменения ЧСС и ВСР отмечаются как во время физических нагрузок, так и в восстановительном периоде, что также является неблагоприятным предиктором ССП и смерти у пациентов с СД 1 типа [5].
Важно отметить, что начальные проявления ДКАН могут быть выявлены у пациентов с СД 1 типа уже в детстве, что неизбежно влечет возрастание риска ССП и смерти в зрелом возрасте [6, 7]. При ДКАН происходит раннее нарушение парасимпатической иннервации сердца и сосудов и увеличение симпатического тонуса, приводящие к повышению ЧСС в покое и нарушению сердечного ритма, характерна также симпатическая денервация, которая распространяется с вершины желудочков к основанию сердца, что также ассоциировано с формированием нарушений сердечного ритма, патогенетической основой которых является повышенное образование активных форм кислорода и оксидативный стресс [2, 8].
В последнее время активно изучается влияние гипергликемии на риски развития ССП [8]. Важно учитывать, что хроническая гипергликемия при низкой вариабельности гликемии (ВГ) в меньшей степени активирует оксидативный стресс, чем интермиттирующая гипергликемия при высокой ВГ, что связано с активацией адаптивных механизмов [9, 10]. Помимо этого, с увеличением ВГ возрастает и риск развития гипогликемических состояний, также обуславливающий усиление оксидативного стресса [11].
Однако неоднородность методологических подходов в имеющихся научных работах и разрозненность представленных в них данных затрудняет сравнение и анализ полученных результатов [12]. Кроме того, поскольку наджелудочковая и желудочковая экстрасистолии у молодых пациентов с СД 1 типа может протекать бессимптомно, требуется поиск наиболее информативных методов исследования.
Цель исследования: изучить показатели ВГ и их взаимосвязь с нарушениями сердечного ритма у пациентов с СД 1 типа по данным глюкокардиомониторирования.
Материалы и методы
В исследование вошли 72 пациента с СД 1 типа без ранее диагностированной сердечно-сосудистой патологии, получавшие лечение в условиях стационара в эндокринологическом отделении ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России в 2019–2022 годах. Средний возраст больных составил 39,7 ± 15,9 года, средняя длительность СД 1 типа — 15,4 ± 10,8 года. В исследование не включались пациенты с ранее диагностированной ишемической болезнью сердца, перенесенным инфарктом миокарда, а также лица, получающие антиаритмическую терапию.
В зависимости от вида проводимого лечения пациенты были разделены на две группы: в 1-ю вошли 34 человека, получавшие помповую инсулинотерапию с использованием аналогов инсулина ультракороткого действия (инсулина аспарт и инсулина лизпро), во 2-ю — 38 больных, которым осуществляли множественные инъекции инсулина аналогами длительного и сверхдлительного (инсулина гларгин и инсулина деглудек) и ультракороткого действия (инсулина аспарт и инсулина лизпро).
Исследуемые группы существенно не различались по основным параметрам (полу, возрасту, длительности СД), что позволило объединить их для дальнейшего изучения (табл. 1).
Таблица 1. Характеристика исследуемых групп пациентов

Для каждого пациента был определен индивидуальный целевой уровень гликированного гемоглобина (HbA1c) согласно клиническим рекомендациям [13]. Содержание HbA1c оценивалось иммунохимическим методом, ВГ диагностировалась на основании данных непрерывного мониторирования глюкозы (НМГ) тканевой жидкости системой iPro-2 с применением сенсора Enlite (Medtronic, CША).
В ходе исследования c помощью программного обеспечения EasyGV Ver. 9.0R2 (Oxford University) были рассчитаны следующие индексы ВГ: SD (standard deviation) — стандартное отклонение, CONGA (continuous overall net glycemic action) — непрерывное частично перекрывающееся изменение гликемии, LI (lability index) — индекс лабильности гликемии, MAGE (mean amplitude of glycemic excursions) — средняя амплитуда колебаний гликемии, MAG (mean absolute glucose) — среднее абсолютное значение гликемии.
Всем пациентам параллельно с НМГ в течение 24 часов проводилось холтеровское мониторирование электрокардиограммы (ХМ-ЭКГ) с помощью монитора Кардиотехника-07 (ИНКАРТ). Оценивались показатели ЧСС, наличие и время возникновения аритмий, изменения корригированного интервала QT (QTc), циркадный индекс (ЦИ) ЧСС, наличие ишемических изменений сегмента ST.
Статистическая обработка данных осуществлялась с использованием пакета программ Statistica 13.3 for Windows. Для оценки нормальности распределения в группах использовался критерий Шапиро — Уилка. Результаты исследования показателей ВГ представлены в виде медианы, 1-го и 3-го квартилей (Me [Q1; Q3]). Для дальнейшего анализа использовался U-критерий Манна — Уитни. Для оценки корреляционных взаимосвязей рассчитывался коэффициент корреляции Пирсона. Различия считались статистически значимыми при р < 0,05.
Результаты
По данным ХМ-ЭКГ у пациентов исследуемых групп средняя ЧСС составила днем 82,1 ± 8,8 уд/мин (от 66 до 107 уд/мин), ночью — 65 ± 9,9 уд/мин (от 46 до 86 уд/мин). Среднее значение ЦИ ЧСС — 1,27 ± 0,17 (от 0,95 до 1,7). У 30 (42%) пациентов было выявлено снижение ЦИ ЧСС менее 1,2, что является признаком ДКАН, а также отсутствие физиологического снижения ЧСС ночью. У 8 (11%) пациентов зарегистрирован ЦИ ЧСС выше 1,5 — показатель повышенной восприимчивости сердца к симпатической стимуляции.
Клинически значимым параметром оценки ХМ-ЭКГ является длительность интервала QTc по формуле Bazett (QTc = QT / (√RR / 60)), который в норме не превышает 440 мс. У 14 (19%) пациентов было зарегистрировано удлинение интервала QTс от 450 до 488 мс. По результатам ХМ-ЭКГ у 62 (86%) пациентов диагностированы различные аритмии, у 60 (83%) выявлены наджелудочковые нарушения ритма, у 8 (11%) — желудочковые нарушения ритма III и более градации по M. Ryan, у 19 (26%) больных число суточных желудочковых нарушений ритма превышало норму. Количество аритмий у пациентов исследуемых групп было сопоставимым (p > 0,05). Ишемических изменений сегмента ST у пациентов в период мониторирования выявлено не было.
Целевые значения HbA1c были достигнуты только у 19 (26%) человек, в том числе у 10 (29%) — в 1-й и у 9 (24%) — во 2-й группе. У пациентов с СД 1 типа зарегистрирована более высокая ВГ, чем у здоровых лиц [14]. Индекс CONGA был значимо ниже у пациентов на помповой инсулинотерапии, чем у больных, получающих множественные инъекции инсулина (р = 0,04), остальные индексы ВГ существенно не различались (табл. 2).
Таблица 2. Показатели вариабельности гликемии у пациентов исследуемых групп, Me [Q1; Q3]
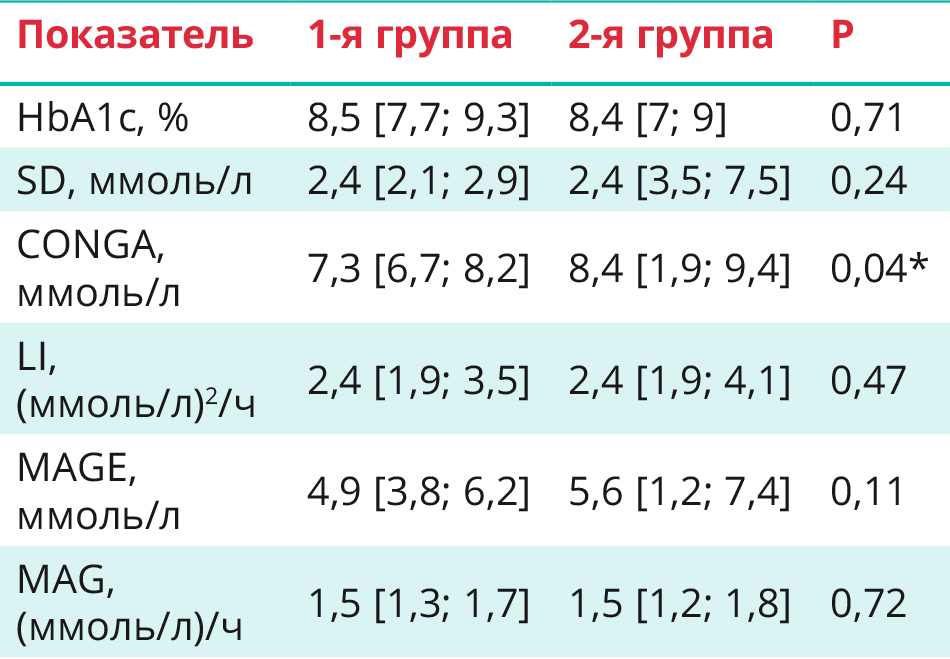
* Различия статистически значимы.
По результатам корреляционного анализа были выявлены слабые обратные корреляционные связи между ЦИ ЧСС и индексом CONGA (r = –0,1), а также индексом MAGE (r = –0,2). Между ЦИ ЧСС и индексом LI определена слабая обратная корреляционная связь (r = 0,15). Так, при увеличении ВГ несколько снижался ЦИ ЧСС, что является признаком автономной дисфункции. Прямая слабая корреляционная связь была установлена между количеством наджелудочковых экстрасистол и индексами LI (r = 0,14), MAGE (r = 0,1) и MAG (r = 0,16). При увеличении лабильности гликемии и скорости ее изменения несколько возрастала частота наджелудочковых экстрасистол. Обнаружены прямые умеренно выраженные корреляционные связи между суточным количеством желудочковых экстрасистол и значениями индексов MAGE (r = 0,31) и MAG (r = 0,23). Между числом желудочковых аритмий и индексом LI выявлена слабая прямая корреляционная связь (r = 0,2). Таким образом, с увеличением ВГ количество желудочковых экстрасистол возрастало. Возникновение эпизодов нарушения ритма у пациентов с СД 1 типа было связано по времени с резкими колебаниями гликемии (рис.).
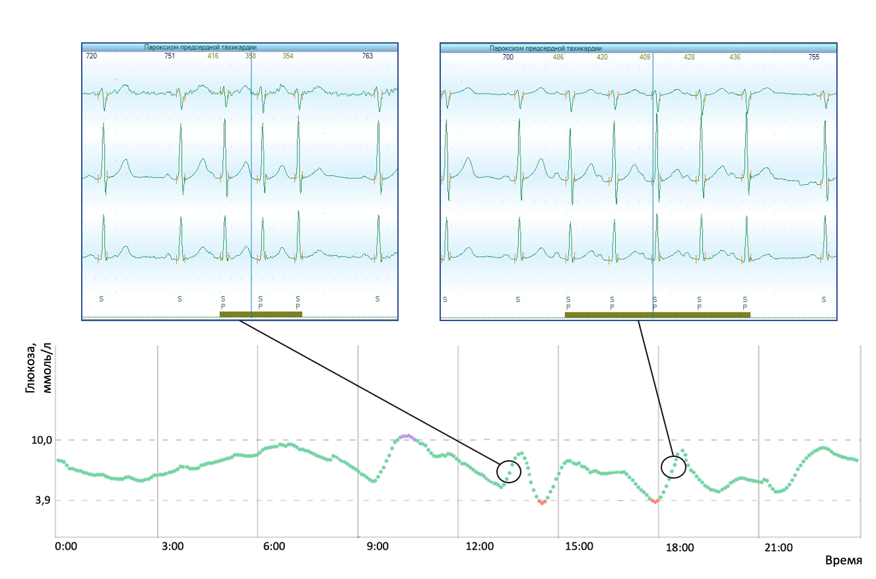
Рис. Графики колебаний уровня глюкозы и сердечного ритма пациента П. при глюкокардиомониторировании. В периоды установления показателей глюкозы в целевом диапазоне при высокой скорости изменения гликемии (MAG > 5 ммоль/л/ч) отмечены пароксизмы предсердной экстрасистолии. Иллюстрация авторов
Обсуждение
Результаты работ, изучающих взаимосвязь высокой ВГ и развития ССП, в том числе ДКАН, крайне противоречивы. При проведении анализа данных Исследования по контролю и осложнениям диабета (Diabetes Control and Complications Trial, DCCT) J.M. Lachin и соавт. не выявили очевидной корреляции между гликемической изменчивостью и развитием микрососудистых осложнений [15]. Это может быть обусловлено тем, что оценка показателей ВГ проводилась по 7-точечному профилю глюкозы капиллярной крови. В нашем исследовании расчет показателей ВГ осуществлялся на основании данных НМГ, что повышает достоверность полученных результатов.
Н.А. Черникова и соавт. продемонстрировали взаимосвязь между ССП и качеством гликемического контроля у пациентов с СД 2 типа [16]. В частности, были установлены четкие корреляции между развитием желудочковых нарушений ритма и увеличением времени в гипогликемическом диапазоне и снижением — в целевом с повышением ВГ (ростом индексов SD и MAG > 4 ммоль/л/ч), а также показано, что высокая ВГ провоцирует удлинение интервала QTc [16]. Связь параметров гликемического контроля и ССП у пациентов с СД 1 типа продемонстрирована и других работах [12, 17]. В ходе нашего исследования была определена следующая корреляционная связь между показателями ВГ и изменениями сердечного ритма у пациентов с СД 1 типа: при увеличении ВГ (повышении индексов LI, MAGE и MAG) снижался ЦИ ЧСС, увеличивалась частота наджелудочковых и желудочковых нарушений ритма.
Известно, что одним из расчетных показателей для оценки вегетативной иннервации сердца является ЦИ ЧСС. Так, снижение ЦИ менее 1,2 (то есть отсутствие уменьшения ЧСС ночью) наблюдается при состояниях, связанных с вегетативной денервацией сердца, и является неблагоприятным прогностическим признаком. Увеличение ЦИ больше 1,5 обусловлено повышенной восприимчивостью сердца к симпатической стимуляции. Для больных СД наиболее характерно понижение ЦИ в рамках ДКАН [18]. По полученным нами данным, снижение ЦИ ЧСС отмечалось у 30 (42%) пациентов, что свидетельствует об отсутствии физиологического уменьшения ЧСС в ночное время. Таким образом, у пациентов с СД 1 типа наблюдается преобладание симпатикотонии как следствия повреждения блуждающего нерва и нарушения иннервации сердца, что характерно для пациентов с ДКАН. Нарушение регуляции синусового узла может приводить к развитию тахикардии покоя — одного из начальных проявлений кардиальной автономной нейропатии. Снижение ЦИ также сопряжено с высоким риском внезапной сердечной смерти. Увеличение ЦИ ЧСС нами зарегистрировано у 8 (11%) пациентов. При этом наблюдалась тахикардия днем на фоне сохранения физиологической ночной брадикардии. Появление дневной тахикардии может быть связано с физической активностью, а также стрессовыми ситуациями в течение дня, что требует дальнейшего углубленного исследования.
Для диагностики электрической нестабильности миокарда был проанализирован интервал QT, и у 14 (19%) пациентов зарегистрировано его удлинение, что является одним из признаков автономной нейропатии, а также независимым предиктором риска возникновения фатальных нарушений ритма и внезапной сердечной смерти.
Проведенный нами корреляционный анализ показал снижение ЦИ ЧСС при увеличении ВГ, что может отражать развитие автономной дисфункции. При росте лабильности гликемии (индекса LI) и скорости ее изменения (индекса MAG) у обследованных пациентов увеличивалась частота как наджелудочковых, так и желудочковых экстрасистол (при увеличении индексов MAG, MAGE, LI).
Заключение
Выявленные изменения ритма сердца на фоне увеличения ВГ у пациентов с СД 1 типа указывают на высокий риск формирования сердечно-сосудистой патологии. Строгий гликемический контроль и нормализация ВГ позволят не только замедлить формирование ДКАН, но и снизить риск возникновения желудочковых нарушений ритма сердца вне зависимости от предшествующего наличия ДКАН у пациентов с СД 1 типа.
[1]IDF Diabetes Atlas 2021. 10th edition. URL: https://diabetesatlas.org/atlas/tenth-edition (дата обращения: 16.05.2023)
Предыдущая статья
С.Н. Лагутина, А.А. Пашкова, И.С. Добрынина, Е.Ю. Есина, В.И. Шевцова, А.Н. Шевцов ФГБОУ ВО «Воро...