Значение прямого определения пикового инспираторного потока для выбора оптимального ингалятора у пациентов с бронхиальной астмой
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Салухов В.В., Харитонов М.А., Асямов К.В., Куренкова И.Г. и др. Ингаляционные средства доставки лекарственных препаратов в современной пульмонологии. Вестник Российской военно-медицинской академии. 2017;2(58):193–200. Salukhov V.V., Kharitonov M.A., Asyamov K.V., Kurenkova I.G. et al. Inhalation drug delivery devices in pulmonology. Bulletin of the Russian Military Medical Academy. 2017;2(58):193–200. (in Russian)
- Mahler D.A., Niu X., Deering K.L., Dembek C. Prospective evaluation of exacerbations associated with suboptimal peak inspiratory flow among stable outpatients with COPD. J. Chron. Obstruct. Pulmon. Dis. 2022;17:559–68. DOI: 10.2147/COPD.S353441
- Шарова Н.В., Черкашин Д.В., Соболев А.Д., Соловьев И.А. Определение пикового инспираторного потока для выбора оптимального ингалятора у пациентов c хронической обструктивной болезнью легких вне обострения. Биотехносфера. 2022;1(67):28–33. Sharova N.V., Cherkashin D.V., Sobolev A.D., Solov'ev I.A. Determination of peak inspirate flow for selection of the optimal inhalator in patients with chronic obstructive pulmonary disease non-exanction. Biotechnosfera. 2022;1(67):28–33. (in Russian). DOI: 10.25960/bts.2022.1.28
- Troy M., Van Vleet J., Tashkin D., Barjaktarevic I. Recent advances predict a bright future for nebulizers. Curr. Opin. Pulm. Med. 2023;29(2):123–32. DOI: 10.1097/MCP.0000000000000941
- Buttini , Brambilla G., Copelli D., Sisti V. et al. Effect of flow rate on in vitro aerodynamic performance of NEXThaler® in comparison with Diskus® and Turbohaler® dry powder inhalers. J. Aerosol. Med. Pulm. Drug Deliv. 2016;29(2):167–78. DOI: 10.1089/jamp.2015.1220
- Архипов В.В. Новые возможности выбора ингаляционного устройства для пациентов с бронхиальной астмой и хронической обструктивной болезнью легких. Русский медицинский журнал. 2020;9:46–50. Arkhipov V.V. New options for choosing an inhalation device for patients with asthma and chronic obstructive pulmonary disease. Russian Medical Journal. 2020;9:46–50. (in Russian)
- Романовских А.Г., Белоцерковская Ю.Г., Смирнов И.П. Выбор ингаляционного устройства у пациентов с бронхообструктивными заболеваниями. Consilium Medicum. 2020;22(3):55–60. Romanovskikh A.G., Belotserkovskaia Yu.G., Smirnov I.P. Inhalation device choice for patients with broncho-obstructive disorders. Consilium Medicum. 2020;22(3):55–60. (in Russian). DOI: 10.26442/20751753.2020.3.20010
2 ФГАОУ ВО Санкт-Петербургский государственный электротехнический университет «ЛЭТИ» им. В.И. Ульянова (Ленина); Россия, г. Санкт-Петербург
Цель исследования. Определить с помощью прибора In-Check DIAL G16 значения пикового инспираторного потока (ПИП) при бронхиальной астме (БА) для оценки соответствия применяемого ингалятора возможностям пациента и выбора оптимального ингалятора.
Дизайн. Одномоментное поперечное когортное исследование.
Материалы и методы. Обследованы 60 пациентов с БА: 16 человек с полным и 22 с частичным контролем заболевания, 22 человека с обострением БА. Контрольную группу составили 29 здоровых людей. Среди больных БА преобладали женщины пожилого возраста. У пациентов диагностированы различные фенотипы БА: легкая форма — у 7, среднетяжелая — у 34, тяжелая — у 19 человек. У 16 больных из 22 отмечалась тяжелая степень обострения заболевания. Определение ПИП проводилось с помощью прибора In-Check DIAL G16.
Результаты. Ограничение ПИП выявлено при полном контроле БА в 6,25–56,2%, при частичном контроле — в 9,1–59,1%, при обострении заболевания — в 9,1–86,4% случаев в зависимости от уровня сопротивления прибора.
Заключение. Ингаляционная терапия БА может быть персонализирована на основе прямого измерения ПИП с помощью приборов типа In-Check DIAL G16, что позволит лечащим врачам осуществлять выбор ингалятора в различные периоды БА с учетом степени контроля, периода заболевания, тяжести бронхиальной обструкции и индивидуальных особенностей пациента. С целью оптимизации ингаляционной терапии БА показана смена порошкового ингалятора с высоким сопротивлением прибора (R3–R5) на ингалятор с низким сопротивлением (R0 — дозированный аэрозольный ингалятор, респимат, ПИ -R1 — бризхалер), при обострении заболевания — использование небулайзера.
Ключевые слова: бронхиальная астма, ингалятор, пиковый инспираторный поток, спирометрия
Скачать PDFШарова Н.В., Черкашин Д.В., Соболев А.Д., Юлдашев З.М., Богданов Д.С. Значение прямого определения пикового инспираторного потока для выбора оптимального ингалятора у пациентов с бронхиальной астмой. Вестник терапевта. 2023. № 5-6 (60-61). DOI: 10.31550/2712-8601-VT-2023-5-6-3. URL: https://journaltherapy.ru/statyi/znachenie-pryamogo-opredeleniya-pikovogo-inspiratornogo-potoka-dlya... (дата обращения: дд.мм.гггг)
Шарова Наталья Викторовна — доцент кафедры и клиники военно-морской терапии Военно-медицинской академии им. С.М. Кирова, к. м. н., доцент. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. https://orcid.org/0000-0002-0120-0632. E-mail: natali.sharowa2014@yandex.ru
Черкашин Дмитрий Викторович — д. м. н., профессор, начальник кафедры и клиники военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. https://orcid.org/0000-0003-1363-6860. E-mail: cherkashin_dmitr@mail.ru
Соболев Алексей Дмитриевич (автор для переписки) — преподаватель кафедры и клиники военно-морской терапии Военно-медицинской академии им. С.М. Кирова. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. https://orcid.org/0000-0003-1908-7954. E-mail: sobolevvmeda@rambler.ru
Юлдашев Зафар Мухамедович — д. тех. н., профессор кафедры «Биотехнические системы», заведующий кафедрой «Биотехнические системы» СПбГЭТУ «ЛЭТИ», 197376, Россия, г. Санкт-Петербург, ул. Профессора Попова, д. 5, литера Ф. E-mail: yuld@mail.ru
Богданов Дмитрий Сергеевич — адъюнкт при кафедре и клинике военно-морской терапии Военно-медицинской академии имени С.М. Кирова. 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6. E-mail: dimbog91@mail.ru
The value of direct determination of peak inspiratory flow for choosing the optimal inhaler in patients with bronchial asthma
N.V. Sharova1, D.V. Cherkashin1, A.D. Sobolev1, Z.M. Yuldashev2, D.S Bogdanov1
1 S.M. Kirov Military Medical Academy; 6 Academician Lebedev Str., St. Petersburg, Russian Federation 194044
2 Saint Petersburg Electrotechnical University “LETI”; 5 Professor Popov Str., litera F, Saint Petersburg, Russian Federation 197376
Aim. Purpose of the study. Using the In-Check DIAL G16 device, determine the values of peak inspiratory flow (PIF) in bronchial asthma (BA) to assess the suitability of the inhaler used to the patient's capabilities and select the optimal inhaler.
Design. Cross-sectional cohort study.
Materials and methods. 60 patients with asthma were examined: 16 people with complete and 22 with partial control of the disease, 22 people with exacerbation of asthma. The control group consisted of 29 healthy people. Among patients with asthma, elderly women predominated. The patients were diagnosed with various asthma phenotypes: mild — in 7, moderate — in 34, severe — in 19 people. 16 out of 22 patients had a severe exacerbation of the disease. The determination of PIP is carried out using the In-Check DIAL G16 device.
Results. Limitation of PIP was detected with complete control of asthma in 6.25–56.2%, with partial control — in 9.1–59.1%, with exacerbation of the disease — in 9.1–86.4% of cases, depending on the level of resistance of the device.
Conclusion. Inhalation therapy for asthma can be personalized based on direct measurement of PIP using devices such as In-Check DIAL G16, which will allow treating physicians to select an inhaler in different periods of asthma, taking into account the degree of control, the period of the disease, the severity of bronchial obstruction and the individual characteristics of the patient. In order to optimize inhalation therapy for asthma, it is recommended to replace a powder inhaler with a high resistance device (R3–R5) with an inhaler with a low resistance (R0 — metered dose aerosol inhaler, respimat, R1 — breathhaler), and in case of exacerbation of the disease — use of a nebulizer.In order to optimize inhalation therapy for asthma, it is recommended to change the PI with a high resistance device (R3–R5) to an inhaler with a low resistance (R0 — MDI, respimat, R1 — breezhaler), and in case of exacerbation of the disease, use a nebulizer.
Keywords: peak inspiratory flow, spirometry, bronchial asthma, inhaler.
Н.В. Шарова1, Д.В. Черкашин1, А.Д. Соболев*1, З.М. Юлдашев2, Д.С. Богданов1
1 ФГБВОУ ВО «Военно-медицинская академия имени С.М. Кирова» Министерства обороны Российской Федерации; Россия, г. Санкт-Петербург
2 ФГАОУ ВО Санкт-Петербургский государственный электротехнический университет «ЛЭТИ» им. В.И. Ульянова (Ленина); Россия, г. Санкт-Петербург
Бронхиальная астма (БА) — распространенное заболевание, которое требует постоянного контроля, лечения и предупреждения развития обострений. Доказана важная роль ингаляционной терапии на всех этапах лечения заболевания[1]. Однако некоторые положения фармакотерапии требуют уточнения. Остаются неясными критерии выбора оптимального ингалятора при различной тяжести БА и степени ее контроля.
Используемая ингаляционная техника подразделяется на ингаляторы под давлением (дозированные аэрозольные ингаляторы (ДАИ) и жидкостный ингалятор респимат), порошковые ингаляторы (ПИ) и небулайзеры. Широкое распространение получили ПИ. ПИ являются средством доставки большинства фармакологических препаратов, не требуют синхронизации начала вдоха и активации, как при ДАИ, что обеспечивает возможность полноценной ингаляции лекарств у больных БА пожилого возраста [1]. Оптимальная доза лекарственного препарата при применении конкретного ПИ зависит от создаваемого пациентом пикового инспираторного потока (ПИП).
Неспособность больного сделать необходимое инспираторное усилие, соответствующее требованиям ПИ, приводит к недостаточному депонированию и действию препарата в бронхах, что проявляется снижением эффективности ингаляционной терапии, ухудшением контроля БА, повышением риска обострений и повторных госпитализаций [2]. ПИП можно определить с помощью прибора In-Check DIAL G16. Исследование ПИП в РФ проводится редко из-за отсутствия отечественной аппаратуры для его измерения.
Цель исследования: определить с помощью прибора In-Check DIAL G16 значения ПИП при БА для оценки соответствия применяемого ингалятора возможностям пациента и выбора оптимального ингалятора.
Материалы и методы
Работа выполнена на базе кафедры и клиники военно-морской терапии Военно-медицинской академии имени С.М. Кирова Минобороны РФ с января 2019 по декабрь 2021 года. Все участники подписали информированное согласие на участие в исследовании. Исследование одобрено локальным этическим комитетом. Всего обследованы 60 пациентов с БА: 16 человек с полным и 22 с частичным контролем заболевания, 22 человека с обострением БА. Контрольную группу составили 29 здоровых людей.
Среди больных БА преобладали женщины пожилого возраста. Участники всех групп существенно не различались по росту, массе, индексу массы тела. У пациентов диагностированы различные фенотипы БА: легкая форма — у 7, среднетяжелая — у 34, тяжелая — у 19 человек. У 16 больных из 22 отмечалась тяжелая степень обострения заболевания.
Коморбидная патология сердечно-сосудистой системы выявлена у 50% пациентов с контролируемой БА и практически у всех больных с обострением заболевания (постинфарктный кардиосклероз, пароксизмальная фибрилляция предсердий, хроническая сердечная недостаточность).
Спирометрия выполнялась на спирографе Flowscreen II фирмы Jaeger и Прессотахоспирографе-ПТС-14П-01 (РФ) с записью кривой «поток — объем» и расчетом следующих показателей: жизненная емкость легких (ЖЕЛ), ЖЕЛ вдоха, форсированная ЖЕЛ (ФЖЕЛ), объем форсированного .ыдоха за первую секунду (ОФВ1), ОФВ1/ФЖЕЛ%, пиковая объемная скорость выдоха, средняя объемная скорость выдоха на 25–75% ФЖЕЛ, пиковая скорость вдоха.
Для определения ПИП применялся портативный прибор In-Check DIAL G16 фирмы Clement Clarke International Limited (Великобритания). Использование прибора возможно у пациентов с БА любой степени тяжести, в амбулаторных и стационарных условиях, он позволяет мониторировать ПИП в процессе лечения. ПИП оценивался на вдохе при имитации сопротивления, выбранного на шкале ингалятора. Панель прибора учитывала ДАИ и респимат (R0, без сопротивления) и пять уровней сопротивления ПИ, каждый из которых соответствовал определенному типу ингалятора: R1 — низкое сопротивление (бризхалер, аэролайзер), R2 — средне-низкое (эллипта), R3 — среднее (спиромакс, турбухалер), R4 — средне-высокое (некстхалер), R5 — высокое (хандихалер). Прибор позволяет изучать ПИП в диапазоне измерений 15–120 л/мин (± 10 л/мин).
Статистическая обработка данных осуществлялась с помощью пакета прикладных программ Statistica 10. Различия между группами оценивались для непрерывных показателей с помощью критерия Манна — Уитни, для дискретных — с помощью точного критерия Фишера. Для оценки динамики использовался критерий Вилкоксона. Статистические характеристики групп для непрерывных показателей описывались с помощью медианы и квартилей. Различия с учетом принципа Бонферрони считались статистически значимыми при р < 0,005.
Результаты и обсуждение
При использовании ПИ диспергирование лекарственного порошка осуществляется за счет форсированного вдоха пациента. ПИП — это максимальный инспираторный поток, создаваемый пациентом во время инспираторного маневра. Оптимальными значениями ПИП считались при R0 ˃ 90 л/мин, R1–R4 ˃ 60 л/мин, R5 ˃ 30 л/мин [2]. Меньшие значения расценивались как субоптимальные (сПИП). При сПИП снижалась клиническая эффективность лекарственной ингаляции. Следует отметить, что выделение пациентов с сПИП (%) для оценки степени ограничения инспираторного усилия более целесообразно, чем ориентация только на значения ПИП.
Перед началом исследования пациенты изучали инструкцию по использованию каждого типа ингалятора и были проинформированы о том, что при применении ПИ после глубокого выдоха следует сделать максимально глубокий и мощный вдох. Выполнение этого условия позволяет избегать самой распространенной ошибки при использовании ПИ — недостаточно глубокого выдоха перед ингаляцией лекарства.
Пациенты в случайном порядке делали по два вдоха через In-Check DIAL при различных показателях сопротивления прибора, соответствующих определенному типу ингалятора.
При обследовании группы здоровых людей показатели ПИП были оптимальными при всех уровнях сопротивления прибора, то есть при использовании всех вариантов ингаляторов. Абсолютные значения ПИП колебались от 120 [120–120] л/мин при R0 до 70 [65–80] л/мин [3]. Полученные результаты согласуются с зарубежными данными [2].
БА — хроническое бронхообструктивное заболевание с характерной вариативной бронхиальной обструкцией, что находит отражение в различной способности пациентов с БА сделать максимальное инспираторное усилие в зависимости от степени контроля и периода обострения заболевания. Обследование больных БА проводилось при полном и частичном контроле над болезнью и в период ее обострения.
Как видно из данных таблицы, в группе БА с полным контролем показатели ПИП у всех больных, как у здоровых лиц, оставались оптимальными при использовании ДАИ и респимата при сохранных спирографических параметрах. Субоптимальные значения ПИП регистрировались у одного пациента на бризхалере (R1) и у двух на эллипте (R2). Эти участники не могли сделать необходимое инспираторное усилие для использования в качестве базисной терапии перечисленные ингаляторы. Они имели одышку по модифицированной шкале Medical Research Council 3-й степени, низкие ФЖЕЛ и ОФВ1, хроническую сердечную недостаточность 2-й стадии. Контроль БА у них достигнут на 3-й ступени БА, при адекватном лечении коморбидной патологии.
Количество больных БА с сПИП увеличилось при имитации пациентами сопротивления — R3 (25%), R4 (56,25%) и R5 (25%), что означало, что этим пациентам (при низких значениях ОФВ1, коморбидной патологией, ХСН), при назначении турбухалера, некстхалера и хандихалера целесообразно прямо оценивать значения ПИП для выбора оптимального ингалятора.
Таблица. Показатели пикового инспираторного потока (ПИП) (МЕ [25%; 75%]) и субоптимального ПИП (сПИП) при имитации различных сопротивлений ингаляторов у пациентов с бронхиальной астмой (БА) при поступлении в клинику в группах с полным или частичным контролем БА, с обострением БА и в контрольной группе
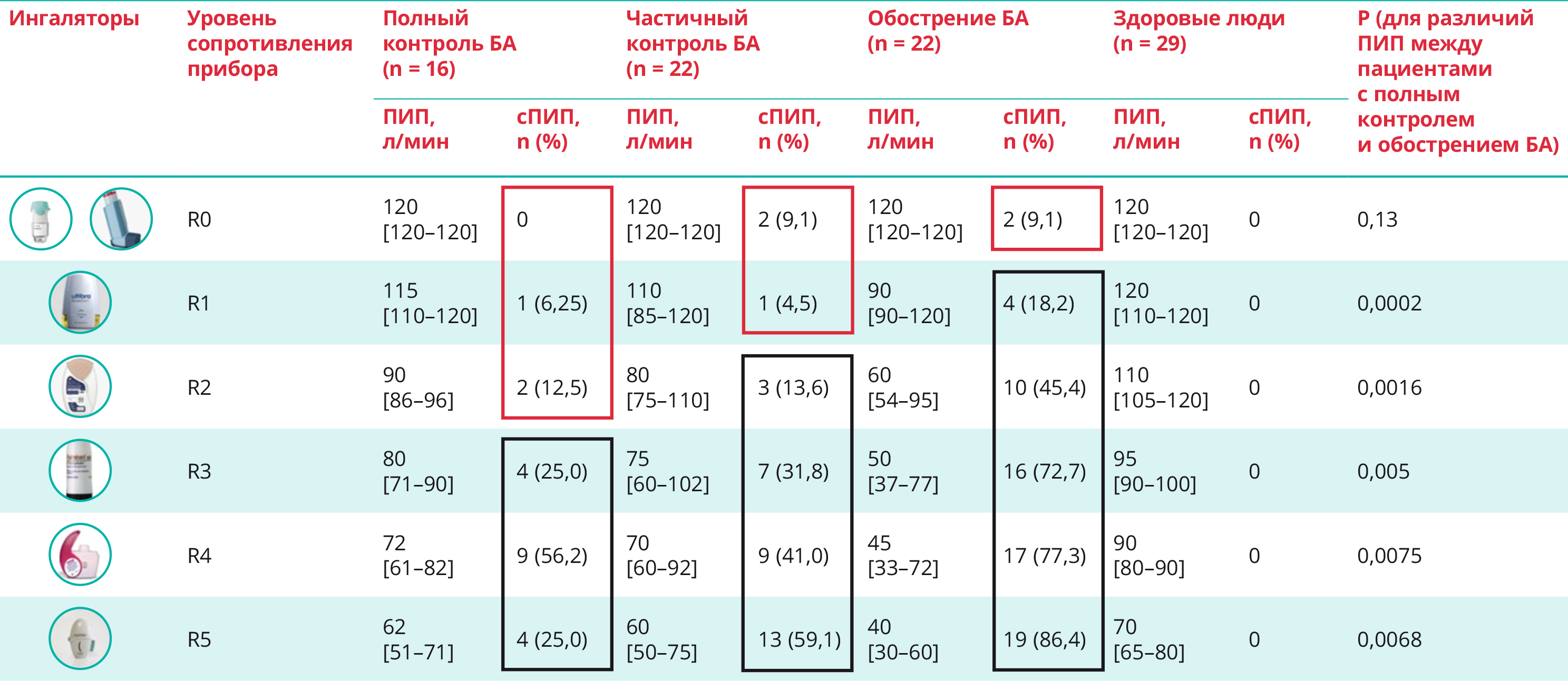
Примечание. Красным цветом выделены незначимые значения субоптимального пикового инспираторного потока, черным цветом — значимые значения.
Note. Insignificant suboptimal peak inspiratory flow values are highlighted in red, significant suboptimal peak inspiratory flow values are highlighted in black.
Больные с частичной утратой контроля БА отличались от пациентов с полным контролем признаками обструкции (ОФВ1 — 75% [50%; 84%] против 90,5% [75%; 94%], p < 0,005) при индексе Генслара 68% [53,5%; 75%] против 74,5% [71,5%; 80,3%], появлением пациентов с сПИП уже при использовании ингаляторов без сопротивления. Количество больных с сПИП при R2 — 3 (13,6%), при R3 — 7 (31,8%), при R4 — 8 (41%), при R5 — 59,1%. Больные БА в этот период заболевания, применявшие в качестве средства базисной терапии формотерол/будесонид турбухалер 4,5/160 мкг 1 раз в сутки, самостоятельно увеличивали дозу и кратность приема препарата для улучшения состояния (SMART-терапия).
В клинике хорошо известен факт возрастания потребности в препарате формотерол/будесонид по мере нарастании бронхиальной обструкции. Возможно, одна из причин этого — возникающее ограничение ПИП. ПИП измеряется во время стандартного исследования функции легких без сопротивления прибора и в литературе обычно обозначается как пиковая скорость вдоха.
Данные рутинной спирометрии, проведенной на аппарате Прессотахоспирограф ПТС-14П-01, показали, что при стандартном бронходилатационном тесте с 400 мкг сальбутамола у пациентов с полным или частичным контролем заболевания (n = 24) отмечен прирост ОФВ1 на 0,55 ± 0,31 л, что сопровождалось приростом пиковой скорости вдоха на 0,40 ± 0,20 л. Экстраполируя эти данные на β2-агонист формотерол с быстрым началом действия, можно объяснить эффективность ингаляционной терапии формотеролом/будесонидом при увеличении дозы и кратности приема препарата с ингалятором турбухалер у пациентов как с полным, так и с частичным контролем БА, так как больные часто переоценивают уровень своего контроля БА.
Больные с обострением БА характеризовались нарастанием частоты и тяжести приступов удушья, низкими функциональными значениями ОФВ1 (36% [28,7%; 45%] при индексе Генслара 56,5% [49,5%; 70%], появлением признаков десатурации, увеличением потребности в короткодействующих β2-агонистах (КДБА) и необходимостью использовать большие дозы ингаляционных глюкокортикостероидов и КДБА с помощью небулайзерной техники в домашних условиях. Всем пациентам была назначена интенсивная терапия, включавшая небулайзерное введение будесонида 1000–2000 мкг и ипратропия бромида/фенотерола 1–2 мл, внутривенное введение преднизолона (180–360 мг/с) и аминофиллина (20 мл/с), оксигенотерапию.
При обострении БА выявлено снижение абсолютных значений ПИП при применении ПИ и значимо бóльшая доля (%) больных сПИП, чем в группах полного и частичного контроля БА и в группе здоровых людей.
Наименьшее количество больных с сПИП отмечено при использовании ингаляторов с нулевым сопротивлением — 9,1%. Это позволяет считать оправданным при обострении болезни предпочтительное применение у всех пациентов небулайзера с принудительной подачей лекарства в дыхательные пути, ДАИ со спейсером или респимата (R0) без предварительного определения ПИП [4].
При имитации сопротивления ингалятора бризхалер (R1) доля пациентов с сПИП увеличилась всего до 18,2%. Этот факт подтверждает, что именно бризхалер может адекватно использоваться как средство доставки современной тройной фиксированной комбинации препаратов (длительно действующий β2-агонист/длительно действующий антихолинергический препарат/ингаляционный глюкокортикостероид) в качестве базисной терапии БА и при ее обострении.
Количество пациентов с обострением с сПИП при применении эллипты — 45%, турбухалера — 72,7%, хандихалера — 86,4%. Это означает, что большинство больных были неспособны сделать достаточное инспираторное усилие при использовании перечисленных ингаляторов для оптимальной ингаляции лекарственных препаратов.
По мнению многих зарубежных авторов, высокая зависимость доставляемой дозы от скорости вдоха ниже 60 л/мин является свойством, за которое подвергается критике ингалятор турбухалер (R3). Только 72, 7% больных с обострением БА смогли произвести ПИП > 60 л/мин с помощью турбухалера. Доказано, что ингаляции препаратов со слишком низким ПИП (< 30 л/мин) не могли купировать бронхоспазм у пациентов во время приступа астмы [5].
Таким образом, при обострении БА требуется временная смена ингалятора со средним и высоким сопротивлением прибора на ингалятор с низким или нулевым сопротивлением для оптимизации ингаляционной терапии.
Целесообразно рассмотреть возможность использования других типов ингаляторов при сохранении той же молекулы препарата — формотерол/будесонид. В настоящее время в распоряжении клинициста имеются несколько ингаляторов, отвечающих данному требованию. Препарат формотерол/будесонид представлен в формах аэролайзера, спиромакса, турбухалера, респифорба комби. Возможность замены турбухалера на ДАИ (рапихалера со спейсером) при обострении БА изучена в работах профессора В.В. Архипова [6], А.Г. Романовских и соавт. [7]. Авторы считают, что применение формотерола/будесонида рапихалера показано больным БА в возрасте 6–11 лет, пожилым пациентам, при сочетании БА и ХОБЛ, предпочитающим использовать ДАИ в силу наличия интуитивной обратной связи (звук, ощущение ингаляции).
Заключение
Перед выбором ингаляционной системы у пациентов с БА, особенно пожилого возраста, важно убедиться, что создаваемый ими инспираторный поток достаточен для обеспечения оптимального введения лекарственного средства.
Мы выявили сПИП при использовании ПИ в таком количестве случаев: 1) при полном контроле БА от 6,25% на бризхалере до 56,2 на некстхалере, 2) при частичном контроле — в 9,1 на бризхалере до 59,1% на хандихалере, 3) при обострении заболевания — в 18,2 на бризхалере – 86,4% на хандихалере в зависимости от уровня сопротивления прибора, что означает несоответствие применяемого ингалятора возможностям пациента.
Ингаляционная терапия БА может быть персонализирована на основе прямого измерения ПИП с помощью приборов типа In-Check DIAL G16, что позволит лечащим врачам осуществлять выбор ингалятора в различные периоды БА с учетом степени контроля, периода заболевания, тяжести бронхиальной обструкции и индивидуальных особенностей пациента.
С целью оптимизации ингаляционной терапии БА при ограничении ПИП и отсутствии возможности его прямого измерения показана смена ПИ с высоким сопротивлением прибора (R3–R5) на ингалятор с низким сопротивлением (R0 — ДАИ, респимат, R1 — бризхалер, рапихалер с применением спейсера), а при обострении заболевания — преимуществееное использование небулайзерной техники, применение которой не зависит от инспираторного усилия пациента.
[1] Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. 2020. Report. URL: https://goldcopd.org/ (дата обращения — 15.11.2023).
Предыдущая статья
Г.С. Акимочкин, С.Е. Матохин, В.В. Скворцов*, Е.М. Скворцова, С.С. Сараев ФГБОУ ВО «Волгоградский...
Следующая статья
Д.Р. Акберова*, Е.С. Бодрягина, К.И. Мидхатова, А.А. Камартдинова ФГБОУ ВО «Казанский государстве...