Комплексный подход к терапии ожирения у детей подросткового возраста
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- На первом занятии проводится сбор анамнеза с помощью анкетирования пациента с ожирением. На основании полученных данных врач делает заключение об особенностях пищевого поведения ребенка (кратности и времени приемов пищи, качестве и количестве потребляемых продуктов, наличии перекусов, употреблении сладких напитков и др.), физической активности (наличии/отсутствии, виде, регулярности, длительности), режиме дня. Проводится анализ протокола биоимпедансометрии пациента, рассчитывается объем необходимой ежедневной водной нагрузки (с учетом исходного веса), сроки достижения желаемой массы тела. Оценивается психологическое состояние ребенка на момент обращения. В конце занятия пациенту объясняются правила ведения пищевого дневника с обязательным взвешиванием порции, определяется объем и кратность выполнения домашних обязанностей для повышения активности в течение дня.
- Второй и третий семинары посвящены вопросам рационального питания. По окончании данного блока занятий проводится анализ пищевого дневника, коррекция рациона и режима питания, обсуждаются правила изменения пищевого поведения как самого пациента, так и его семьи.
- На четвертом семинаре обсуждается необходимость физической активности для снижения массы тела и постоянного контроля терапии. Анализируются причины возможных неудач в лечении, трудностей в применении усвоенных правил.
- Пятое занятие подводит итоги проведенного обучения. Оценивается степень усвоения знаний с использованием контрольно-обучающей программы «Магазин умной еды», созданной с помощью программы PowerPoint Presentation операционной системы Windows 7 и представляющей собой интерактивный продуктовый магазин, который состоит из семи разных отделов (молочного, сырного, овощного, фруктового, хлебобулочного, рыбного, бакалейного). Пациент должен выбрать подходящие ему продукты, используя функцию гиперссылки. В случае совершения ошибки, программа дает пояснительную информацию и предоставляет возможность вернуться к заданию, чтобы выбрать иной вариант ответа (иной продукт). Правильный выбор обозначается звуковым или анимационным поощрением. Переход к каждому последующему этапу программы (отделу магазина) возможен только после того, как пациент верно соберет весь набор продуктов.
- Литература
- Тимашева Я.Р., Балхиярова Ж.Р., Кочетова О.В. Современное состояние исследований в области ожирения: генетические аспекты, роль микробиома и предрасположенность к COVID-19. Проблемы Эндокринологии. 2021;67(4):20–35. Timasheva Y.R., Balkhiyarova Z.R., Kochetova O.V. Current state of the obesity research: genetic aspects, the role of microbiome, and susceptibility to COVID-19. Problems of Endocrinology. 2021;67(4):20–35. (in Russian). DOI: 10.14341/probl12775
- Петеркова В.А., Безлепкина О.Б., Болотова Н.В., Богова Е.А. и др. Клинические рекомендации «Ожирение у детей». Проблемы Эндокринологии. 2021;67(5):67–83. Peterkova V.A., Bezlepkina O.B., Bolotova N.V., Bogova E.A. et al. Clinical guidelines "Obesity in children". Problems of Endocrinology. 2021;67(5):67–83. (in Russian). DOI: 14341/probl12802
- Райгородская Н.Ю., Филина Н.Ю. Вегетативные расстройства при гипоталамическом синдроме у подростков: клинические проявления и возможности транскраниальной магнитотерапии. В сб.: Куликов А.Г., Болотова Н.В., Райгородский Ю.М., ред. Транскраниальная физиотерапия (Магнитотерапия и ее сочетание с электростимуляцией). Саратов: Изд. Сар. Мед. ун-та; 2013: 50–6. Raygorodskaya N.Yu., Filina N.Yu. Autonomic disorders in hypothalamic syndrome in adolescents: clinical manifestations and possibilities of transcranial magnetotherapy. In: A.G. Kulikov, Bolotova N.V., Raygorodsky Yu.M., eds. Transcranial physiotherapy (Magnetotherapy and its combination with electrical stimulation). Saratov: Ed. Sar. Med. University; 2013: 50–6. (in Russian)
- Аверьянов А.П., Болотова Н.В., Зотова Ю.А., Райгородская Н.Ю. и др. Новые технологии в комплексном лечении осложненных форм ожирения у детей. В сб.: Куликов А.Г., Болотова Н.В., Райгородский Ю.М., ред. Транскраниальная физиотерапия (Магнитотерапия и ее сочетание с электростимуляцией). Саратов: Изд. Сар. Мед. ун-та; 2013: 57–67. Averyanov A.P., Bolotova N.V., Zotova Yu.A., Raigorodskaya N.Yu. et al. New technologies in the complex treatment of complicated forms of obesity in children. In: A.G. Kulikov, Bolotova N.V., Raygorodsky Yu.M., eds. Transcranial physiotherapy (Magnetotherapy and its combination with electrical stimulation). Saratov: Ed. Sar. Med. University; 2013: 57–67 (in Russian)
- Зотова Ю.А., Воскресенская О.В., Болотова Н.В., Григорьева Е.А. и др. Немедикаментозное лечение головной боли у детей с различными формами ожирения. Транскраниальная физиотерапия (Магнитотерапия и ее сочетание с электростимуляцией). В сб.: Куликов А.Г., Болотова Н.В., Райгородский Ю.М., ред. Транскраниальная физиотерапия (Магнитотерапия и ее сочетание с электростимуляцией). Саратов: Изд. Сар. Мед. ун-та; 2013: 73–82. Zotova Yu.A., Voskresenskaya O.V., Bolotova N.V., Grigorieva E.A. et al. Non-drug treatment of headache in children with various forms of obesity. In: A.G. Kulikov, Bolotova N.V., Raygorodsky Yu.M., eds. Transcranial physiotherapy (Magnetotherapy and its combination with electrical stimulation). Saratov: Ed. Sar. Med. University; 2013: 73–82 (in Russian)
- Болотова Н.В., Аверьянов А.П., Дронова Е.Г., Райгородский Ю.М. и др. Немедикаментозная коррекция нейроэндокринных нарушений у девочек пубертатного возраста с ожирением. В сб.: Куликов А.Г., Болотова Н.В., Райгородский Ю.М., ред. Транскраниальная физиотерапия (Магнитотерапия и ее сочетание с электростимуляцией). Саратов: Изд. Сар. Мед. ун-та; 2013: 90–8. Bolotova N.V., Averyanov A.P., Dronova E.G., Raigorodsky Yu.M. et al. Non-drug correction of neuroendocrine disorders in obese pubertal girlsIn: A.G. Kulikov, Bolotova N.V., Raygorodsky Yu.M., eds. Transcranial physiotherapy (Magnetotherapy and its combination with electrical stimulation). Saratov: Ed. Sar. Med. University; 2013: 90–8. (in Russian)
- Bolotova N.V., Filina Yu.N., Kurdiyan M.S., Kompaniets O.V. et al. Using transcranial magnetic therapy in combination with electrostimulation for correcting neuroendocrine-immune disorders in obese boys. Russian Open Medical Journal. 2022; 11(1):e0111. DOI: 10.15275/rusomj.2022.0111
- Srivastava G., Fox C.K., Kelly A.S., Jastreboff M. et al. Clinical considerations regarding the use of obesity pharmacotherapy in adolescents with obesity. Obesity (Silver Spring). 2019;27(2):190–204. DOI: 10.1002/oby.22385
- Анциферов М.Б., Маркова Т.Н. Современные возможности медикаментозного лечения ожирения. Доктор.Ру. 2021;20(2):45–50. Antsiferov M.B., Markova T.N. State-of-the-art drug therapies of obesity. Doctor.Ru. 2021;20(2):45–50. (in Russian). DOI: 10.31550/1727-2378-2021-20-2-45-50
- Матвеев Г.А., Голикова Т.И., Васильева А.А., Васильева Е.Ю. и др. Сравнение эффектов терапии ожирения лираглутидом и сибутрамином. Ожирение и метаболизм. 2021;18(2):218–28. Matveev G.A., Golikova T.I., Vasileva A.A., Vasilieva E.V. et al. Comparison of the effects of liraglutide and sibutramine in obese patients. Obesity and Metabolism. 2021;18(2):218– (in Russian). DOI: 10.14341/omet12498
- Логвинова О.В., Трошина Е.А. Влияние лираглутида 3,0 мг на характеристики пищевого поведения у пациентов с алиментарным ожирением. Медицинский совет. 2021; (7), 156–164. Logvinova O.V., Troshina E.A. Effect of liraglutide 3.0 mg on eating behavior in patients with obesity. Medical Council. 2021;(7):156– (in Russian). DOI: 10.21518/2079-701X-2021-7-156-164
- Логвинова О.В., Трошина Е.А. Прогнозирование раннего ответа на терапию агонистом рецепторов глюкагоноподобного пептида-1 лираглутидом у пациентов с экзогенно-конституциональным ожирением. Ожирение и метаболизм. 2020;17(1):3–12. Logvinova O.V., Troshina E.A. Prediction of early response to liraglutide therapy in patients with obesity. Obesity and Metabolism. 2020;17(1):3– DOI: 10.14341/omet12274
- Iqbal J., Wu H.X., Hu N., Zhou Y.H. et.al. Effect of glucagon-like peptide-1 receptor agonists on body weight in adults with obesity without diabetes mellitus — a systematic review and meta-analysis of randomized control trials. Obes. Rev. 2022;23(6):e13435. DOI: 1111/obr.13435
- Neeland I.J., Marso S.P., Ayers C.R., Lewis B. et al. Effects of liraglutide on visceral and ectopic fat in adults with overweight and obesity at high cardiovascular risk: a randomised, double-blind, placebo-controlled, clinical trial. Lancet. Diabetes Endocrinol. 2021;9(9):595–605. DOI: 10.1016/S2213-8587(21)00179-0
- Maselli D., Atieh J., Clark M.M., Eckert D. et al. Effects of liraglutide on gastrointestinal functions and weight in obesity: a randomized clinical and pharmacogenomic trial. Obesity (Silver Spring), 2022;30(8):1608–20. DOI: 10.1002/oby.23481
- Marshall W.A., Tanner J.M. Variations in the pattern of pubertal changes in boys. Arch. Dis. Child. 1970;45(239):13–23. DOI: 10.1136/adc.45.239.13
- O'Connor E.A., Evans C.V., Burda B.U., Walsh E.S. et al. Screening for obesity and intervention for weight management in children and adolescents: evidence report and systematic review for the US Preventive Services Task Force. JAMA. 2017;317(23):2427–44. DOI: 10.1001/jama.2017.0332
- Болотова Н.В., Райгородская Н.Ю., Аверьянов А.П., Дронова Е.Г. и др. Особенности нейроэндокринно-иммунного статуса мальчиков-подростков с ожирением. Вопросы детской диетологии. 2020;18(2):15–22. Bolotova N.V., Raigorodskaya N.Yu., Averyanov A.P., Dronova E.G. et al. Specificities of neuroendocrine-immune status in obese adolescent boys. Pediatric Nutrition. 2020;18(2):15–22. (in Russian). DOI: 10.20953/1727-5784-2020-2-15-22
- Kadouh H., Chedid V., Halawi H., Burton D.D. et al. GLP-1 analog modulates appetite, taste preference, gut hormones, and regional body fat stores in adults with obesity. J. Clin. Endocrinol. Metab. 2020;105(5):1552–63. DOI: 10.1210/clinem/dgz140
- Son J.W., Kim S. Comprehensive review of current and upcoming anti-obesity drugs. Diabetes Metab. J. 2020;44(6):802–18. DOI: 10.4093/dmj.2020.0258
- Barrera J.G., Sandoval D.A., D’Alessio D.A., Seeley R.J. GLP-1 and energy balance: an integrated model of short-term and long-term control. Nat. Rev. Endocrinol. 2011;7(9):507–16. DOI: 10.1038/nrendo.2011.77
- Матвеев Г.А., Голикова Т.И., Васильева А.А., Васильева Е.Ю. и др. Сравнение эффектов терапии ожирения лираглутидом и сибутрамином. Ожирение и метаболизм. 2021;18(2):218–28. Matveev G.A., Golikova T.I., Vasilyeva A.A., Vasilyeva E.Yu. et al. Comparison of the effects of obesity therapy with liraglutide and sibutramine. Obesity and Metabolism. 2021;18(2): 218–28. (in Russian). DOI: 10.14341/omet12498
- Бабенко А.Ю., Кононова Ю.А., Мартьянова М.В., Симаненкова А.В. и др. Терапия агонистами глюкагоноподобного пептида-1 у пациентов с сахарным диабетом и ожирением. Клиническая медицина, 2020;98(3):210–7. Babenko A.Yu., Kononova Yu.A., Martyanova M.V., Simanenkova A.V. et al. Glucagon-like peptide-1 agonists therapy in patients with diabetes mellitus and obesity. Clinical Medicine (Russian Journal). 2020;98(3):210–7. (in Russian). DOI: 10.30629/0023-2149-2020-98-3-210-217
- Model J.F.A., Lima M.V., Ohlweiler R., Lopes Vogt E. et al. Liraglutide improves lipid and carbohydrate metabolism of ovariectomized rats. Mol. Cell. Endocrinol. 2021;524:111158. DOI: 10.1016/j.mce.2021.111158
- Matikainen N., Söderlund S., Björnson E., Pietiläinen K. et al. Liraglutide treatment improves postprandial lipid metabolism and cardiometabolic risk factors in humans with adequately controlled type 2 diabetes: a single-centre randomized controlled study. Diabetes Obes. Metab. 2019;21(1):84–94. DOI: 10.1111/dom.13487
- Лерман О.В., Лукина Ю.В., Кутишенко Н.П., Марцевич С.Ю. Медикаментозное лечение ожирения: особенности врачебных назначений, информированность, приверженность и отношение больных к лекарственной терапии ожирения. Клиницист. 2019;13(1–2):27–33. Lerman O.V., Lukina Y.V., Kutishenko N.P., Martsevich S.Yu. Medical treatment of obesity: peculiarities of medical treatments, information, responsibility and relation to medical treatment of obesity of patients. The Clinician. 2019;13(1–2):27–33. (in Russian) DOI: 10.17650/1818-8338-2019-13-1-2-27-33
- Мартынова И.Н., Винярская И.В. Оптимизация лечебно-профилактической помощи детям с ожирением в условиях детской поликлиники. Российский педиатрический журнал. 2017;20(5):276–82. Martynova I.N., Vinyarskaya I.V. Development and evaluation of the effectiveness of the health school for children with obesity under the conditions of the child polyclinic. Russian Pediatric Journal, 2017;20(5):276–82. (in Russian)
- Шарафетдинов Х.Х., Дербенева С.А., Зайнудинов З.М., Завистяева Т.Ю. и др. Диетотерапевтическая программа по снижению массы тела и оценка ее эффективности у лиц с избыточной массой тела и ожирением. Вопросы питания. 2021;90(3):84–92. Sharafetdinov Kh.Kh., Derbeneva S.A., Zainudinov Z.M., Zavistyaeva T.Yu., et al. Diet therapy program for weight loss and essessment of its effectiveness in overweight and obese person. Problems of Nutrition. 2021;90(3):84–92. (in Russian). DOI: 10.33029/0042-8833-2021-90-3-84-92
- Статова А.В. Факторы риска развития и оптимизация лечения ожирения у детей Краснодарского края: дис. … канд. мед наук: Ставрополь; 2018. 169 c. Statova A.V. Risk factors for the development and optimization of the treatment of obesity in children of the Krasnodar Territory: ... candidate of medical sciences: Stavropol, 2018. 169 p. (in Russian)
- Perdew M., Liu S., Rhodes R., Ball G.D.C. et al. The effectiveness of a blended in-person and online family-based childhood obesity management program. Child. Obes. 2021;17(1):58–67. DOI: 10.1089/chi.2020.0236
- Augustijn M.J.C.M., Di Biase M.A, Zalesky A, Van Acker L. et al. Structural connectivity and weight loss in children with obesity: a study of the "connectobese". Int. J. Obes. (Lond.). 2019;43(11):2309–21. DOI: 10.1038/s41366-019-0380-6
- Владимирова Ю.В. Особенности ведения детей с экзогенно-конституциональным ожирением на фоне лептиновой резистентности: дис. канд. мед наук: Самара; 2020. 145 с. Vladimirova Yu.V. Features of the management of children with exogenous constitutional obesity against the background of leptin resistance: ... candidate of medical sciences. Samara; 2020. 145 p. (in Russian)
- Mastrandrea L.D., Witten L., Carlsson Petri K.C., Hale P.M. et al. Liraglutide effects in a paediatric (7–11 y) population with obesity: a randomized, doubleblind, placebo-controlled, short-term trial to assess safety, tolerability, pharmacokinetics, and pharmacodynamics. Pediatr. Obes. 2019;14(5):e12495. DOI: 10.1111/ijpo.12495
- Kelly A.S., Auerbach P., Barrientos-Perez M., Gies I. et al. A randomized, controlled trial of liraglutide for adolescents with obesity. N. Engl. J. Med. 2020;382(22):2117–28. DOI: 10.1056/NEJMoa1916038
Цель исследования: оценить эффективность различных методов терапии ожирения у детей подросткового возраста.
Дизайн исследования: проспективное одноцентровое рандомизированное клиническое исследование.
Материалы и методы. В исследование включены 64 ребенка 12–17 лет с экзогенно-конституциональным ожирением 2–3-й степени. Контрольную группу составили 29 детей того же возраста с нормальной массой тела, не имеющие сопутствующей хронической патологии. В основной группе методом случайной выборки выделены три подгруппы: 1A — 22 подростка, которые в качестве метода терапии ожирения проходили обучение в «Школе снижения массы тела», 1B — 21 пациент, которому помимо посещения занятий по модификации образа жизни была назначена битемпоральная транскраниальная магнитотерапия (ТкМТ) в сочетании с транскраниальной электростимуляцией (ТЭС), 1C — 21 подросток, обучающийся в «Школе снижения массы тела» и дополнительно получающий лечение препаратом лираглутид 3,0 мг.
Для оценки состояния углеводного и липидного обменов у всех пациентов выполнялся биохимический анализ крови: определялось содержание глюкозы крови, иммунореактивного инсулина, С-пептида, гликированного гемоглобина, индекс Homeostasis model assessment, показатели уровня холестерина, триглицеридов, липопротеинов низкой плотности, липопротеинов высокой плотности. С целью определения нейроэндокринно-иммунного статуса изучался гормональный профиль (показатели уровня фолликулостимулирующего гормона, лютеинизирующего гормона, тестостерона общего, эстрадиола, пролактина), значения ряда нейромедиаторов (кисспептина, лептина, фактора роста нервов, β-эндорфина) и цитокинов (интерлейкинов 1 и 10).
ТкМТ в сочетании с ТЭС выполнялась с помощью аппарата «АМО-АТОС-Э» (ООО «ТРИМА», г. Саратов, регистрационное удостоверение МЗ РФ № ФСР 209-04 781). Курс лечения включал 10 процедур. Медикаментозное лечение ожирения осуществлялось препаратом лираглутид 3,0 мг (номер регистрационного удостоверения: ЛП-003491), который вводился подкожно 1 раз в сутки, стартовая доза — 0,6 мг/сут.
Статистическая обработка полученных данных производилась с использованием пакета статистических программ Statistica 8.
Результаты. Независимо от пола у подростков с экзогенно-конституциональным ожирением по сравнению со здоровыми детьми статистически значимые различия выявлены в состоянии углеводного и жирового обменов, а также нейроэндокринно-иммунного статуса. Девочки основной группы имели более высокие уровни ЛГ и тестостерона общего, чем пациентки контрольной группы. У мальчиков с экзогенно-конституциональным ожирением в сравнении с группой контроля выявлены более высокие значения показателей кисспептина, лептина и эстрадиола и более низкие — тестостерона. В основной группе у детей обоих полов отмечено статистически значимое снижение уровня β-эндорфина — одного из факторов, способствующих возникновению удовлетворенности от приема пищи.
После посещения занятий в «Школе снижения массы тела» у мальчиков 1А подгруппы отчетливо прослеживалась тенденция к постепенному снижению массы тела на 1-м и 3-м месяце терапии с последующим значимым набором к 6-му месяцу лечения. У девочек 1А подгруппы увеличение массы тела отмечалось уже с 3-го месяца терапии. В подгруппе 1B мальчики имели достоверно значимое снижение массы тела, окружности талии и бедер в течение всех периодов наблюдения, с замедлением темпов снижения массы тела к 6-му месяцу терапии; у девочек к 6-му месяцу лечения отмечалась тенденция к небольшому повышению повышению величины стандартных отклонений индекса массы тела. У детей подгруппы 1C вне зависимости от пола зафиксировано значимое снижение массы тела, уменьшение объема талии и бедер, сохраняющиеся на протяжении всех 6 месяцев терапии.
Заключение. Наибольшее влияние на снижение массы тела пациентов оказала терапия лираглутидом во время посещения «Школы снижения массы тела». При проведении сеансов ТкМТ в сочетании с ТЭС и обучением принципам модификации образа жизни были достигнуты более низкие результаты, что говорит о необходимости повторения курсов через 6 месяцев и постоянного контроля пациентов. Занятия в «Школе снижения массы тела» способствовали сопоставимому с остальными методами терапии снижению массы тела подростков лишь в течение 1-го месяца лечения с последующим трендом на повышение к 3-му и выраженному набору веса к 6-му месяцу терапии. Поскольку ТкМТ в сочетании с ТЭС и лираглутид обладают разными механизмами воздействия на звенья патогенеза ожирения, в целях улучшения результатов терапии возможно комплексное применение этих методов в лечении ожирения у подростков.
Ключевые слова: лираглутид, ожирение, программы снижения массы тела, транскраниальная физиотерапия
Скачать PDFБолотова Н.В., Белоусова М.С., Чередникова К.А., Филина Н.Ю., Поляков В.К., Аверьянов А.П. Комплексный подход к терапии ожирения у детей подросткового возраста. Вестник терапевта. 2023. № 3 (58) URL: https://journaltherapy.ru/statyi/kompleksnyj-podhod-k-terapii-ozhirenija-u-detej-podrostkovogo-vozrasta/ (дата обращения: дд.мм.гггг)
Болотова Нина Викторовна (автор для переписки) — д. м. н., профессор, профессор кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 5061-1600. https://orcid.org/0000-0002-8148-526X. E-mail: kafedranv@mail.ru
Белоусова Маргарита Сергеевна — ассистент кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 1950-6497. https://orcid.org/0000-0002-8979-5131. E-mail: margo_sergeevna94@mail.ru
Чередникова Ксения Александровна — к. м. н., доцент кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 5609-0099. https://orcid.org/0000-0001-8119-0405. E-mail: iw.nazarenko2012@yandex.ru
Филина Наталья Юрьевна — д. м. н., заведующая кафедрой пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 3390-1811. https://orcid.org/0000-0002-1613-4156. E-mail: natalya-filina@rambler.ru
Поляков Вадим Константинович — д. м. н., профессор кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 9928-9682. https://orcid.org/0000-0001-6162-7884. E-mail: polyakov_vk@mail.ru
Аверьянов Андрей Петрович — д. м. н., профессор кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. 410012, Россия, г. Саратов, ул. Большая Казачья, 112. eLIBRARY.RU SPIN: 1940-8093 https://orcid.org/0000-0002-0341-3199. E-mail: andaveryanov@mail.ru
A comprehensive approach to the treatment of obesity in adolescent children
N.V. Bolotova, M.S. Belousova, K.A. Cherednikova, N.Y. Filina, V.K. Polyakov, A.P.Averyanov
Saratov State Medical University named after V.I. Razumovsky, 112 Bolshaya Kazachia Str., Saratov, Russian Federation, 410012
Abstract
Aim: To evaluate the effectiveness of various methods of obesity therapy in adolescent children.
Design: A prospective single-center randomized clinical study.
Materials and methods: 64 children aged 12–17 years with exogenous constitutional obesity of 2–3 degrees were examined. The control group consisted of 29 children of the same age with normal body weight, without concomitant chronic pathology. In the main group, three subgroups were identified using random sampling: 1A — 22 adolescents who were trained at the School of Weight Loss as a method of treating obesity; 1B — 21 patients who, in addition to attending classes on lifestyle modification, were prescribed bitemporal transcranial magnetic therapy (TcMT) in combination with transcranial electrical stimulation (TES), 1C — 21 adolescents studying at the School of Weight Loss and additionally receiving treatment with liraglutide 3.0 mg.
To assess the state of carbohydrate and lipid metabolism, a biochemical blood test was performed in all patients: the content of blood glucose, immunoreactive insulin, C-peptide, glycated hemoglobin, the Homeostasis model assessment index, cholesterol levels, triglycerides, low-density lipoproteins, and high-density lipoproteins were determined. In order to determine the neuroendocrine-immune status, the hormonal profile was studied (levels of follicle-stimulating hormone, luteinizing hormone, total testosterone, estradiol, prolactin), the values of a number of neurotransmitters (kisspeptin, leptin, nerve growth factor, β-endorphin) and cytokines (interleukins 1 and 10). Bitemporal transcranial magnetic therapy (TcMT) in combination with transcranial electrical stimulation (TES) was performed using the AMO-ATOS-E apparatus (LLC "TRIMA", Saratov, registration certificate of the Ministry of Health of the Russian Federation No. FSR 209-04 781). The course of treatment included 10 procedures. Medical treatment of obesity included the use of the drug liraglutide (Registration certificate number: LP-003491). The drug was administered subcutaneously, 1 time per day, the starting dose was 0.6 mg / day. Statistical processing of the obtained data was carried out using the Statistica 8 statistical software package.
Study results: Regardless of gender, in adolescents with exogenous constitutional obesity compared with healthy children, statistically significant differences were found in the state of carbohydrate and fat metabolism, as well as neuroendocrine-immune status. Girls in the main group had higher levels of LH and total testosterone than patients in the control group. In boys with exogenous constitutional obesity, in comparison with the control group, higher values of kisspeptin, leptin and estradiol and lower values of testosterone were revealed. Both boys and girls showed a statistically significant decrease in the level of β-endorphin, one of the factors that ensure satisfaction from the feeling of eating.
After attending classes at the "School for Weight Loss", boys in subgroup 1A clearly showed a tendency toward a gradual decrease in body weight in the 1st and 3rd months of therapy, followed by a significant gain by the 6th month of treatment. In girls of subgroup 1A, an increase in body weight was noted already from the 3rd month of therapy. In subgroup 1B, boys had a significantly significant decrease in body weight, waist and hip circumference during all observation periods, with a slowdown in the rate of weight loss by the 6th month of therapy; in girls, by the 6th month of treatment, there was a tendency to a moderate increase in the standard deviations of body mass index. In children of subgroup 1C, regardless of gender, a significant decrease in body weight, a decrease in waist and hip volume was recorded, which persisted throughout all 6 months of therapy.
Conclusion: Therapy with liraglutide during a visit to the "Weight Loss School" had the greatest impact on patients’ weight loss. When conducting TcMT sessions in combination with EFT and training in the principles of lifestyle modification, lower results were achieved, which indicates the need to repeat courses after 6 months and constantly monitor patients. Classes at the "School of Body Weight Loss" contributed to a reduction in body weight in adolescents, comparable to other methods of therapy, only during the 1st month of treatment, with a subsequent trend towards an increase by the 3rd month and a pronounced weight gain by the 6th month of therapy. Since TcMT in combination with TES and liraglutide have different mechanisms of action on the pathogenesis of obesity, in order to improve the results of therapy, it is possible to use these methods comprehensively in the treatment of obesity in adolescents.
Keywords: obesity, liraglutide, transcranial physiotherapy, weight loss programs.
Н.В. Болотова, М.С. Белоусова, К.А. Чередникова, Н.Ю. Филина, В.К. Поляков, А.П. Аверьянов
ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Министерства здравоохранения Российской Федерации; Россия, г. Саратов
Медико-социальная значимость проблемы ожирения в детском и подростковом возрасте обусловлена его высокой распространенностью, тяжестью метаболических нарушений, ранним развитием ассоциированных с ожирением заболеваний и состояний, приводящих к потере трудоспособности, инвалидизации, снижению репродуктивного потенциала. Ожирение — это мультифакторное заболевание, которое развивается в результате сложного интегративного взаимодействия условий внешней среды, генетической предрасположенности и психологических особенностей человека. Связь между этими факторами объясняет Джейн Уордл в своей теории поведенческой восприимчивости (Behavioural susceptibility theory — BST) [1], согласно которой генетическая предрасположенность к избыточному накоплению жировой массы влияет на механизмы регуляции аппетита, что приводит к формированию нарушения пищевого поведения. Таким образом, трудность терапии ожирения обусловлена сложным характером взаимодействия всех его патогенетических звеньев, а также низкой мотивацией общества на соблюдение принципов здорового образа жизни.
Стратегия терапии ожирения у детей изложена в клинических рекомендациях 2021 года: ведущая роль в них отводится немедикаментозным методам лечения [2]. Важнейший компонент эффективной терапии —обучение в мотивационных школах контроля массы тела, где пациенты усваивают необходимую информацию о принципах рационального питания, важности физической активности, осуществляется динамическое наблюдение за детьми и оказание психологической поддержки. Ряд исследований посвящен применению физиотерапевтических методов лечения ожирения — транскраниальной магнитотерапии с эффектом бегущего магнитного поля (ТкМТ) в сочетании с транскраниальной электростимуляцией (ТЭС) и цветоритмотерапии, способствующим снижению аппетита и коррекции вегетососудистой дисфункции, которая возникает на фоне ожирения [3–7].
Возможности медикаментозной терапии ожирения у детей до настоящего времени были ограничены. Единственным препаратом, разрешенным для лечения ожирения у детей в Российской Федерации, являлся орлистат. Однако частота и тяжесть побочных эффектов терапии, таких как болевой абдоминальный синдром, метеоризм, отхождение газов с выделением каловых масс, учащение кратности стула, ограничивают возможности его применения. Метформин может быть использован в комплексной терапии ожирения лишь в случае выявления нарушений углеводного обмена и при достижении возраста 10 лет [8]. В январе 2021 года в педиатрической практике был зарегистрирован препарат группы агонистов глюкакогоноподобного пептида 1 (ГПП-1) — лираглутид 3,0 мг, показавший высокую эффективность в отношении терапии ожирения и ассоциированных с ним нарушений метаболического статуса у взрослых [9–15]. Однако результаты его применения у детей подросткового возраста в специальной литературе освещены недостаточно.
Цель исследования: оценить эффективность различных методов терапии ожирения у детей подросткового возраста.
Материалы и методы
Нами проведено проспективное одноцентровое рандомизированное клиническое исследование 64 детей с экзогенно-конституциональным ожирением 2–3-й степени (33 мальчиков и 31 девочки), которые проходили лечение в Университетской клинической больнице № 1 им. С.Р. Миротворцева г. Саратова в 2020–2022 годах. Протокол одобрен этической комиссией ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Министерства здравоохранения Российской Федерации по контролю над исследовательскими работами с участием человека. Все обследованные дети (с 15 лет) и/или их родители подписывали информированное согласие для участия в исследовании.
Критерии включения в исследование: возраст пациентов 12–17 лет, наличие экзогенно-конституционального ожирения 2–3-й степени. Критерии исключения: отсутствие ожирения, синдромальные формы ожирения, наличие тяжелой сопутствующей соматической патологии. Контрольную группу составили 29 детей того же возраста с нормальной массой тела, без сопутствующей хронической патологии.
На первом этапе пациенты основной и контрольной групп были обследованы по единому алгоритму, включающему изучение жалоб, анамнеза заболевания и жизни, оценку объективных данных, результатов лабораторно-инструментальных исследований.
На втором этапе исследования группа детей с ожирением была разделена на три подгруппы методом случайной выборки. В подгруппу 1А включены 22 подростка, которые в качестве метода терапии ожирения проходили обучение в «Школе снижения массы тела», в подгруппу 1B — 21 пациент, которому помимо посещения занятий по модификации образа жизни была назначена физиотерапия ТкМТ в сочетании ТЭС, в подгруппу 1C — 21 подросток, обучающийся в «Школе снижения массы тела» и дополнительно получающий лечение препаратом лираглутид 3,0 мг.
Антропометрические параметры пациентов (показатели роста, массы тела, индекса массы тела (ИМТ)) изучались в динамике через 1, 3 и 6 месяцев. Производился расчет стандартных сигмальных отклонений (Standard Deviation Score, SDS) с помощью приложения Auxology (Munich Auxology Project, Kromeyer-Hauschild et al., 2001). Ожирение диагностировалось при повышении SDS ИМТ более 2,0: 2,0–2,5 — 1-я степень, 2,6–3,0 — 2-я степень, 3,1–3,9 — 3-я степень, ≥ 4,0 — морбидное ожирение. Определение стадии полового развития осуществлялось по шкале Таннера [16].
Оценка липидного и углеводного обменов проводилась на основании показателей биохимического анализа крови: определялось содержание холестерина, триглицеридов, липопротеинов низкой плотности (ЛПНП), липопротеинов высокой плотности (ЛПВП), глюкозы крови, иммунореактивного инсулина, С-пептида, гликированного гемоглобина, наборами IMMULITE 2000 XPi и ARCHTEST i2000SR (Siemens, Abbot, Германия). Уровень лептина анализировался с помощью Leptin ELISA DBC, Vertion 10 (Германия). Рассчитывался индекс Homeostasis model assessment (НОМА) по формуле: HOMA = (ИРИ0 × Г0) / 22,5, где ИРИ (иммунореактивный инсулин) — концентрация инсулина в сыворотке крови натощак, мкЕД/мл, Г0 (глюкоза) — глюкоза плазмы натощак, ммоль/л).
Оценка гормонального профиля производилась на основании определения уровней тиреотропного гормона (ТТГ), фолликулостимулирующего гормона (ФСГ), лютеинизирующего гормона (ЛГ), тестостерона (Т), пролактина, эстрадиола наборами IMMULITE 2000 XPi и ARCHTEST i2000SR (Siemens, Abbot, Германия). Дополнительно для исключения патологических изменений всем детям было проведено ультразвуковое исследование (УЗИ) щитовидной железы аппаратом COMBISON-320 S (Германия).
Исследованы уровни нейропептида кисспептина (Kiss1, Cloud-Clone Corp, Китай), фактора роста нервов (RayBio Human beta-NGFELISA Kit) и β-эндорфина (EIA Kitforbeta-Endorphin PLI). Определялись значения интерлейкинов 1 и 10 (ИЛ-1 и ИЛ-10) наборами ИФА Вектор-Бест (Россия).
Для диагностики стеатогепатоза, стеатогепатита проведено УЗИ органов брюшной полости аппаратом COMBISON-320 S (Германия), исследование содержания аспартатаминотрансферазы (АсТ), аланинаминотрансферазы (АлТ), билирубина общего наборами IMMULITE 2000 XPi и ARCHTEST i2000SR (Siemens, Abbot, Германия).
Для оценки морфофункциональных особенностей состава тела использован метод биоимпедансометрии, исследование проведено на анализаторе ABC-01 «Медасс» (Россия).
Битемпоральная ТкМТ в сочетании с ТЭС выполнялась с помощью аппарата «АМО-АТОС-Э» (ООО «ТРИМА», г. Саратов, регистрационное удостоверение МЗ РФ №ФСР 209-04 781), включающего приставку «Оголовье» и блок ТЭС-терапии с лобно-сосцевидными электродами на фиксаторах терминалов «Оголовья». Курс лечения — 10 процедур.
Медикаментозная терапия ожирения состояла в применении препарата лираглутид (номер регистрационного удостоверения: ЛП-003491), который вводился пациентам подкожно 1 раз в сутки, стартовая доза составляла 0,6 мг/сут. При хорошей переносимости препарата титрация дозы осуществлялась 1 раз в неделю, при появлении выраженных побочных эффектов — 1 раз в 2 недели. В одном случае интенсификация терапии проводилась 1 раз в 3 недели в связи с развитием выраженных побочных эффектов при повышении дозы 1 раз в 2 недели.
Статистическая обработка полученных данных производилась с использованием пакета статистических программ Statistica 8. Все данные в работе представлены для непараметрических критериев. Для сравнения двух групп по количественным признакам рассчитывался критерий Манна — Уитни; различия считались статистически значимым при р < 0,05. При сравнении трех и более зависимых совокупностей, распределение которых отличалось от нормального, использовался непараметрический критерий Фридмана с апостериорными сравнениями с помощью критерия Коновера — Имана с поправкой Холма; различия считались статистически значимыми при p < 0,05. При сравнении трех и более независимых совокупностей, распределение которых отличалось от нормального, применялся тест Краскела — Уоллиса, различия считались статистически значимыми при p < 0,05. Клинически значимым изменением SDS ИМТ считалось его снижение на 0,2, порогом для клинически значимого изменения — снижение в диапазоне от 0,2 до 0,25 [17]
Результаты
Из 64 пациентов при поступлении в стационар лишь 50 (78,1%) детей предъявляли жалобы на повышенную массу тела, что подчеркивает отсутствие восприятия ожирения как заболевания. Жалобы на повышенный аппетит имели 36 (56,2%) детей, головные боли — 37 (57,8%), повышение артериального давления (АД) — 25 (39,0%), одышку при привычной физической нагрузке — 34 (53,1%), потливость — 12 (18,8%). Различные нарушения овариально-менструального цикла (НОМЦ) отмечали 25 (80,6%) девочек, избыточный рост волос — 7 (22,6%).
При изучении анамнеза жизни установлено, что у 25 (39,0%) пациентов избыточный набор массы тела определялся в раннем детском возрасте — в 1–3 года, у 16 (25,0%) — в 4–6, у 12 (18,8%) — в 6–12, у 4 (6,3%) — в 12–17 лет. Избыточную массу тела при рождении имели 8 (12,5) детей. У подавляющего большинства пациентов отмечалась отягощенная наследственность: 47 (73,4%) детей имели родственников 1-й и 2-й степени родства, страдающих ожирением различной степени выраженности, 26 (40,6%) — сахарным диабетом 2 типа, 36 (56,3%) — артериальной гипертензией.
Распределение подкожно-жировой клетчатки у пациентов основной группы было неравномерным, с преимущественным отложением в области живота. У 26 (40,6%) детей диагностирована гиперпигментация естественных кожных складок, у 13 (20,3%) — фолликулит, у 27 (42,2%) — полосы растяжения от жемчужно-розового до ярко-розового цвета. У 21 (63,6%) мальчика диагностирована ложная гинекомастия. Избыточный рост волос в гирсутных зонах имели 8 (25,8%) девочек. При оценке антропометрических показателей медиана SDS роста у мальчиков составила 0,9 [0,3; 1,6], ИМТ — 35,7 [30,4; 39,7], SDS ИМТ — 3,3 [2,9; 3,8], у девочек SDS роста — 0,5 [0,0; 1,4], ИМТ — 32,7 [31,2; 34,2], SDS ИМТ — 3,1 [2,7; 3,3]. Экзогенно-конституциональное ожирение 2-й степени диагностировано у 22 (34,4%) детей, 3-й степени — у 42 (65,6%).
Оценка степени половой зрелости показала, что в стадии Таннер I были 3 (9,0%) мальчика (из них у 2 (6,0%) отмечена задержка полового развития), Таннер II и III — 24 (72,7%), Таннер IV и V — 6 (18,3%). Среди девочек в стадии Таннер II и III были 10 (32,3%) пациенток, Таннер IV и V — 21 (67,7%).
НОМЦ были у 25 (80,6%) девочек: наиболее часто диагностировалась вторичная олигоменорея, вторичная аменорея — у 14 (45,2%), дисменорея — у 6 (19,4%), гиперменорея — у 5 (16,1%).
Результаты анализа метаболического статуса детей с экзогенно-конституциональным ожирением в сравнении с группой контроля пациентов представлены в таблице 1.
Таблица 1. Метаболические параметры пациентов в группах исследования, Ме [Q1; Q3]
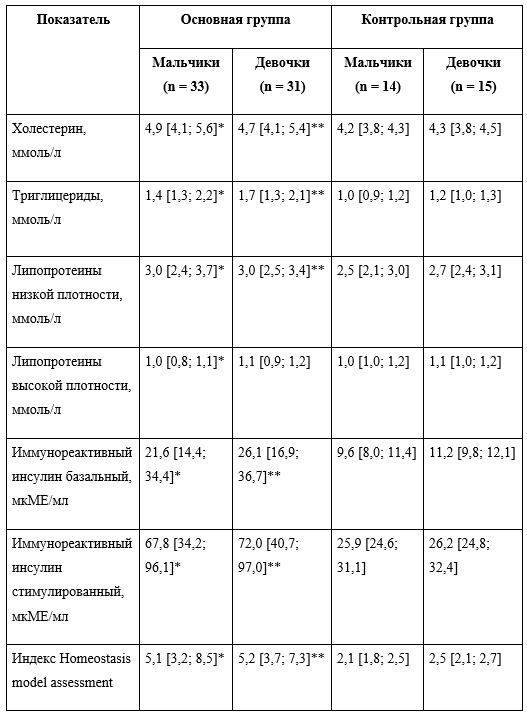

Примечание. Отличия от контрольной группы статистически значимы (*, **) — p < 0,05.
Независимо от пола у пациентов с экзогенно-конституциональным ожирением уровни гликированного гемоглобина, базального и стимулированного иммунореактивного инсулина, С-пептида и индекс НОМА были достоверно выше, чем у детей контрольной группы. Гиперинсулинемия и инсулинорезистентность диагностированы у 51 (79,7%) ребенка с ожирением. При проведении перорального глюкозо-толерантного теста нарушение толерантности к глюкозе выявлено у 9 (14,0%) пациентов, гипергликемия натощак — у 2 (3,1%), сахарный диабет 2 типа — у 3 (4,7%).
Показатели общего холестерина, триглицеридов, ЛПНП у пациентов основной группы были достоверно выше, а ЛПВП — ниже, чем в контрольной. Дислипидемия, гиперхолестеринемия, гипертриглицеридемия были диагностированы в половине случаев.
Диффузные изменения печени выявлены у всех детей основной группы. Значимых различий между уровнем трансаминаз, билирубина общего в группах выявлено не было.
При оценке нейроэндокринно-иммунного статуса у детей с ожирением в сравнении контрольной группой были выявлены статистически значимые различия (табл. 2).
Таблица 2. Параметры нейроэндокринно-иммунного статуса в группах исследования, Ме [Q1; Q3]


Примечание. Отличия от контрольной группы статистически значимы (*, **) — p < 0,05.
У девочек с экзогенно-конституциональным ожирением отмечены более высокие показатели ЛГ, тестостерона общего, чем у пациенток контрольной группы, а также снижение уровня эстрадиола общего, однако статистически значимых различий выявлено не было. В сочетании с метаболическим синдромом выявленные нарушения в дальнейшем могут стать причиной развития различных НОМЦ и синдрома поликистозных яичников. Обращает на себя внимание значимое снижение уровня кисспептина на фоне высоких концентраций лептина, что свидетельствует о нарушении характера их физиологического взаимодействия в связи с развитием гиперлептинемии и лептинорезистентности.
У мальчиков основной группы по сравнению с представителями контрольной группы зафиксированы более высокие значения уровня кисспептина, лептина и эстрадиола, ниже уровень тестостерона общего. Высокий показатель кисспептина и низкий — тестостерона общего у мальчиков с экзогенно-конституциональным ожирением может быть причиной задержки, пролонгации пубертата [18].
В основной группе отмечено статистически значимое повышение уровня провоспалительных (ИЛ-1) и противовоспалительных (ИЛ-10) цитокинов по сравнению с данными контрольной группы. Более высокое содержание исследуемых интерлейкинов указывает на развитие хронического низкоинтенсивного воспаления на фоне экзогенно-конституционального ожирения. Усиление продукции ИЛ-10 способствует хронизации и неблагоприятному течению воспаления [18].
И у мальчиков, и у девочек основной группы было выявлено статистически значимое снижение уровня β-эндорфина — одного из факторов, способствующих возникновению удовлетворенности от приема пищи.
Патологических изменений в структуре щитовидной железы у детей основной группы выявлено не было. Уровень тиреоидных гормонов соответствовал нормальным значениям.
Исследование компонентного состава тела проведено в группе пациентов с экзогенно-конституциональным ожирением. Ввиду отсутствия значимых различий оценка характера выявленных нарушений производилась совместно для обоих полов. У 54 (84,4%) детей показатель активной клеточной массы был в пределах нормальных значений, однако у 25 (39,1%) доля активной клеточной массы была снижена. Несмотря на достаточный объем скелетной мускулатуры (кг), у 19 (29,7%) пациентов была снижена доля скелетно-мышечной массы. Полученные результаты говорят о развитии ложной гипертрофии мышечной массы за счет чрезмерного разрастания жировой ткани, приводящего к атрофии мышечных волокон. [18]. Сочетанное снижение объема скелетно-мышечной массы (кг) и доли скелетно-мышечной массы отмечалось у 7 (10,9%) детей, что свидетельствует о развитии саркопении и формировании саркопенического ожирения. Низкий удельный основной обмен имели 2/3 (66,6%) пациентов. Повышенный уровень общей и внеклеточной жидкости выявлен у 56 (87,5%) детей.
Для оценки эффективности различных подходов к терапии ожирения методом случайной выборки пациенты с экзогенно-конституциональным ожирением были распределены на 3 подгруппы. Дети подгруппы 1А (n = 22) проходили обучение в «Школе снижения массы тела», которая была создана на базе кафедры пропедевтики детских болезней, детской эндокринологии и диабетологии ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Министерства здравоохранения Российской Федерации в 2006 году. Программа школы включает 5 семинаров, посвященных вопросам модификации образа жизни, физиотерапевтическое лечение, консультации психолога и ежемесячный осмотр эндокринолога. Длительность наблюдения пациентов в рамках данной программы составляет 6 месяцев. Семинары носят индивидуальный, семейно-ориентированный характер, поскольку вовлеченность и поддержка со стороны семьи имеют важное значение для достижения положительного результата терапии [20]. Занятия в «Школе снижения массы тела» проводятся 1 раз в неделю в течение 45–60 минут. Семинары включают следующие этапы:
Подведение итогов работы детей в «Школе снижения массы тела» проводится с применением мер поощрения (грамот, призов).
Из числа обследованных лишь 9 (40,9%) детей подгруппы 1А прошли полный цикл занятий в «Школе снижения массы тела». Пациенты, не окончившие обучение, получили дополнительные рекомендации по модификации образа жизни.
Таблица 3. Динамика антропометрических показателей пациентов подгруппы 1А, Ме [Q1; Q3]
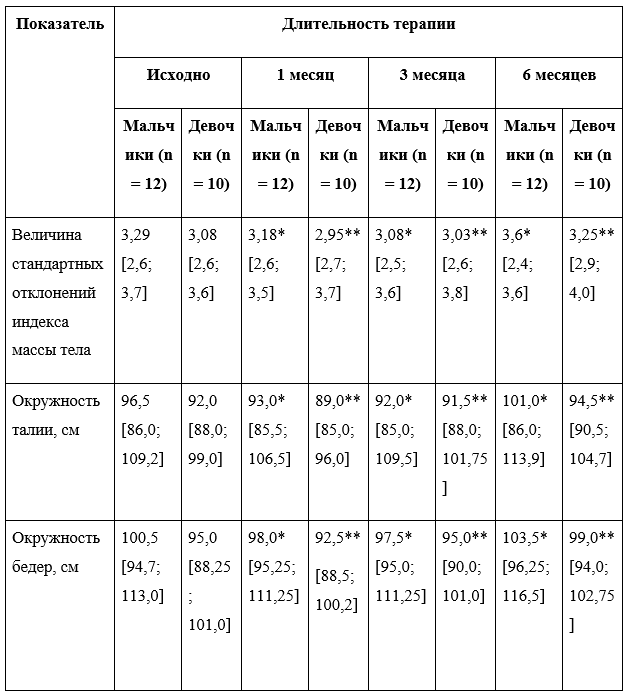
Примечание. Отличия от контрольной группы статистически значимы (*, **) — p < 0,05.
Изменения антропометрических параметров пациентов подгруппы 1А в ходе всего периода наблюдения были статистически значимыми (табл. 3). У мальчиков отмечена тенденция к постепенному снижению массы тела на 1-м и 3-м месяце терапии с последующим значимым набором к 6-му месяцу, у девочек увеличение массы тела зафиксировано с 3-го месяца терапии. Тем не менее, прибавка массы тела уже на 1-м месяце лечения отмечалась у 7 (31,8%) пациентов, на 3-м— у 8 (36,4%), на 6-м — у 18 (81,8%). Клинически значимое снижение SDS ИМТ на 1-м месяце терапии было достигнуто у 1 (4,5%) ребенка, к 3-му —у 3 (13,6%), к 6-му не отмечено ни у одного ребенка.
Для повышения эффективности обучения в «Школе снижения массы тела» в группе пациентов с экзогенно-конституциональным ожирением выделена подгруппа 1B (n = 21), в которой для лечения детей использовалась ТКмТ в сочетании с ТЭС. Такая сочетанная терапия позволяет комплексно воздействовать на центры голода и насыщения гипоталамо-гипофизарной системы, что способствует снижению аппетита и нормализации пищевого поведения. Положительный эффект лечения реализуется за счет нормализации нейромедиаторного дисбаланса, это приводит к повышению физиологических и эмоционально-аффективные показателей, улучшению местных механизмов микроциркуляции, способствует усилению саногенетических реакций [7].
Таблица 4. Динамика антропометрических показателей пациентов подгруппы 1B, Ме [Q1; Q3]

Примечание. Отличия от контрольной группы статистически значимы (*, **) — p < 0,05.
На фоне ТкМТ в сочетании с ТЭС в динамике у мальчиков отмечалось статистически значимое снижение массы тела, окружности талии и бедер, с замедлением темпов снижения массы тела к 6-му месяцу терапии. У девочек к 6-му месяцу лечения отмечалась тенденция к умеренному повышению значений SDS ИМТ, замедлению темпов уменьшения окружности талии и бедер (табл. 4). Прибавка массы тела на 3-м месяце терапии была отмечена лишь у 1 (4,8%) ребенка, на 6-м — у 2 (9,5%). Клинически значимое снижение SDS ИМТ на 1-м месяце терапии было достигнуто у 3 (14,3%), к 3-му — у 10 (47,6%), к 6-му — у 4 (19,0%) пациентов данной подгруппы.
В подгруппе 1C (n = 21) дополнительно к обучению пациентам был назначен препарат лираглутид, который продемонстрировал положительное влияние на снижение массы тела, обусловленное его способностью подавлять аппетит и модулировать вкусовые предпочтения [19]. Этот эффект реализуется, с одной стороны, за счет воздействия на рецептор ГПП-1 в гипоталамусе, что приводит к прямой стимуляции анорексигенных нейромедиаторных систем (проопиомеланокортина, кокаин- и амфетамин-регулируемых транскриптов) и подавлению орексигенных (нейропептида Y, агути-родственного белка), а с другой — за счет замедления опорожнения желудка и всей моторики желудочно-кишечного тракта [20]. ГПП-1 моделирует секрецию инсулина в зависимости от характера поступающей пищи, что обеспечивает нормализацию показателей углеводного обмена [21]. Он также состояние липидного обмена [22–25]. К наиболее распространенным побочным эффектам препарата относятся нарушения со стороны желудочно-кишечного тракта: тошнота, рвота, учащение кратности стула, абдоминальный болевой синдром. Однако при приеме по схеме титрации дозы в соответствии с инструкцией они проявляются умеренно или незначительно, что не требует отмены препарата.
У всех пациентов подгруппы 1С возникали побочные эффекты различной степени выраженности. Незначительную тошноту в 1–3-и сутки после начала введения препарата или повышения его дозы отмечали 12 (57,1%) детей. Умеренная боль в животе, тошнота, сохраняющиеся в течение 3–4 суток после начала терапии и повышения дозы препарата, беспокоили 2 (9,5% пациентов). В соответствии с переносимостью лечения титрация дозы 1 раз в неделю производилась у 17 (81,0%) пациентов, 1 раз в 2 недели — у 4 (19,0%). Итоговой дозы препарата 3,0 мг/сут. достигли 18 (85,7%) пациентов, 2,4 мг/сут. —2 (9,5%), 1,8 мг/сут. — 1 (4,8%). Особенно стоит отметить одного пациента, у которого на фоне повышения дозы препарата 1 раз в 2 недели развивалась выраженная тошнота, 1–2-кратная рвота, интенсивные боли в животе, сохраняющиеся в течение 2–3 суток. При согласии родителей ребенка было принято решение о переходе на режим титрации 1 раз в 3 недели, на фоне чего тяжелые побочные эффекты были полностью нивелированы — пациент испытывал лишь незначительную тошноту, как и большинство детей данной подгруппы.
Таблица 5. Динамика антропометрических показателей пациентов подгруппы 1C, Ме [Q1; Q3]
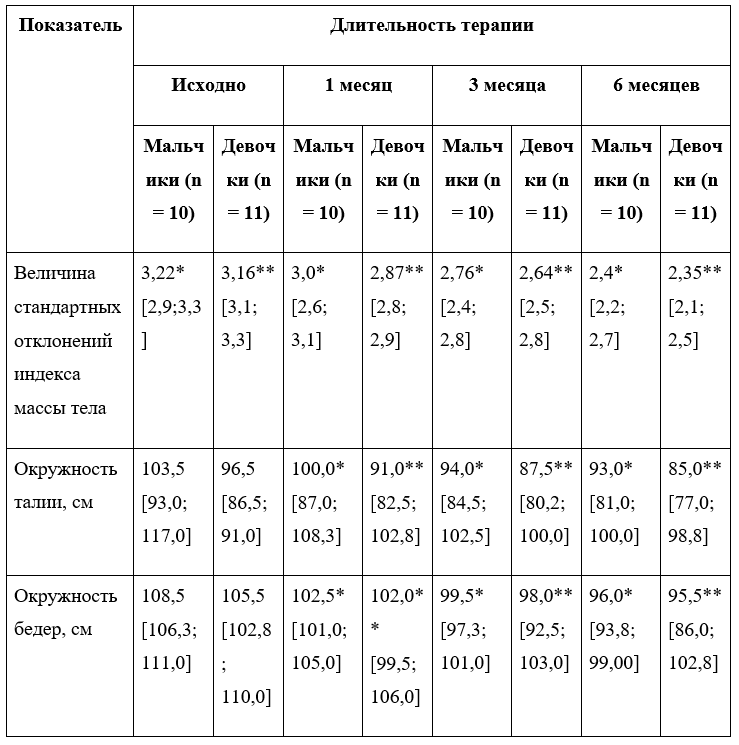
Примечание. Отличия от контрольной группы статистически значимы (*, **) — p < 0,05.
У всех пациентов подгруппы 1С вне зависимости от пола зафиксировано значимое снижение массы тела, уменьшение объема талии и бедер, сохраняющиеся на протяжении всех 6 месяцев терапии (табл. 5). Однако у 2 детей, несмотря на исходно значимую потерю массы тела к 1-му месяцу терапии, на фоне продолжающегося введения лираглутида в суточной дозе 3,0 мг отмечался прогрессивный набор массы тела с возвращением ранее потерянных килограммов к 3-му месяцу лечения, у 1 пациента аналогичная динамика наблюдалась к 6-му месяцу терапии. Клинически значимое снижение SDS ИМТ на 1-м месяце лечения было достигнуто у 17 (81,0%) пациентов, к 3-му — у 3 (14,3%), к 6-му — у 1 (4,8%).
При анализе полученных данных установлено, что статически значимые различия в динамике SDS ИМТ при использовании разных подходов к терапии ожирения отмечались уже с 3-го месяца лечения (рис. 1, 2).

Рис. 1. Динамика величины стандартных отклонений индекса массы тела на фоне различных методов терапии ожирения у мальчиков
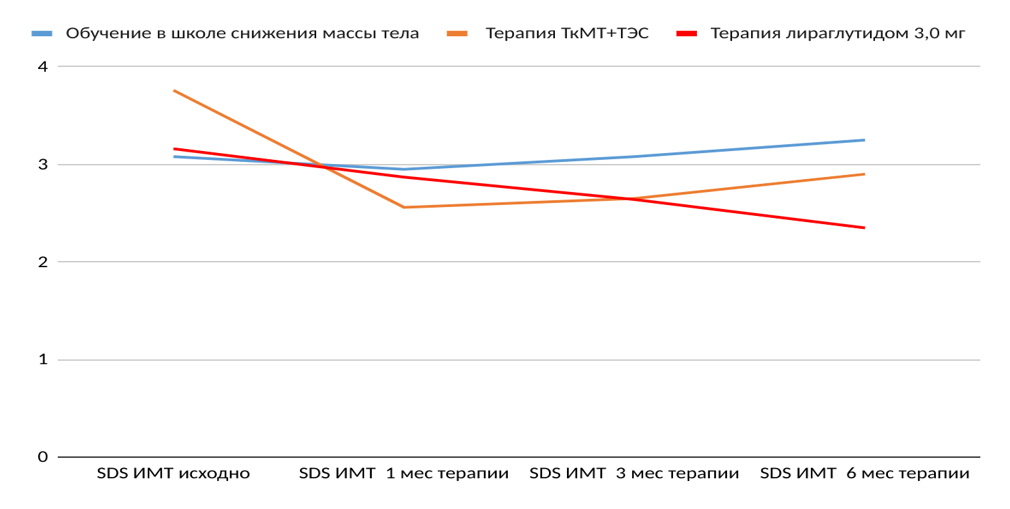
Рис. 2. Динамика величины стандартных отклонений индекса массы тела на фоне различных методов терапии ожирения у девочек
Оценка динамики SDS ИМТ по данным линейной диаграммы показала, что наиболее высоких результатов в отношении снижения массы тела удалось достичь при применении лираглутида 3,0 мг. Менее выраженный эффект зарегистрирован у ТкМТ в сочетании с ТЭС. Обучение в «Школе снижения массы тела» обеспечивало сопоставимое с ТкМТ в сочетании с ТЭС снижение массы тела в течение 1-го месяца терапии с последующим трендом на повышение к 3-му и выраженному повышению к 6-му месяцу терапии.
Обсуждение
Отсутствие жалоб на избыточную массу тела у 14 (21,9%) детей основной группы, небольшой процент пациентов, полностью завершивших обучение в «Школе снижения массы тела» свидетельствуют о низкой обеспокоенности детей и прежде всего их родителей проблемой ожирения. В исследовании О.В. Лерман и соавт., посвященном информированности, приверженности и отношению пациентов к лекарственной терапии ожирения, были получены аналогичные результаты. Каждый 6-й взрослый пациент с ожирением 1-й степени считал свою массу тела нормальной, лишь 76,5% были готовы продолжить ее снижать, более 70% не хотели тратить денежные средства на борьбу с ожирением, 90% не считали необходимыми расходы на медикаментозную терапию [26]. В исследование И.Н. Мартыновой и соавт. Были включены 368 детей, имеющих экзогенно-конституциональное ожирение, но семьи лишь 98 (26,6%) из них самостоятельно обратились по данному поводу на первичную консультацию к эндокринологу, в том числе только 50 согласились на прохождение «Школы снижения массы тела» [27].
Некоторые авторы отмечают высокую эффективность программ снижения массы тела непосредственно после окончания их прохождения [27–29]. В нашем исследовании высокие результаты зафиксированы только на 1-м месяце терапии, в последующем у пациентов определялся прогрессивный набор веса к 6-му месяцу наблюдения. Аналогичные данные были получены в работе M. Perdew и соавт.: на фоне прохождения семейно-ориентированной программы по снижению массы тела продолжительностью 10 недель значимой динамики SDS ИМТ у детей отмечено не было; авторы предположили, что, возможно, необходим более длительный период обучения [30]. Таким образом, современный пациент, страдающий экзогенно-конституциональным ожирением, в большинстве случаев имеет низкую мотивацию на модификацию образа жизни.
Одной из причин недостаточной эффективности программ снижения массы тела также может являться выявленный дисбаланс в нейроэндокринном и иммунном статусе у детей с ожирением. Так, у мальчиков-подростков с экзогенно-конституциональным ожирением на фоне снижения массы тела не было отмечено значимой динамики параметров нейроэндокринно-иммунного статуса [7]. В работе M.J.C.M. Augustijn и соавт. было выявлено, что даже на фоне снижения массы тела у пациентов с ожирением сохранялись нарушения в структурных связях моторной коры и системы поощрения головного мозга [31].
Становится очевидным, что усиление терапии ожирения необходимо не только для повышения приверженности к лечению, но и для коррекции нейроэндокринно-иммунного дисбаланса, что в совокупности должно обеспечивать высокую эффективность терапии.
Интенсификация терапии ожирения с применением ТкМТ в сочетании с ТЭС значимо способствовала снижению массы тела. Однако, учитывая выявленную тенденцию к замедлению темпов снижения массы тела к 6-му месяцу терапии у мальчиков, умеренному повышению значений SDS ИМТ у девочек, необходимо рассмотреть возможность проведения повторных сеансов физиотерапии с интервалом не более 6 месяцев для достижения более стойкого результата. В исследовании Ю.В. Владимировой на фоне последовательного проведения 3 курсов магнитотерапии с интервалом между повторными процедурами в 1 месяц было получено стойкое снижение массы тела пациентов [32]. Эти данные подтверждают нашу гипотезу о необходимости проведения повторных курсов терапии.
Применение лираглутида 3,0 мг в комплексной терапии ожирения в подгруппе 1С способствовало наибольшему снижению SDS ИМТ по сравнению с показателями пациентов остальных подгрупп, что согласуется с данными других авторов, а также данными рандомизированного плацебо-контролируемого исследования SCALE Teens [33, 34]. Однако стоит учитывать, что, несмотря на высокую эффективность данного препарата, у 3 пациентов отмечался значительный набор массы тела на фоне продолжающегося лечения в дозе 3,0 мг/сут.
Заключение
Наибольшую эффективность в отношении снижения массы тела продемонстрировала терапии лираглутидом на фоне обучения в «Школе снижения массы тела». Сеансы ТкМТ в сочетании с ТЭС и обучением принципам модификации образа жизни показали менее высокие результаты, что требует повторения курсов лечения через 6 месяцев и постоянного контроля пациентов. Обучение в «Школе снижения массы тела» обеспечивало сопоставимое с остальными методами терапии снижение массы тела лишь в течение 1-го месяца терапии с последующим трендом на повышение к 3-му и выраженному набору веса к 6-му месяцу лечения. Поскольку ТкМТ в сочетании с ТЭС и лираглутид обладают разными механизмами воздействия на звенья патогенеза ожирения, в целях улучшения результатов терапии возможно комплексное применение этих методов в лечении ожирения у подростков.
Финансирование
Исследование выполнено в рамках научного проекта ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» МЗ РФ. №SSMU-2022-006 «Разработка программ персонифицированного лечения детей с ожирением».
Предыдущая статья
Р.Т. Макишева ФГБОУ ВО «Тульский государственный университет»; Россия, г. Тула Ожире...
Следующая статья
И.В. Уфимцева1, С.В. Яковлева1, И.Ю. Пирогова2 1 ООО ...