Влияние коморбидности на течение и эффективность лечения неалкогольной жировой болезни печени в сочетании с желчнокаменной болезнью
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- возраст пациентов 18–65 лет;
- наличие ЖКБ;
- согласие на участие в исследовании.
- злокачественные новообразования (в анамнезе до 5 лет);
- тяжелые заболевания сердечно-сосудистой системы, легких и почек в течение 5 лет;
- ментальные расстройства и психические заболевания, затрудняющие контакт;
- наличие заболеваний печени другой этиологии.
- Литература
- Ивашкин В.Т., Лапина Т.Л. ред. Гастроэнтерология. Национальное руководство. Краткое издание. М.: ГЭОТАР-Медиа; 2015. 480 с. Ivashkin V.T., Lapina T.L. Gastroenterology. National leadership. Short edition. M.: GEOTAR-Media; 2015. 480 p. (in Russian)
- Бордин Д.С. Рекомендации научного общества гастроэнтерологов России по диагностике и лечению желчнокаменной болезни. Экспериментальная и клиническая гастроэнтерология. 2012;4:114–23.Bordin D.S. Recommendations of the Gastroenterologists Scientific Society of Russia in the diagnosis and treatment of cholelithiasis disease. Experimental and Clinical Gastroenterology. 2012;4:114–23. (in Russian)
- Скворцова Т.Э., Ситкин С.И., Радченко В.Г, Селиверстов П.В. и др. Желчнокаменная болезнь. Современные подходы к диагностике, лечению и профилактике: пособие для врачей. М.: Фортепринт, 2013. 32 с. Skvortsova T.E., Sitkin S.I., Radchenko V.G., Seliverstov P.V. et al. Modern approaches to diagnostics, treatment and preventive policies: a guide for physicians. M.: Forteprint, 2013. 32 p. (in Russian)
- Chen L.Y., Qiao Q.H., Zhang S.C., Chen H. et al. Metabolic syndrome and gallstone disease. World J. Gastroenterol. 2012;18(31):4215–20. DOI:10.3748/wjg.v18.i31.4215
- Буеверов А.О. Клинико-патогенетические параллели неалкогольной жировой болезни печени и желчнокаменной болезни. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2019;29(1):17–23. Bueverov A.O. Clinical and pathogenetic parallels of nonalcoholic fatty liver disease and gallstone disease. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2019;29(1):17– (in Russian). DOI: 10.22416/1382-4376-2019-29-1-17-23
- Zhao S.F., Wang A.M., Yul X.J., Wang L.L. et al. Association between gallstone a cardio-cerebrovascular disease: systematic review and meta-analysis. Exp. Ther. Med. 2019;17(4):3092–3100. DOI:10.3892/etm.2019.7291
- Kawada T. Liver fat, visceral fat and metabolic syndrome in patients with severe obesity. Int. J. Surg. 2015;22:153. DOI: 10.1016/j.ijsu.2015.09.001
- DiCiaula A., Portincasa P. Recent advances in understanding and managing cholesterol gallstones. F1000Res. 2018;7:F1000. DOI: 10.12688/f1000research.15505.1
- Monzón G., Castrillón J.V., Porrero J.L., Alonso M.T. et al. Prevalence and risk factors for biopsy-proven non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in a prospective cohort of adult patients with gallstones. Liver Int. 2015;35(8):1983–91. DOI: 10.1111/liv.1281
- Nogueira L., Freedman N.D., Engels E.A., Warren J.L. et al. Gallstones, cholecystectomy, and risk of digestive system cancers. Am. J.Epidemiol.2014;179(6):731–9. DOI: 10.1093/aje/kwt322
- Shen S., Gong J., Wang X., ChenL.et al. Promotional effect of nonalcoholic fatty liver disease on Gallstone disease: a systematic review and meta-analysis. Turk. J. Gastroenterol. 2017;28(1):31–9. DOI:10.5152/tjg.2016.0357
- Маевская М.В., Ивашкин В.Т. ред. Диагностика и лечение неалкогольной жировой болезни печени: методические рекомендации для врачей. М.: МЕДпресс-информ; 2012. 31 с. Mayevskaya M.V., Ivashkin V.T. ed. Diagnosis and treatment of non-alcoholic fatty liver disease: guidelines for doctors. : MEDpress-inform. 2012. 31 p. (in Russian)
- Комшилова К.А., Трошина Е.А. Ожирение и неалкогольная жировая болезнь печени. Лечение и профилактика. 2012;1(2):99–108. Komshilova K.A., Troshina E.A. Obesity and non-alcoholic fatty liver disease. Treatment and Prevention. 2012;1(2):99–108. (in Russian)
- Комшилова К.А., Трошина Е.А. Ожирение и неалкогольная жировая болезнь печени: метаболические риски и их коррекция. Ожирение и метаболизм. 2015;12(2):35–9. Komshilova K.A., Troshina E.A. Obesity and nonalcoholic fatty liver disease: metabolic risks and their correction. Obesity and Metabolism. 2015;12(2):35–9. (in Russian). DOI: 14341/omet2015234-38
- Лазебник Л.Б., Голованова Е.В., Туркина С.В., Райхельсон К.Л. и др. Неалкогольная жировая болезнь печени у взрослых: клиника, диагностика, лечение. Рекомендации для терапевтов, третья версия. Экспериментальная и клиническая гастроэнтерология. 2021;1(1):4–52. Lazebnik L.B., Golovanova E.V., Turkina S.V., Raikhelson K.L. et al. Non-alcoholic fatty liver disease in adults: clinic, diagnostics, treatment. Guidelines for therapists, third version. Experimental and Clinical Gastroenterology. 2021;1(1):4– (in Russian). DOI: 10.31146/1682-8658-ecg-185-1-4-52
- Пирогова И.Ю., Уфимцева И.В., Ушакова И.В., Жерносек Н.А. и др. Диагностическая и лечебная тактика ведения пациентов желчно-каменной болезнью. Уральский медицинский журнал. 2019;(3):30–8. Pirogova I.Yu., Ufimtseva I.V., Ushakova I.V., Zhernosek N.A. et al. Management the patients with gallstone disease. Ural Medical Journal. 2019;(3):30–8. (in Russian). DOI:10.25694/URMJ.2019.03.18
- Буеверов А.О. Холецистэктомия как фактор риска прогрессирования неалкогольной жировой болезни печени. Consilium Medicum. 2019;21(8):93–7. Bueverov A.O. Cholecystectomy as a risk factor of non-alcoholic fatty liver disease progression. Consilium 2019;21(8):93–7. (in Russian). DOI: 10.26442/20751753.2019.8.190503
- Chang Y., Noh Y.H., Suh B.S., Kim, et al. Bidirectional association between nonalcoholic fatty liver disease and gallstone disease: a cohort study. J. Clin. Med. 2018;7(11):458. DOI:10.3390/jcm7110458
- Malik A.A., Wani M.L., Tak S.I., Irshad I.et al. Association of dyslipidaemia with cholilithiasis and effect of cholecystectomy on the same. Int. J. Surg. 2011;9(8):641–2. DOI: 10.1016/j.ijsu.2011.08.003
- Honda A., Yoshida T., Tanaka N., Matsuzaki Y. et al. Increased bileacid concentration in liver tissue with cholesterol gallstone disease. Gastroenterol. 1995;30(1):61-6. DOI: 10.1007/BF01211376
- Ивашкин В.Т., Маевская М.В., Павлов Ч.С., Тихонов И.Н. и др. Клинические рекомендации по диагностике и лечению неалкогольной жировой болезни печени Российского общества по изучению печени и Российской гастроэнтерологической ассоциации. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(2):24– Ivashkin V.T., Mayevskaya M.V., Pavlov C.S., Tikhonov I.N. et al. Diagnostics and treatment of non-alcoholic fatty liver disease: clinical guidelines of the Russian Scientific Liver Society and the Russian gastroenterological association. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2016;26(2):24–42. (in Russian). DOI:10.22416/1382-4376-2016-26-2-24-42
- Комшилова К.А., Трошина Е.А. Ожирение и неалкогольная жировая болезнь печени: метаболические риски и их коррекция. Ожирение и метаболизм. 2015;12(2):35–9. Komshilova K.A., Troshina E.A. Obesity and nonalcoholic fatty liver disease: metabolic risks and their correction. Obesity and Metabolism. 2015;12(2):35– (in Russian). DOI: 10.14341/omet2015234-38
Цель исследования: оценить влияние коморбидных заболеваний на течение желчнокаменной болезни (ЖКБ) в сочетании с неалкогольной жировой болезнью печени (НАЖБП) или без нее, определить факторы, оказывающие наибольшее воздействие на эффективность терапии.
Дизайн: проспективное когортное исследование методом поперечного среза.
Материалы и методы. В исследование включены 114 пациентов с ЖКБ от 18 до 65 лет: 75 (65,8%) женщин и 39 (34,2%) мужчин (средний возраст — 48,4 ± 13,3 года). Пациенты разделены на две группы: в 1-ю вошли 65 больных с сочетанием ЖКБ и НАЖБП, во 2-ю — 49 человек только с ЖКБ, без НАЖБП. У всех пациентов выполнялись общеклинические, биохимические анализы крови, ультразвуковое исследование и мультиспиральная компьютерная томография брюшной полости, эластометрия печени, рассчитаны индекс фиброза (Fibrosis-4 и Aspartate Aminotransferase to Platelet Ratio Index) и индекс стеатоза (Fatty Liver Index). Все пациенты получали терапию урсодезоксихолевой кислотой (УДХК) в дозе 15 мг/кг в течение 1 года.
Результаты. В 1-й группе статистически значимо чаще, чем во 2-й, встречались патология сердечно-сосудистой системы, ожирение, инсулинорезистентность, были выше индекс коморбидности Cumulative Illness Rating Scale for Geriatrics (CIRS-G) (p < 0,001), показатели общего холестерина, триглицеридов, липопротеинов низкой плотности, γ-глутамилтранспептидазы, аспартатаминотрансферазы, аланинаминотрансферазы, амилазы, индекс Homeostasis model assessment (HOMA), индекс массы тела, окружность талии, преобладали желчные камни большой плотности и размеров. На фоне терапии УДХК эффективного литолиза удалось достигнуть у 34 (69,4% человек во 2-й группе, тогда как в 1-й — только у 22 (33,8%). Среди 57 пациентов без коморбидности эффективный литолиз произошел у 41 (70,2%), а среди 57 больных с высокой коморбидностью — только у 16 (28,1%) человек критерий χ2 Пирсона, р < 0,001). Регресса стеатоза достигли 40 (62%) пациентов с меньшим индексом коморбидности. На регресс стеатоза и литолиз желчных камней наибольшее влияние оказали индексы HOMA и CIRS-G, степень стеатоза, параметры желчного камня, ожирение.
Заключение. В амбулаторной практике есть возможности для своевременного консервативного лечения НАЖБП и ЖКБ при условии их ранней диагностики. Наличие отягощающих факторов и коморбидной патологии является препятствием для проведения литолиза желчных камней и регресса стеатоза. Воздействие на модифицируемые факторы риска помогает добиться успеха в терапии НАЖБП и ЖКБ.
Ключевые слова: желчнокаменная болезнь, коморбидность, литолиз, неалкогольная жировая болезнь печени
Скачать PDFУфимцева И.В., Яковлева С.В., Пирогова И.Ю. Влияние коморбидности на течение и эффективность лечения неалкогольной жировой болезни печени в сочетании с желчнокаменной болезнью. Вестник терапевта. 2023. № 3 (58) URL: https://journaltherapy.ru/statyi/vlijanie-komorbidnosti-na-techenie-i-jeffektivnost-lechenija-nealkogolnoj-zhirovoj-bolezni-pecheni-v-sochetanii-s-zhelchnokamennoj-boleznju/ (дата обращения: дд.мм.гггг)
Уфимцева Ирина Владимировна (автор для переписки) — врач-гастроэнтеролог ООО МЦ «Лотос», 454092, Россия, г. Челябинск, ул. Энгельса, 4. E-mail: ufimtsevaiv77@mail.ru
Яковлева София Васильевна — врач-кардиолог ООО МЦ «Лотос». 454092, Россия, г. Челябинск, ул. Энгельса, 4. E-mail: ysv9090831979@gmail.com
Пирогова Ирина Юрьевна — д. м. н., профессор кафедры общеврачебной практики РУДН. 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6. E-mail: irina_pirogova@inbox.ru
The effect of comorbidity on the course and effectiveness of treatment of non-alcoholic fatty liver disease in combination with cholelithiasis
I.V. Ufimtseva1, S.V. Yakovleva1, I.Yu. Pirogova2
1 Medical Center "Lotos"; 4 Engels Str., Chelyabinsk, Russian Federation 454092
2 Peoples' Friendship University of Russia named after Patrice Lumumba; 6 Miklukho-Maklay Str., Moscow, Russian Federation 117198
Abstract
Aim: to evaluate the impact of comorbid diseases on the course of cholelithiasis (GSD) in combination with non-alcoholic fatty liver disease (NAFLD) or without it, to determine the factors that have the greatest impact on the effectiveness of therapy.
Design: Prospective cross-sectional cohort study.
Materials and methods. The study included 114 patients with cholelithiasis from 18 to 65 years old: 75 (65.8%) women and 39 (34.2%) men (average age — 48.4 ± 13.3 years). The patients were divided into two groups: the 1st group included 65 patients with a combination of cholelithiasis and NAFLD, the 2nd group included 49 people with cholelithiasis only, without NAFLD. All patients underwent general clinical and biochemical blood tests, ultrasound and multislice computed tomography of the abdominal cavity, liver elastometry, and the fibrosis index (Fibrosis-4 and Aspartate Aminotransferase to Platelet Ratio Index) and steatosis index (Fatty Liver Index) were calculated. All patients received therapy with ursodeoxycholic acid (UDCA) at a dose of 15 mg/kg for 1 year.
Results. In group 1, pathology of the cardiovascular system, obesity, insulin resistance was statistically significantly more common than in group 2, the Cumulative Illness Rating Scale for Geriatrics (CIRS-G) comorbidity index was higher (p < 0.001), and total cholesterol levels were higher, triglycerides, low-density lipoproteins, γ-glutamyltranspeptidase, aspartate aminotransferase, alanine aminotransferase, amylase, Homeostasis model assessment (HOMA) index, body mass index, waist circumference, gallstones of large density and size predominated. During UDCA therapy, effective litholysis was achieved in 34 (69.4%) people in group 2, while in group 1 — only in 22 (33.8%). Among 57 patients without comorbidity, effective litholysis occurred in 41 (70.2%), and among 57 patients with high comorbidity — in only 16 (28.1%) people (Pearson χ2 test, p < 0.001). Regression of steatosis was achieved in 40 (62%) patients with a lower comorbidity index. The regression of steatosis and litholysis of gallstones was most influenced by the HOMA and CIRS-G indices, the degree of steatosis, gallstone parameters, and obesity.
Conclusion. In outpatient practice, there are opportunities for timely conservative treatment of NAFLD and cholelithiasis, provided they are diagnosed early. The presence of aggravating factors and comorbid pathology is an obstacle to litholysis of gallstones and regression of steatosis. Targeting modifiable risk factors helps achieve success in the treatment of NAFLD and cholelithiasis.
Keywords: non-alcoholic fatty liver disease, comorbidity, litholysis, cholelithiasis.
И.В. Уфимцева1, С.В. Яковлева1, И.Ю. Пирогова2
1 ООО Медицинский центр «Лотос»; Россия, г. Челябинск
2 ФГАОУ ВО «Российский университет дружбы народов имени Патриса Лумумбы»; Россия, г. Москва
Желчнокаменная болезнь (ЖКБ) — это хроническое заболевание, к которому существует генетическая предрасположенность, при нем происходит образование камней в желчных путях. ЖКБ относят к так называемым болезням цивилизации, поскольку она занимает третье место по частоте среди хронических заболеваний после сердечно-сосудистых болезней и сахарного диабета. В настоящее время ЖКБ широко распространена среди людей старше 40 лет (от 5 до 12% населения мира), а в группе лиц старше 50 лет заболеваемость возрастает уже в 2 раза (до 13–23%).
ЖКБ чаще всех остальных заболеваний желудочно-кишечного тракта становится причиной госпитализаций, это одна из болезней пищеварительной системы, которые приводят к наибольшим финансовым затратам систем здравоохранения [1].
В связи с ростом частоты ожирения в мире увеличивается и распространенность неалкогольной жировой болезни печени (НАЖБП), патогенетически связанной с ЖКБ. По результатам многих исследований, избыточная масса тела коррелирует с камнеобразованием и НАЖБП [2]. В основе литогенеза лежат нарушение липидного обмена, инсулинорезистентность, ожирение и НАЖБП.
Современные знания о механизмах образования камней в желчном пузыре базируются на результатах исследований, в которых доказано, что нестабильная литогенная желчь секретируется поврежденными гепатоцитами с последующей нуклеацией кристаллов моногидрата холестерина, кристаллизацией в муциновом матриксе на фоне гипомоторной дисфункции желчного пузыря. Эти данные положены в основу классификации ЖКБ, рекомендованной к применению в клинической практике на III съезде Научного общества гастроэнтерологов России, согласно которой выделяют четыре стадии течения ЖКБ [1–3]:
I стадия — начальная (предкаменная), включающая:
a) формирование густой неоднородной желчи;
b) образование билиарного сладжа (с наличием микролитов, замазкообразной желчи или сочетания замазкообразной желчи с микролитами);
II стадия — формирование желчных камней, которые различают:
a) по локализации: в желчном пузыре, в холедохе или в печеночных протоках;
b) по количеству: одиночные или множественные;
c) по составу: холестериновые, пигментные или смешанные;
d) по клиническому течению: латентное или с наличием клинических симптомов;
III стадия — хронический рецидивирующий калькулезный холецистит;
IV стадия — осложнения: водянка или эмпиема желчного пузыря, кальцификация стенки, абсцессы, прободение с развитием желчного перитонита, пузырно-кишечные и холедоходуоденальные свищи, прогрессирующая печеночная недостаточность, билиарный панкреатит и некроз поджелудочной железы, холангит, вторичный билиарный цирроз печени, рак желчного пузыря.
Еще в 1996 году U. Leuschner выделил три основных типа желчных камней: холестериновые, черные и коричневые пигментные камни (табл. 1).
Таблица 1. Характеристика желчных камней
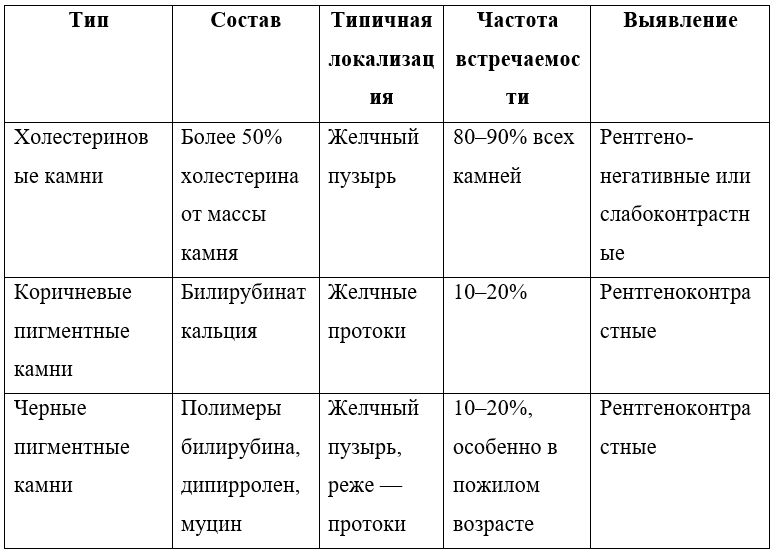
Пигментные камни чаще встречаются при хроническом гемолизе, бактериальной контаминации желчных путей, заболеваниях с поражением подвздошной кишки, наложении анастомозов, муковисцидозе, циррозе печени, синдроме Жильбера. Холестериновые камни наблюдаются у пациентов с метаболическим синдром, ожирением и инсулинорезистентностью и поддаются литолизу [2–4].
Процесс образования желчных камней при метаболическом синдроме и НАЖБП может быть запущен нарушением липидного обмена, окисления жирных кислот и усилением липогенеза [5]. При НАЖБП риск камнеобразования связан с повреждением гепатоцитов, снижением синтеза желчных кислот и секреции аполипопротеинов АI и AII [6]. Обнаружена связь ЖКБ с развитием сердечно-сосудистых и цереброваскулярных заболеваний у женщин в молодом возрасте [7, 8].
Наиболее распространенными факторами риска НАЖБП и ЖКБ признаны ожирение, инсулинорезистентность, сахарный диабет 2 типа, дислипидемия, артериальная гипертензия [9]. Выявлена прямая связь между ЖКБ и раком желчного пузыря, раком желудка, гепатоцеллюлярной карциномой, холангиокарциномой, раком поджелудочной железы, колоректальным раком [10], что делает особенно актуальными своевременную диагностику и лечение ЖКБ.
Установлено, что распространенность ЖКБ увеличивается по мере возрастания стадии фиброза печени: на стадии 0–II она составляет 15%, на стадии III — 29%, а на стадии IV (цирроз) — 56% [11], что подтверждает общность патогенеза этих заболеваний.
В условиях метаболических нарушений функционально измененные гепатоциты синтезируют неполноценные желчные мицеллы с повышенным содержанием в них холестерина и низким количеством фосфолипидов, что увеличивает литогенность желчи, усиливает выработку муцина стенкой желчного пузыря и повышает агрегацию микролитов желчи [12].
Согласно клиническим рекомендациям, основным методом диагностики ЖКБ и НАЖБП является ультразвуковое исследование (УЗИ) брюшной полости, чувствительность и специфичность которого составляют 60–94% и 88–95% соответственно и снижаются по мере увеличения индекса массы тела (ИМТ) и степени стеатоза [13].
Биохимические исследования крови у пациентов с ЖКБ и НАЖБП на начальных стадиях могут не обнаруживать никаких отклонений от нормы, но по мере прогрессирования заболеваний возможно развитие гипергликемии натощак, гипербилирубинемии, гиперхолестеринемии, гипертриглицеридемии, дислипидемии, повышаются уровни γ-глутамилтранспептидазы (ГГТП), щелочной фосфатазы [12]. Синдром цитолиза чаще свидетельствует о переходе НАЖБП в стадию стеатогепатита, но нормальные показатели трансаминаз не исключают воспалительных и фиброзных изменений в печени [14].
В настоящее время «золотым стандартом» диагностики фиброза и стеатоза печени остается пункционная биопсия, однако применение данного метода в широкой клинической практике ограничено. Для неинвазивной оценки фиброза и стеатоза печени у больных НАЖБП предложены различные расчетные формулы: Fibrosis-4 (FIB-4), Aspartate Aminotransferase to Platelet Ratio Index (APRI), Fatty Liver Index (FLI), Fibrotest и др. Из инструментальных неинвазивных методов диагностики НАЖБП широко используются эластография на аппарате FibroScan с измерением затухания ультразвуковой эховолны САP (Controlled Attenuation Parameter) и УЗИ-эластография сдвиговой волной системы Aixplorer, позволяющие определить степень фиброза и стеатоза печени.
Метод с высокими чувствительностью (до 95%) и специфичностью (90%) — мультиспиральная компьютерная томография (МСКТ) брюшной полости, позволяющая определить плотность печени и одновременно наличие сопутствующей патологии, в частности ЖКБ с оценкой размера и плотности желчного камня в единицах Хаунсфилда (HU) [15]. Методика МСКТ брюшной полости удобна при обследовании пациентов с сочетанием ЖКБ и НАЖБП, доступна и неинвазивна. МСКТ дает возможность определить параметры желчного камня, которые в дальнейшем будут учитываться при отборе пациентов на литолитическую терапию [3]. По рентгенологической плотности камни желчного пузыря делятся на рентгенонегативные (40–74 HU), слабоконтрастные (75–100 HU) и рентгенопозитивные (более 100 HU), а средняя плотность желчи — 10–15 HU.
Показаниями для консервативной терапии урсодезоксихолевой кислотой (УДХК) являются плотность желчного камня до 100 UH и диаметр до 10–15 мм при наличии единичных камней или заполнении ими менее 1/3 желчного пузыря [1, 2]. Камни плотностью более 100 UH и диаметром более 15 мм являются пигментными, или содержат билирубинат кальция, и плохо поддаются растворению [3]. Согласно нашим исследованиям, эффективность литолиза при правильной оценке показателей в ходе отбора пациентов может составлять 81,7% при лечении УДХК в дозе 15 мг/кг в течение 1 года [16].
Актуальность своевременной диагностики и лечения ЖКБ и НАЖБП подтверждается современными данными о последствиях холецистэктомии, которая не компенсирует сложные патофизиологические нарушения, имеющиеся при ЖКБ. После операции выпадает физиологическая роль желчного пузыря, нарушаются работа сфинктерного аппарата билиарного тракта и нейрогуморальная регуляция выделения желчи, а также повышается риск развития НАЖБП [17].
В настоящее время известно, что холецистэктомия изменяет метаболизм желчных кислот и влияет на обмен глюкозы и липидов в печени через фарнезоидные Х-рецепторы и G-белок-сцепленные рецепторы. После холецистэктомии понижается уровень фактора роста фибробластов, регулирующего синтез желчных кислот и липогенез в печени, который секретируется слизистой оболочкой желчного пузыря [18, 19], а также повышается пузырно-независимая энтерогепатическая циркуляция желчных кислот с образованием гидрофобной гепатотоксичной дезоксихолевой желчной кислоты и накоплением ее в печени с формированием морфологических изменений в виде неспецифического гепатита и холестаза [20].
Таким образом, мы видим, что холецистэктомия не избавляет больного от обменных нарушений, лежащих в основе заболевания. С учетом роста числа больных с коморбидной патологией и кардиометаболическими факторами риска становится все более актуальным консервативный подход к терапии ЖКБ и своевременному лечению НАЖБП.
Цель исследования: оценить влияние коморбидных заболеваний на течение ЖКБ в сочетании с НАЖБП и без нее, выявить факторы, оказывающие наибольшее воздействие на эффективность терапии.
Материалы и методы
В исследовании приняли участие 114 пациентов с ЖКБ от 18 до 65 лет: 75 (65,7%) женщин и 39 (34,3%) мужчин (средний возраст — 48,4 ± 13,3 года), наблюдавшиеся у гастроэнтеролога в Медицинском центре «Лотос» г. Челябинска с 2019 по 2022 год.
Критерии включения:
Критерии исключения:
Пациенты были разделены на две группы: в 1-ю вошли 65 больных с сочетанием ЖКБ и НАЖБП, во 2-ю — 49 человек только с ЖКБ, без НАЖБП.
У всех больных собран анамнез, измерены антропометрические параметры (рост, масса тела, ИМТ, окружность талии), выполнены общеклинические анализы крови и мочи, биохимический анализ крови: изучены активность аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ) и ГГТП, уровни общего и прямого билирубина, амилазы, глюкозы, инсулина, показатели липидограммы, индекс Homeostasis model assessment (НОМА).
Для определения степени фиброза и стеатоза печени рассчитаны индексы фиброза (FIB-4, APRI) и стеатоза печени (FLI). Для выявления ЖКБ и НАЖБП проводилось УЗИ брюшной полости, для характеристики рентгенологической плотности желчного камня и его размера, плотности печени, а также диагностики сопутствующих заболеваний — МСКТ брюшной полости. Эластометрия печени осуществлялась на аппарате FibroScan с датчиком XL.
НАЖБП диагностировали на основании следующих параметров: наличие жирового гепатоза по данным УЗИ брюшной полости; значение индекса FLI более 60; показатель плотности печени по результатам МСКТ менее 50 HU; значение САР-эластометрии печени более 200 dB/м. Все пациенты получали терапию препаратами УДХК в дозе 15 мг/кг в течение 1 года.
Статистическая обработка данных исследования выполнялась с помощью программы IBM SPSS Statistics 19. Данные представлены в виде медины (Me) и интерквартильного размаха [25%–75%]. Проверка нормальности распределения производилась с использованием критерия Шапиро — Уилка. Распределение в выборках не удовлетворяло требованиям параметрического анализа, поэтому для статистической обработки количественных данных были применены непараметрические методы (критерий Манна — Уитни). Различия считали статистически значимыми при p < 0,05. Для оценки различий использовался коэффициент корреляции Спирмена, для сравнения групп по признакам — χ2 Пирсона, для прогнозирования вероятности литолиза у пациентов с ЖКБ — метод логистической регрессии и анализ ROC-кривой.
Результаты
Анализ лабораторных данных показал статистически значимые различия между группами до и после терапии по активности АСТ, АЛТ, ГГТП, по уровням общего холестерина (ОХС), триглицеридов (ТГ), липопротеинов низкой плотности (ЛПНП), глюкозы, по индексу НОМА (критерий Манна — Уитни). После терапии различие в концентрации липопротеинов высокой плотности (ЛПВП) тоже стало значимым.
При сравнении параметров до и после терапии УДХК в обеих группах зафиксированы статистически значимые различия по активности АСТ, АЛТ, ГГТП, по концентрациям общего билирубина, амилазы, ОХС, ТГ, ПНП, ЛПВП, по индексу НОМА (критерий Уилкоксона), а во 2-й группе и по уровню глюкозы. Данные представлены в таблице 2.
Таблица 2. Биохимические показатели в группах исследования до и после терапии урсодезоксихолевой кислотой, Ме [25–75%]
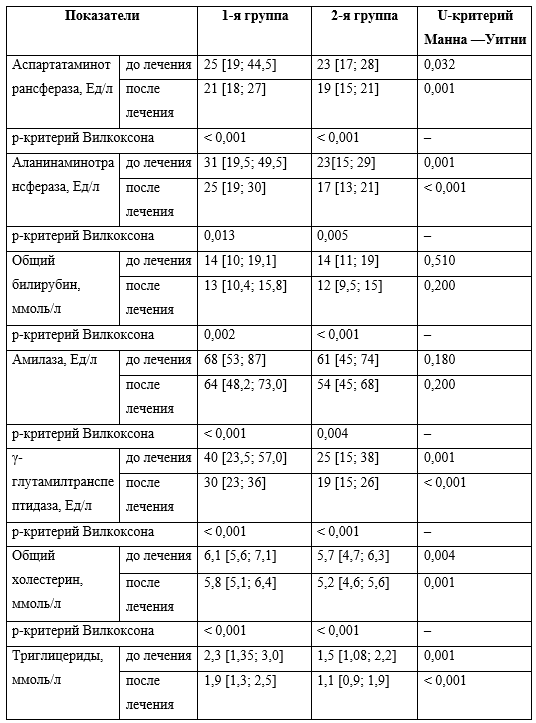
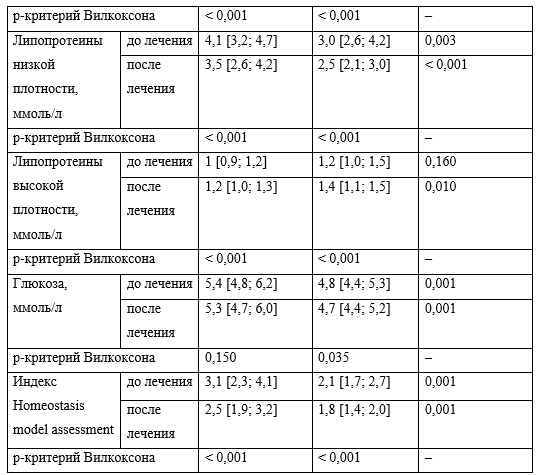
Таким образом, на фоне терапии УДХК мы наблюдали снижение биохимических показателей цитолиза, холестаза, нормализацию липидного и углеводного обменов.
Согласно данным УЗИ и МСКТ брюшной полости, в результате лечения размер желчных камней значимо уменьшился во 2-й группе (Ме снизилась от 7 до 0,1 мм), в 1-й группе динамика была незначительной (Ме — от 8,1 до 7,3 мм); р = 0,001. Плотность желчных камней на фоне терапии во 2-й группе также существенно уменьшались (Ме — от 85 до 35 HU); р = 0,002. Во 2-й группе чаще, чем в 1-й, встречались камни маленьких размеров (до 10 мм) и малой плотности: у 36 (73,5%) и 35 (53,8%) человек соответственно.
Показатели эластометрии печени значительно различались в группах: до лечения 1-й группе Ме = 305 dB/м, во 2-й группе Ме = 167 dB/м (р = 0,05). После терапии в 1-й группе снизилась до 243 dB/м (р < 0,001).
Эффективный литолиз (полное растворение желчных камней или уменьшение в 2 и более раз) наблюдался у 70,2% пациентов без коморбидности (индекс CIRS-G менее 7 баллов) и только у 28,1% больных с высокой коморбидностью (критерий χ2 Пирсона, р < 0,001). Это подтверждает неблагоприятное влияние сопутствующей патологии на эффективность консервативного лечения ЖКБ. Данные по сопряженности коморбидности и литолиза представлены в таблице 3.
Таблица 3. Показатели сопряженности коморбидности и эффективного литолиза, n (%)
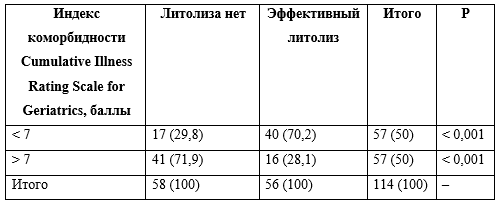
Выявлено, что у пациентов с высоким индексом коморбидности плотность камней была больше, чем у лиц без коморбидности (25 (50,9%) и 14 (28,8%) человек соответственно, р < 0,001), отмечен более высокий индекс НОМА (33 (66,7%) и 14 (29,8%) пациентов соответственно, р = 0,023), чаще диагностирована НАЖБП (у 37 (75,4%) и 19 (38,6%) больных соответственно, р = 0,001).
При оценке коморбидной патологии у пациентов с регрессом стеатоза и без него определено влияние эндокринных заболеваний (ЭЗ) на эффективность лечения НАЖБП: у больных без ЭЗ регресс стеатоза достигнут у 82,5% пациентов, при наличии ЭЗ — всего у 17,5%р < 0,05).
Анализ результатов литолитической терапии показал, что больные с удавшимся литолизом были статистически значимо моложе (Ме = 45 лет против 52,5 года), у них оказались меньше размеры (Ме = 5 мм) и плотность желчных камней (Ме = 69,5 HU, р = 0,021), реже встречалась инсулинорезистентность (Ме индекса НОМА = 2).
У пациентов без коморбидности отмечены более низкие индекс FLI (Ме = 41 против 59,5, р = 0,022), показатели cтеатоза печени (Ме = 213 против 306 dB/м, р = 0,005).
Из вышеизложенного следует, что наибольшее значение для достижения эффективного литолиза имели индекс НОМА, параметры желчного камня, индекс коморбидности CIRS-G, степень стеатоза печени. Факторы, влиявшие на регресс стеатоза, — индекс FLI, уровень глюкозы в крови, ИМТ, окружность талии.
Терапия УДХК была успешной (при полном растворении или уменьшении размеров камней более чем в 2 раза) у 34 (69,4%) пациентов ез НАЖБП и только у 21 (32,3%) — с НАЖБП, р = 0,001.
Регресс стеатоза на фоне терапии УДХК в течение 12 месяцев достигнут у 31 (63,2%) человека без коморбидности.
Таким образом, мы выявили модифицируемые факторы риска, оказывающие влияние на эффективность терапии НАЖБП и ЖКБ, — индекс НОМА, ИМТ, окружность талии, степень стеатоза — воздействуя на которые, возможно достичь лучших результатов лечения.
Клиническое наблюдение
Пациентка Н., 1987 г. р., обратилась в Медицинский центр «Лотос» г. жалобами на приступообразные острые боли в правом подреберье через 30 минут после еды, тошноту, запоры в течение 3–4 дней. В анамнезе хронические заболевания отсутствовали. Общее состояние удовлетворительное, кожа чистая. Дыхание везикулярное, хрипов не было. Тоны сердца ритмичные, частота сердечных сокращений — 68 в минуту, артериальное давление — 110/70 мм рт. ст. Живот мягкий, болезненный в правом и левом подреберье, печень не увеличена, по Курлову — 10/10/9 см, не выступала из-под реберной дуги. Живот вздут, слышалось урчание. Стул 1 раз в 3–4 дня. ИМТ — 21 кг/м2. Индекс коморбидности Чарльсона — 0 баллов, CIRS-G — 1 балл.
Из обследования: показатели общего анализа крови — без изменений, активность АСТ — 25 ЕД/л, АЛТ — 19 ЕД/л, уровень общего билирубина — 15 ммоль/л, глюкозы— 4,5 ммоль/л, ОХС — 4,5 ммоль/л, ЛПНП — 2,4 ммоль/л, ЛПВП — 1,6 ммоль/л, ТГ — 0,98 ммоль/л, индекс НОМА — 0,96. Имелись МСКТ-признаки хронического калькулезного холецистита, мелких камней желчного пузыря (до 53 ед.) диаметром 3 мм.
Пациентке назначено лечение, включавшее спазмолитики, пробиотики, лактулозу, на 4 недели и препарат УДХК в дозе 15 мг/ кг сроком на 12 месяцев. Симптоматика была купирована в течение 2 недель, но терапия УДХК продолжена до полного растворения камней, в данном случае — 6 месяцев.
Показатели после лечения: активность АСТ — 17 ЕД/л, АЛТ — 15 ЕД/л, уровень общего билирубина — 9 ммоль/л, глюкозы — 4,3 ммоль/л, ОХС — 3,5 ммоль/л, ЛПНП — 1,9 ммоль/л, ЛПВП — 1,7 ммоль/л, ТГ — 0,86 ммоль/л. В ходе МСКТ через 6 месяцев терапии УДХК рентгенпозитивные камни не обнаружены (рис.)
А 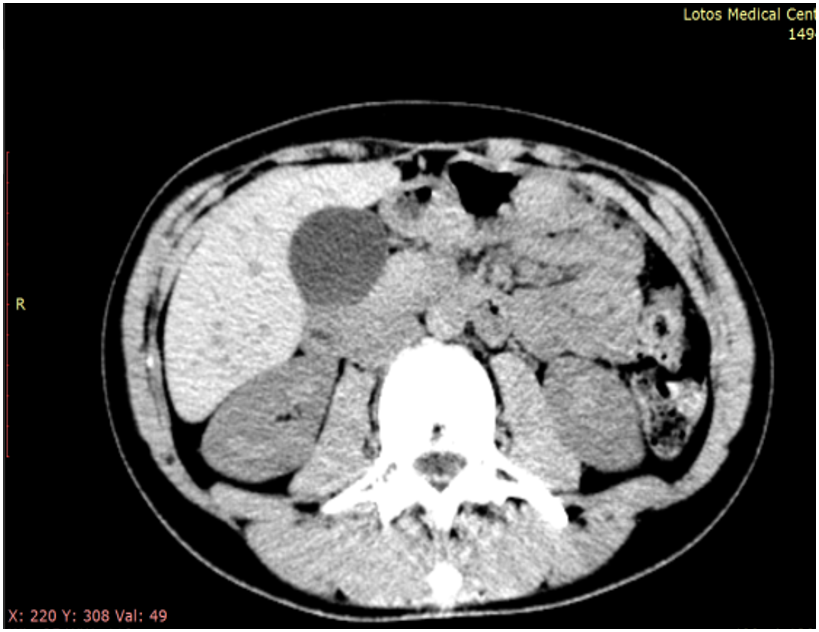
В 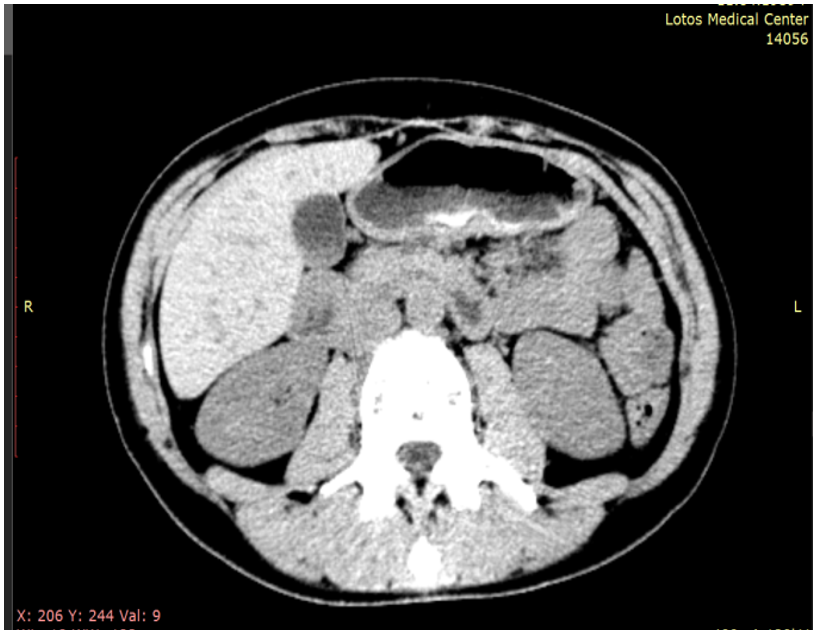
Рис. Мультиспиральная компьютерная томограмма пациентки Н. A — до лечения: слабоконтрастные (50–65 HU) и мелкие желчные камни (до 4 мм). В — после лечения: желчные камни отсутствуют, желчь однородная (15 HU). Иллюстрация авторов
Данный клинический пример демонстрирует эффективность проведения литолитической терапии у больной без отягощающей сопутствующей патологии и НАЖБП.
Обсуждение
Результаты нашего исследования показывают, что у пациентов с коморбидностью и НАЖБП можно выделить следующие особенности течения ЖКБ: бóльшие плотность и размеры желчных камней, чем у больных только с ЖКБ и без коморбидности, выше индекс стеатоза печени, чаще отмечаются инсулинорезистентность, дислипидемия, нарушение гликемии натощак, как правило, у них больше ИМТ и окружность талии, что косвенно может указывать на висцеральное ожирение, которое является предиктором кардиометаболических факторов риска и НАЖБП у больных с ЖКБ. Терапия УДХК у таких пациентов помогает скорректировать показатели цитолиза, холестаза, липидограммы и индекса НОМА, но практически не влияет на растворение желчных камней.
Нами выявлены факторы, влияющие на успешность литолитической терапии (индекс НОМА, индекс коморбидности CIRS-G, параметры желчного камня по данным МСКТ), а также регресса стеатоза (индекс FLI, ИМТ, окружность талии уровень глюкозы в крови). Из ранее проведенных исследований известно, что условиями для осуществления успешной литолитической терапии являются низкая плотность желчных камней (менее 100 HU) и размер не более 10 мм, сохранение сократительной способности желчного пузыря, наполнение камнями не более 2/3 объема желчного пузыря. Эти данные подтверждены и в нашем исследовании, но влияние коморбидности на эффективность литолитической терапии ранее оценено не было. При правильном определении предикторов эффективности терапии растворение желчных камней может составить 2,86 мма 3 месяца у 85% лиц с ЖКБ [3]. В нашем исследовании литолиз был эффективным значительно чаще у пациентов без коморбидности, чем у больных с высокой коморбидностью. Это подтверждает отягощающее влияние сопутствующей патологии на процесс растворения желчных камней.
Эффективность терапии НАЖБП также зависит от степени стеатоза печени: чем ниже степень стеатоза и индекс FLI, тем лучше результат лечения.
Применение УДХК позволило произвести литолиз желчных камней, добиться регресса стеатоза печени и положительно повлиять на метаболизм в целом (улучшить показатели липидного и углеводного обменов). Фармакологические эффекты УДХК связаны с ее способностью снижать насыщение желчи холестерином за счет подавления его кишечной абсорбции и реабсорбции, угнетения синтеза в печени и уменьшения секреции в желчь. УДХК снижает всасывание гидрофобных эндогенных желчных кислот из тонкой кишки, растворяет их соли и усиливает выделение желчи, в целом оказывает многофакторное действие на состояние гепатобилиарной системы и метаболизм [21].
Известно также, что препараты УДХК обладают плейотропным влиянием на липидный обмен: увеличивается уровень ЛПВП и снижаются содержание ЛПНП, активность АЛТ, АСТ и ГГТ, степени стеатоза и фиброза печени [22].
Международное многоцентровое исследование «Успех», показало, что монотерапия УДХК у коморбидных пациентов с НАЖБП значимо уменьшает гепатологические (биохимические показатели цитолиза и холестаза, степени стеатоза и фиброза) и сердечно-сосудистые риски (уровни ЛПНП, ТГ, толщину комплекса интима-медиа в сочетании с повышением концентрации ЛПВП) [21].
Заключение
В амбулаторной практике есть возможности для своевременного консервативногоечения НАЖБП и ЖКБ при условии их ранней диагностики. Наличие отягощающих факторов и коморбидной патологии является препятствием для проведения литолиза желчных камней и регресса стеатоза. Воздействие на модифицируемые факторы риска помогает добиться успеха в терапии НАЖБП и ЖКБ.
Предыдущая статья
Н.В. Болотова, М.С. Белоусова, К.А. Чередникова, Н.Ю. Филина, В.К. Поляков, А.П. Аверьянов ФГБОУ ...
Следующая статья
М.А. Харитонов, Н.А. Варавин, В.П. Кицышин, Ю.Б. Говердовский, А.А. Сантаков ФГБВОУ ВО «Военно-ме...