Роль кишечной микробиоты в развитии метаболических нарушений
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Затевалов А.М., Безродный С.Л., Марданлы С.Г., Помазанов В.В. Оценка степени тяжести сахарного диабета 2 типа методом микробиом-ассоциированной экспосомики у пациентов с нарушениями углеводного и липидного обмена. Известия ГГТУ. Медицина, фармация. 2021;(4):43–53. Zatevalov A.M., Bezrodny S.L., Mardanly S.G., Pomazanov V.V. Evaluation of the severity of type 2 diabetes mellitus by microbiome-associated exposomes in patients with disorders of carbohydrate and lipid metabolism. Izvestiya GSTU. Medicine, pharmacy. 2021;(4):43–53. (in Russian). EDN: JKPGAE
- Звенигородская Л.А., Шинкин М.В., Мкртумян А.М. и др. Роль печени и микрофлоры желудочно-кишечного тракта в патогенезе сахарного диабета 2 типа и ожирения. Эффективная фармакотерапия. 2020;16(36):34–45. Zvenigorodskaya L.A., Shinkin M.V., Mkrtumyan A.M. et al. The role of the liver and microflora of the gastrointestinal tract in the pathogenesis of type 2 diabetes mellitus and obesity. Effective pharmacotherapy. 2020;16(36):34–45. (in Russian). DOI 10.33978/2307-3586-2020-16-36-32-42. EDN HNEKQV
- Бондаренко О.А., Сорочка М.И. Метаболический тандем: неалкогольная жировая болезнь печени и стеатоз поджелудочной железы; терапевтическая значимость пробиотиков (клинический случай). Вестник клуба панкреатологов. 2020;(3):54–69. Bondarenko O.A., Sorochka M.I. Metabolic tandem: non-alcoholic fatty liver disease and pancreatic steatosis; therapeutic significance of probiotics (clinical case). Bulletin of the club of pancreatologists. 2020;(3):54–69. (in Russian). EDN ZYKGHK
- Буйваленко А.В., Покровская Е.В. Взаимодействие микробиома кишечника и пероральных сахароснижающих препаратов: обзор литератур. Проблемы эндокринологии. 2022;68(2):66–71. Buyvalenko A.V., Pokrovskaya E.V. Interaction of the intestinal microbiome and oral hypoglycemic drugs: a review of the literature. Problems of Endocrinology. 2022;68(2):66–71. (in Russian). DOI: 10.14341/probl12835. EDN TZRUDM
- Плотникова Е.Ю. Микробный пейзаж кишечника и метаболический синдром — что общего? Вестник клуба панкреатологов. 2016;(2):63–72. Plotnikova, E.Yu. Microbial landscape of the intestine and metabolic syndrome — what do they have in common? Bulletin of the club of pancreatologists. 2016;(2):63–72. (in Russian). EDN WHTFWT
- Zheng Y., Ley S., Hu F. Global aetiology and epidemiology of type 2 diabetes mellitus and its complications. Nat. Rev. Endocrinol. 2018;14:88–98. Doi: 10.1038/nrendo.2017.151
- Zhang Y., Lin C., Chen R. et al. Association analysis of SOCS3, JAK2 and STAT3 gene polymorphisms and genetic susceptibility to type 2 diabetes mellitus in Chinese population. Diabetol. Metab. Syndr. 2022;14(1):4. Doi: 10.1186/s13098-021-00774-w
- Berg G., Rybakova D., Fischer D. et al. Microbiome definition re-visited: old concepts and new challenges. Microbiome. 2020;8(1):103. Doi: 10.1186/s40168-020-00875-0
- Hillman E.T., Lu H., Yao T., Nakatsu C.H. Microbial ecology along the gastrointestinal tract. Microbes Environ. 2017;32:300–313. Doi: 10.1264/jsme2.ME17017
- Fan Y., Pedersen O. Gut microbiota in human metabolic health and disease. Nat. Rev. Microbiol. 2021;19:55–71. Doi: 10.1038/s41579-020-0433-9
Изъятие статьи произведено по запросу авторов в связи с неверным указанием списка лиц, принимавших участие в написании статьи.
Авторы:
П.А. Чижков1, C.Н. Лагутина2, В.Н. Попов1, М.Ю. Сыромятников1, А.А. Зуйкова2, О.С. Скуратова2
2 ФГБОУ ВО «Воронежский государственный медицинский университет имени Н.Н. Бурденко» Минздрава России; Российская Федерация, г. Воронеж
Цель исследования: оценка биоразнообразия кишечной микробиоты у пациентов с метаболическими нарушениями (сахарный диабет 2 типа, ожирение различной степени тяжести).
Дизайн: сравнительное исследование.
Материалы и методы. В исследовании приняли участие 20 человек, средний возраст которых составил 56,0 ± 2,5 года. Было проведено 16s-РНК-секвенирование кала для оценки биоразнообразия кишечной микробиоты.
Результаты. Выявлено достоверное увеличение числа представителей микробиоты «метаболического» кластера, таких как Roseburia, Holdemanella, Subdoligranulum, Christensenellaceae R-7, способных напрямую влиять на липидный и углеводный обмены за счёт увеличенной продукции активных метаболитов. Они воздействуют на процесс глюконеогенеза, изменяя чувствительность к инсулину ещё на латентной стадии заболевания по сравнению с группой контроля. Помимо этого отмечено значительное увеличение числа патогенных бактерий (Clostridium sensu stricto) и уменьшение количества представителей нормофлоры (Bifidobacterium, Lactobacterium), дисбаланс между которыми способен отягощать течение патологического процесса основного заболевания.
Заключение. Изменение соотношения различных представителей микробиоты кишечника может служить диагностическим признаком метаболических нарушений и способствовать своевременному лечению данной патологии, улучшению качества жизни пациентов.
Ключевые слова: диагностика, микробиота кишечника, ожирение, сахарный диабет 2 типа, скрининг
Скачать PDFЧижков П.А., Лагутина C.Н., Попов В.Н., Сыромятников М.Ю., Зуйкова А.А., Скуратова О.С. Роль кишечной микробиоты в развитии метаболических нарушений. Вестник терапевта. 2023; 2(57). URL: https://journaltherapy.ru/statyi/rol-kishechnoj-mikrobioty-v-razvitii-metabolicheskih-narushenij/ (дата обращения: дд.мм.гг.)
Чижков Павел Андреевич (автор для переписки) — аспирант кафедры генетики, цитологии и биоинженерии; ФГБОУ ВО «Воронежский государственный университет». 394018, Россия, г. Воронеж, Университетская площадь, д. 1; eLIBRARY.RU SPIN: 5108-3444. https://orcid.org/0000-0002-5626-0579. E-mail: qooleer@yandex.ru
Лагутина Светлана Николаевна — ординатор кафедры поликлинической терапии; ФГБОУ ВО «Воронежский государственный медицинский университет им. Н.Н. Бурденко». 394036, Россия, г. Воронеж, ул. Студенческая, д. 10. eLIBRARY.RU SPIN: 3165-2380. https://orcid.org/0000-0003-3730-5265. E-mail: svlagutina97@mail.ru
Попов Василий Николаевич — д. м. н., профессор, заведующий кафедрой генетики, цитологии и биоинженерии; ФГБОУ ВО «Воронежский государственный университет». 394018, Россия, г. Воронеж, Университетская пл., д. 1. eLIBRARY.RU SPIN: 7257-5052. https://orcid.org/0000-0003-1294-8686. E-mail: pvn@mail.ru
Сыромятников Михаил Юрьевич — к. б. н., доцент, ведущий научный сотрудник лаборатории метагеномики и пищевых биотехнологий; ФГБОУ ВО «Воронежский государственный университет». 394018, Россия, г. Воронеж, Университетская пл., д. 1. eLIBRARY.RU SPIN: 7321-3642. https://orcid.org/0000-0001-9028-0613. E-mail: mihan.vrn@mail.ru
Зуйкова Анна Александровна — д. м. н., профессор, заведующая кафедрой поликлинической терапии; ФГБОУ ВО «Воронежский государственный медицинский университет им. Н.Н. Бурденко». 394036, Россия, г. Воронеж, ул. Студенческая, д. 10. eLIBRARY.RU SPIN: 7605-1630. https://orcid.org/0000-0002-5378-4959. E-mail: zuikova@vrngmu.ru
Скуратова Ольга Сергеевна — ординатор кафедры поликлинической терапии; ФГБОУ ВО «Воронежский государственный медицинский университет им. Н.Н. Бурденко». 394036, Россия, г. Воронеж, ул. Студенческая, д. 10. eLIBRARY.RU SPIN: 5178-7940. https://orcid.org/0000-0002-1471-8967. E-mail: prokopova15@mail.ru
The role of the intestinal microbiota in the development of metabolic disorders
P.A. Chizhkov1, S.N. Lagutina2, V.N. Popov1, M.Yu. Syromyatnikov1, A.A. Zuikova2, O.S. Skuratova2
1 Voronezh State University; 1 Universitetskaya sqr., Voronezh, Russian Federation 394018
2 Voronezh State Medical University named after N.N. Burdenko of the Ministry of Health of Russia; 10 Studencheskaya Str., Voronezh, Russian Federation 394036
The purpose of the study: to assess the biodiversity of the intestinal microbiota in patients with metabolic disorders (type 2 diabetes mellitus, obesity of varying severity).
Design: comparative study.
Materials and methods. The study involved 20 people, whose average age was 56.0 ± 2.5 years. Fecal 16S-RNA sequencing was performed to assess the biodiversity of the gut microbiota.
Results. A significant increase in the number of representatives of the microbiota of the «metabolic» cluster, such as Roseburia, Holdemanella, Subdoligranulum, Christensenellaceae R-7, was revealed, which can directly affect lipid and carbohydrate metabolism due to increased production of active metabolites. They affect the process of gluconeogenesis, changing insulin sensitivity even at the latent stage of the disease compared with the control group. In addition, there was a significant increase in the number of pathogenic bacteria (Clostridium sensu stricto) and a decrease in the number of representatives of the normoflora (Bifidobacterium, Lactobacterium), the imbalance between which can aggravate the course of the pathological process of the underlying disease.
Conclusion. A change in the ratio of various representatives of the intestinal microbiota can serve as a diagnostic sign of metabolic disorders and contribute to the timely treatment of this pathology and improve the quality of life of patients.
Keywords: gut microbiota, type 2 diabetes mellitus, obesity, diagnosis, screening
П.А. Чижков1, C.Н. Лагутина2, В.Н. Попов1, М.Ю. Сыромятников1, А.А. Зуйкова2, О.С. Скуратова2
1 ФГБОУ ВО «Воронежский государственный университет»; Российская Федерация, г. Воронеж
2 ФГБОУ ВО «Воронежский государственный медицинский университет имени Н.Н. Бурденко» Минздрава России; Российская Федерация, г. Воронеж
Рост неинфекционной патологии в структуре общей заболеваемости занимает лидирующие позиции во всём мире. Сахарный диабет 2 типа, ожирение различной степени тяжести входят в тройку заболеваний, приводящих к ранней инвалидизации населения за счёт развивающихся осложнений (инсульт, хроническая болезнь почек, острый коронарный синдром, хроническая сердечная недостаточность). Более 300 млн человек имеют в анамнезе данную патологию, что оставляет актуальным поиск новых диагностических маркеров, способных выявить изменения на латентной стадии. Проведение глюкозотолерантного теста, изучение лабораторных показателей (общий холестерин, липопротеиды низкой и очень низкой плотности, глюкоза, гликированный гемоглобин) позволяет определить тенденцию к росту уже на поздних стадиях заболевания, когда появляется клиническая симптоматика [1]. Установлена важная роль кишечной микробиоты в формировании патологического процесса. Это связано с активной выработкой короткоцепочечных жирных кислот, таких как ацетат, пропионат, сукцинат, бутират, в избыточном количестве, что увеличивает синтез активных форм кислорода и провоцирует развитие окислительного стресса. Бутират-ацетоацетат-КоА-трансфераза, участвующая в метаболизме бутирата, была обнаружена в более высоких концентрациях у взрослых с ожирением. Увеличение уровня данного фермента у пациентов с избыточным весом предполагает, что бутират может участвовать в накоплении энергии, которая нарушает процесс липогенеза и приводит к изменению фракций липопротеидов, триглицеридов [2–4]. Помимо этого нарушается и промежуточная стадия метаболизма простых сахаров, что способствует стремительному развитию сахарного диабета 2 типа. Изменение численности родового и видового состава кишечной микробиоты происходит ещё на латентной стадии и может служить ранним диагностическим признаком метаболических нарушений, напрямую влияющих на течение и исход основного заболевания, а также указывать на необходимость коррекции терапии (метаболиты бактерий способны влиять на синтез дипептидаз (дипептидилпептидазы-1,4, глюкагоноподобного пептида-1), ингибиторами которых являются современные сахароснижающие препараты) [5–7].
Цель работы — оценка биоразнообразия кишечной микробиоты у пациентов с сахарным диабетом 2 типа, ожирением различной степени тяжести.
Дизайн: сравнительное исследование.
Материалы и методы
В исследовании приняли участие 20 человек, средний возраст которых составил 56,0 ± 2,5 года. Первый этап представлял собой анкетирование, включавшее вопросы о возрасте, питании, физической активности, наличии в анамнезе инфекционной и неинфекционной патологии, приеме лекарственных препаратов, в том числе гормональных и антибактериальных (за последние 6 мес). Также определялись антропометрические показатели (рост, вес с последующим расчетом индекса массы тела (ИМТ), окружность талии (ОТ). Всем пациентам был проведен биохимический анализ крови с определением уровня общего холестерина, липопротеидов низкой и высокой плотности, триглицеридов, коэффициента атерогенности, глюкозы, гликированного гемоглобина. На основании этих данных пациенты были разделены на две группы: 1-я группа — соматически здоровые без признаков метаболических нарушений (10 человек — 4 мужчины и 6 женщин); 2-я группа — пациенты с сахарным диабетом 2 типа и ожирением (10 человек — 3 мужчины и 7 женщин). Среди пациентов 2-й группы у 3 больных диагностировано ожирение 1 степени (30,0 < ИМТ < 34,9 кг/м2), у 5 — ожирение 2-й степени (35,0 < ИМТ < 39,9 кг/м2; ОТ > 102 см у мужчин, ОТ > 84 см у женщин). Для включения в исследование все пациенты подписали информированное добровольное согласие, одобренное локальным этическим комитетом ФГБОУ ВО «Воронежский государственный университет». Был произведен забор материала (кала) в стерильную емкость для последующей оценки биоразнообразия кишечной микробиоты (методом 16S-РНК-секвенирования) в лаборатории прикладных геномных технологий ФГБОУ ВО «Воронежский государственный университет инженерных технологий». Исследование проводилось согласно протоколу с помощью секвенатора (Zymo Research, США). Область V3 гена 16S-РНК была выбрана для подготовки библиотеки и дальнейшего секвенирования с использованием платформы Ion Torrent PGM, универсальных праймеров 337-F (50-GAC-TCC-TAC-GGG-AGG-CWG-CAG-30) и 518-R (50-GTA-TTA-CCG-CGG-CTG-CTG-30) и набора 5X ScreenMix-HS Master Mix Kit (Россия). После этого продукты ПЦР очищали с использованием магнитных частиц и приступали непосредственно к приготовлению библиотек для секвенирования. Затем была проведена статистическая обработка полученных данных методом прямого моделирования. Результаты выражали как среднее ± стандартная ошибка среднего (SEM). Альфа-разнообразие для каждой группы рассчитывали с использованием индекса Шеннона, достоверно значимым считали значение р < 0,05.
Результаты
По результатам анкетирования было выявлено, что за последние 6 мес пациенты не принимали антибактериальные и гормональные препараты. У 12 (67%) пациентов отмечалась низкая физическая активность. Из сопутствующих заболеваний у 4 (22%) человек была диагностирована артериальная гипертензия. Результаты лабораторного исследования крови пациентов приведены в табл. 1.
Таблица 1 / Table 1
Показатели биохимического анализа крови пациентов
Indicators of biochemical analysis of blood of patients
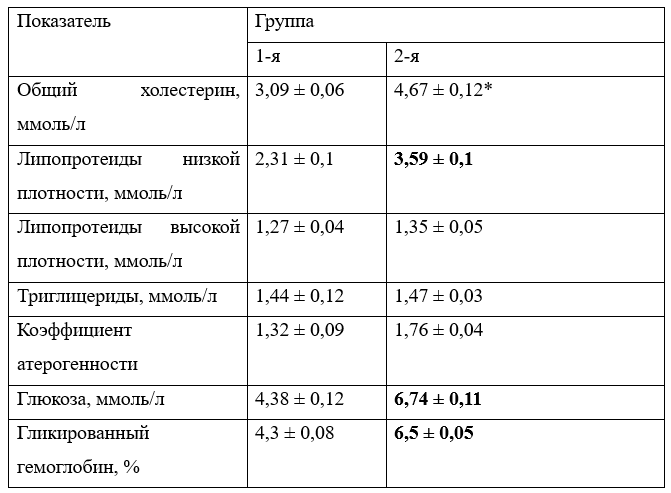
Примечание. *Пациенты получали гиполипидемическую терапию (статины) в течение последних 12 мес.
Затем были изучены особенности родового разнообразия кишечной микробиоты у соматически здоровых пациентов и больных с сахарным диабетом 2 типа и ожирением. У больных с ожирением статистически достоверно (р < 0,026) увеличивалось содержание бактерий рода Faecalibacterium (на 29,5%), которые являются важным членом микробиоты кишечника человека, основным производителем бутирата, противовоспалительного и иммуномодулирующего метаболита других полезных бактерий. Увеличение представителей этих бактерий связано с избыточной массой тела, ожирением и возможными нарушениями обмена веществ из-за способности лучше усваивать энергию из пищи. Склонность бактерии к размножению определяет устойчивость к метаболическим нарушениям и изменения на ранней стадии заболевания.
У пациентов 2-й группы по сравнению с 1-й группой было увеличено число представителей рода Roseburia (на 3,2%; p < 0,01). Представители рода Ruminococcus являются основными деструкторами муцина, изменяющими состав слизи, что помогает быстрому развитию защитного эффекта от воспалительных и метаболических нарушений. Ruminococcus — бактерия, проникающая в кишечник и обладающая способностью ферментировать сложные углеводы, а также продуцировать ацетат и пропионат, является представителем нормальной микрофлоры кишечника. Снижение ее численного состава может свидетельствовать о развитии патологических нарушений. Во 2-й группе уровень этих бактерий стойко снижался (до 0,25%; р < 0,004) по сравнению с 1-й группой (2,6%), но увеличивалось число бактерий рода Catenibacterium (3,05%; р < 0,02). Представители данного рода используют глюкозу для образования уксусной, молочной, масляной и изомасляной кислот. Высокое количество Catenibacterium может быть связано с повышенной проницаемостью кишечника и развитием метаболических нарушений. Помимо представителей нормальной кишечной флоры статистически значимые изменения произошли среди патогенного кластера бактерий — увеличение представителей рода Clostridium sensu stricto (2,21%; р < 0,01). Этот род бактерий играет важную роль в регуляции перистальтики кишечника и секреции эпителия. Недавние исследования показали, что местная кишечная микробиота модулирует передачу сигналов и использует сенсорные рецепторы для обнаружения пищевых и микробиотических сигналов из просвета для последующей передачи информации в центральную нервную систему. Clostridium, увеличивая проницаемость кишечника, может способствовать ожирению, вызванному диетой с высоким содержанием жиров.
Содержание бактерий рода Holdemanella увеличилось до 1,93% (p < 0,007). В некоторых исследованиях высокий уровень бактерий рода Holdemanella связывают с нарушением обмена веществ, нездоровым липидным профилем сыворотки крови, что может способствовать увеличению образования общего холестерина и липопротеидов низкой и очень низкой плотности [6].
Уровень бактерий рода Subdoligranulum — продуцентов бутирата — положительно коррелировал с бактериальным разнообразием микробиоты, а также с уровнями холестерина и липопротеидов высокой плотности и с показателями чувствительности к инсулину. Отмечено статистически значимое изменение количества бактерий этого рода (р < 0,01%) с 1,56% в 1-й группе до 6,23% во 2-й группе, что может свидетельствовать о нарушении липидного и углеводного обменов. Отмечалось статистически значимое увеличение бактерий рода Megasphaera (3,4%), которые являются частью микрофлоры толстой кишки человека. В процессе жизнедеятельности они способны продуцировать короткоцепочечные жирные кислоты: масляную, изомасляную, валериановую, капроновую, изовалериановую, изокапроновую, входящие в состав нормальной микрофлоры кишечника. Эта бактерия способна утилизировать лактат и производить полезный бутират. Лактат вырабатывается микробами, колонизирующими кишечник человека, как конечный продукт ферментации углеводов, редко встречается в нормальных условиях, т.к. быстро превращается другими бактериями в полезные жирные кислоты.
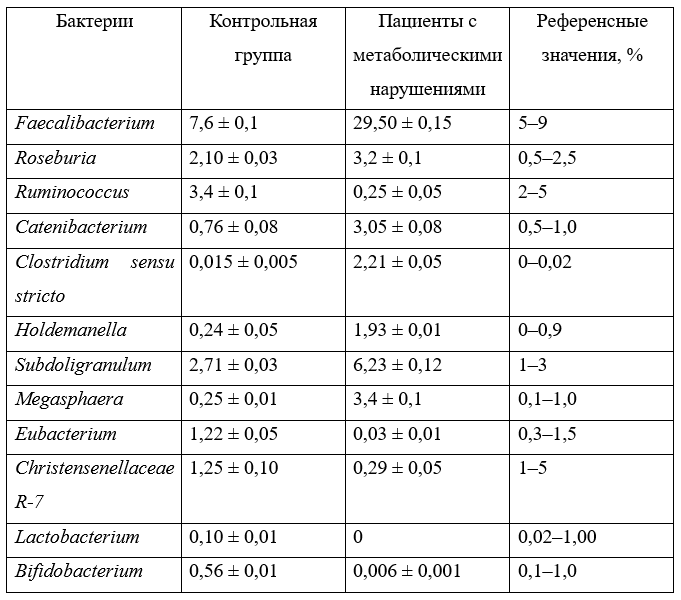
У пациентов 2-й группы было достоверно значимо (р < 0,02) увеличено число бактерий рода Eubacterium — типичного представителя нормальной микрофлоры кишечника человека — 0,03%, что в несколько раз ниже, чем в 1-й группе (1,22%). Это может быть связано с более медленным углеводным обменом у пациентов с ожирением, вызывает дальнейшее увеличение массы тела. Некоторые виды бактерий способны превращать холестерин в копростерин и тем самым участвовать в деконъюгации желчных кислот. Помимо этого, данный род метаболизирует углеводы и пептоны с накоплением органических кислот, используемых энтероцитами в основных процессах метаболизма. Большинство бактерий рода Eubacterium способны ферментировать углеводы в избытке с накоплением смеси короткоцепочечных жирных кислот. Наряду с этим отмечалось изменение численности Christensenellaceae R-7 типа, которая отвечает за развитие абдоминального ожирения у людей, причем большее влияние наблюдается у пожилых пациентов. Разница во 2-й (0,29%) и 1-й (1,25%) группах была статистически значимой (p < 0,04), что подтверждает данные других исследований о зависимости уровня бактерий этого рода от избыточной массы тела. Стоит отметить достоверное снижение представителей нормофлоры (Bifidobacterium, Lactobacterium) у пациентов с метаболическими нарушениями до полного отсутствия или крайне низкого значения (р < 0,01%). Показатели родового биоразнообразия микробиоты кишечника у исследуемых групп представлены в табл. 2.
Таблица 2 / Table 2
Показатели родового биоразнообразия микробиоты кишечника у исследуемых групп
Indicators of the generic biodiversity of the intestinal microbiota in the studied groups
Обсуждение
Высокая представленность вышеперечисленных бактерий, выявленных при секвенировании, может настораживать в отношении развития метаболических заболеваний. Повышенное значение может свидетельствовать о риске развития метаболического синдрома и сахарного диабета 2 типа. Данное бактериальное распределение может ассоциироваться с метаболическими нарушениями, а также связано с избыточным весом за счет способности бактерий из типа Firmicutes лучше поглощать энергию из пищи, синтезируя бутират, важнейший бактериальный метаболит, который стимулирует образование кишечного серотонина, и этот периферический источник является регулятором гомеостаза глюкозы. Новые исследования подчеркивают важную роль серотонина, полученного из кишечных энтерохромаффинных клеток, в регуляции продукции глюкозы в печени, липолиза, а также в развитии ожирения и сахарного диабета 2 типа [7]. Данные исследования подтверждают изменение углеводного обмена за счет способности продуцировать и высвобождать серотонин из проксимального отдела кишки, что тесно связано с увеличением массы тела и уровнем глюкозы, являясь важным звеном патогенеза ожирения и сахарного диабета 2 типа. Увеличение представителей кишечной микробиоты может наблюдаться на латентной стадии заболевания, что является важным диагностическим признаком и способствует назначению лекарственной терапии [8–10]. На основании анализа литературных источников, а также данных собственных исследований, следует сделать вывод, что изменение числа представителей метаболического кластера микробиоты кишечника может быть ранним маркером в верификации диагноза.
Заключение
Ранний скрининг изменений состава кишечной микробиоты, вероятно, может способствовать своевременному лечению метаболических нарушений, а значит улучшению качества жизни каждого конкретного пациента. Требуются дальнейшие исследования о роли микробиоты кишечника. Если эта роль подтвердится, анализ микробиоты может стать одним из диагностических показателей раннего патологического процесса, необходимого для своевременных лечебно-профилактических мероприятий, улучшения качества жизни и увеличения ее продолжительности.
Предыдущая статья
Т.В. Калинкина, Н.В. Ларёва, М.В. Чистякова ФГБОУ ВО «Читинская государственная медицинская акаде...
Следующая статья
Е.Б. Киреева, С.В. Гайдук, П.В. Агафонов ФГБВОУ ВО «Военно-медицинская академия имени С.М. Кирова...