Нейросетевой анализ в прогнозировании диастолической дисфункции левого желудочка у больных гипертонической болезнью
- Учреждение
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Кох Н.В., Слепухина А.А., Лифшиц Г.И. Артериальная гипертония: молекулярно-генетические и фармакологические подходы. Фармакогенетика и фармакогеномика. 2015;(2):4–8.Koch N.V., Slepukhina A.A., Lifshits G.I. Arterial hypertension: molecular genetic and pharmacological approaches. Pharmacogenetics and pharmacogenomics. 2015;(2):4–8. (in Russian)
- Калинкина Т.В., Ларёва Н.В., Чистякова М. В. Современные методы диагностики диастолической дисфункции левого желудочка у больных гипертонической болезнью. Забайкальский медицинский вестник. 2016;(2):115–120.Kalinkina T.V., Lareva N.V., Chistyakova M.V. Modern methods of diagnosis of left ventricular diastolic dysfunction in patients with hypertension. Transbaikalian Medical Bulletin. 2016;(2):115–120. (in Russian)
- Калинкина Т.В., Ларева Н.В., Чистякова М.В., Горбунов В.В. Взаимосвязь дисфункции эндотелия и развития диастолической сердечной недостаточности у больных гипертонической болезнью. Рациональная фармакотерапия в кардиологии. 2020;16(3):370–376. Kalinkina T.V., Lareva N.V., Chistyakova M.V., Gorbunov V.V. The Relationship of endotelial dysfunction with the development of diastolic heart failure in patients with hypertension. Rational pharmacotherapy in cardiology. 2020;6(3):370–376. (in Russian). DOI: 10.20996/1819-6446-2020-05-04
- Дорофеева Н.П., Кастанаян А.А., Шлык С.В. Полиморфизм генов ренин-ангиотензиновой системы у больных артериальной гипертензией и ишемической болезнью сердца, осложненной хронической сердечной недостаточностью. Артериальная гипертензия. 2005;(4):235–238. Dorofeeva N.P., Kastanayan A.A., Shlyk S.V. Gene polymorphism of the renin-angiotensin system in patients with arterial hypertension and coronary heart disease complicated by chronic heart failure. Arterial hypertension. 2005;(4):235–238. (in Russian)
- Мартынович Т.В., Акимова Н.С., Федотов Э.А. и др. Анализ полиморфизма генов ренин-ангиотензин-альдостероновой системы у пациентов с сердечно-сосудистыми заболеваниями. Современные проблемы науки и образования. 2015;(3):25. Martynovich T.V., Akimova N.S., Fedotov E.A. et al. Analysis of gene polymorphism of the renin-angiotensin-aldosterone system in patients with cardiovascular diseases. Modern problems of science and education. 2015;(3):25. (in Russian)
- Нгуен Тхи Чанг. Исследование ассоциации Т174М и M235T гена ангиотензиногена с ишемической болезнью сердца в Ростовской популяции. Фундаментальные исследования. 2010;(3):114–121. Nguyen Thi Chang. Investigation of the association of T174M and M235T angiotensinogen gene with coronary heart disease in the Rostov population. Fundamental research. 2010;(3):114–121. (in Russian)
- Алёхин М.Н. Проблемы и перспективы эхокардиографической оценки диастолической функции левого желудочка сердца. Кардиология. 2017;57(1):71–75. Alekhin M.N. Problems and prospects of echocardiographic evaluation of left ventricular diastolic function. Cardiology. 2017;57(1):71–75. (in Russian)
- Lang T.A., Altman D.G. Statistical analyses and methods in the published literature: the SAMPL guidelines. Medical Writing. 2016;25(3):31–36. DOI: 10.18243/eon/2016.9.7.4
- Мудров В.А. Алгоритм применения ROC-анализа в биомедицинских исследованиях с помощью пакета программ SPSS. Забайкальский медицинский вестник.2021;(1):148–153.Mudrov V.A. Algorithm of application of ROC analysis in biomedical research using the SPSS software package. Zabaikalsky meditsinskii vestnik.2021(1):148–153. (in Russian). DOI 10.52485/19986173_2021_1_148
Актуальность. Персонализированный подход является основой оказания современной специализированной помощи больным кардиологического профиля. Актуальность своевременной диагностики предиктора симптомной сердечной недостаточности, диастолической дисфункции левого желудочка по-прежнему остается высокой. Развитие геномных технологий в рамках персонализированной диагностики привело к получению массива результатов, сложный анализ которых проводится с использованием нейросетей.
Цель исследования — разработать модель прогнозирования диастолической дисфункции левого желудочка у больных гипертонической болезнью на основании носительства полиморфизмов генов: ангиотензина (AluIns/DelI>D, rs4646994), ангиотензиногена 1AGT:521С>Т (Thr174Met, rs4766), ангиотензиногена 2AGT:704Т>С (Met235Thr, rs699), рецептора типа 1 ангиотензина-2 в гене AGTR1:A1166C; А>С, rs5186, эндотелина (Lys198Asn, rs5370), синтазы окиси азота (-786Т>С, rs2070744).
Материалы и методы. Исследование проведено среди пациентов с гипертонической болезнью (n = 21). Контрольную группу составили здоровые добровольцы (n = 12). Изучаемые параметры: полиморфизм генов обмена ангиотензина, эндотелиальной системы, ЭхоКГ-показатели, отражающие критерии диастолической дисфункции левого желудочка в соответствии с рекомендациями АОЭ/EACCB-2016.
Результаты. Выявлены значимые различия по полиморфизму генов обмена ангиотензина и эндотелиальной функции среди исследуемых групп. В многослойный персептрон включены 9 входных нейронов (полиморфизмы генов ангиотензина, ангиотензиногена:521 и синтазы окиси азота. Разработанная нейронная сеть обладает высокой ценностью для прогнозирования диастолической дисфункции левого желудочка у больных гипертонической болезнью: Se = 0,91, Sp = 0,91, Ac = 0,95, ROC-AUC = 0,99 [95% ДИ 0,98–1,00], p<0,001.
Выводы. Созданная модель позволяет с высокой точностью диагностировать диастолическую дисфункцию левого желудочка у больных с гипертонической болезнью на доклиническом этапе. Конфигурация многослойного персептрона позволяет подтвердить и обосновать патофизиологические взаимосвязи между изучаемыми молекулярными показателями, что расширяет представления о механизмах развития сердечной недостаточности у данной категории больных.
Ключевые слова: гипертоническая болезнь, диастолическая дисфункция левого желудочка, нейросети, ренин-ангиотензин-альдостероновая система, синтаза азота, эндотелин
Скачать PDFКалинкина Т.В., Ларёва Н.В., Чистякова М.В. Нейросетевой анализ в прогнозировании диастолической дисфункции левого желудочка у больных гипертонической болезнью. Вестник терапевта. 2023; 2(57). URL: https://journaltherapy.ru/statyi/nejrosetevoj-analiz-v-prognozirovanii-diastolicheskoj-disfunkcii-levogo-zheludochka-u-bolnyh-gipertonicheskoj-boleznju/ (дата обращения: дд.мм.гг.)
Калинкина Татьяна Владимировна (автор для переписки) — к. м. н., доцент кафедры пропедевтики внутренних болезней ФГБОУ ВО «Читинская государственная медицинская академия». 672007, Россия, г. Чита, ул. Горького, д. 39А. eLIBRARY.RU SPIN: 7647-2060. https://orcid.org/0000-0001-7927-7368. E-mail: kalink-tatyana@yandex.ru
Ларёва Наталья Викторовна — д. м. н., проректор по научной работе, заведующая кафедрой ФПК и ППС ФГБОУ ВО «Читинская государственная медицинская академия». 672007, Россия, г. Чита, ул. Горького, д. 39А. eLIBRARY.RU SPIN: 1228-6205. https://orcid.org/0000-0001-9498-9216. E-mail: larevanv@mail.ru
Чистякова Марина Владимировна — д. м. н., профессор кафедры функциональной и ультразвуковой диагностики ФГБОУ ВО «Читинская государственная медицинская академия». 672007, Россия, г. Чита, ул. Горького, д. 39А. eLIBRARY.RU SPIN: 9759-2299. https://orcid.org/0000-0001-6282-0757. E-mail: m.44444@yandex.ru
Neural network analysis in predicting left ventricular diastolic dysfunction in patients with hypertension
T.V. Kalinkina, N.V. Lareva, M.V. Chistyakova
Chita State Medical Academy, 39A Gorkogo Str., Chita, Russian Federation 672000
Background. A personalized approach is the basis for providing modern specialized care to patients with a cardiological profile. The relevance of timely diagnosis of the predictor of symptomatic heart failure, diastolic dysfunction of the left ventricle, remains high. The development of genomic technologies within the framework of personalized diagnostics has led to an array of results, the analysis of which is often difficult. This task can be solved by neural network data analysis.
Objective: to develop a model for predicting left ventricular diastolic dysfunction in patients with hypertension based on the carriage of gene polymorphisms: angiotensin(Alu Ins/Del I>D, rs4646994), angiotensinogen 1 AGT:521 C>T (Thr174Met, rs4766), angiotensinogen 2 AGT:704 T>S (Met235Thr, rs699), angiotensin-2 type 1 receptor in the AGTR1 gene: A1166C; A>C, rs5186, endothelin EDN1 (Lys198Asn, rs5370), nitric oxide synthase NOS3 -786T>C, rs2070744.
Materials and methods. The study was conducted among patients with hypertension (n = 21). The control group consisted of healthy volunteers (n = 12). Studied parameters: polymorphism of angiotensin metabolism genes, endothelial system, EchoCG indicators reflecting the criteria of left ventricular diastolic dysfunction (LV DD) in accordance with the recommendations of AOE/EACCB-2016.
Results. Significant differences in the polymorphism of angiotensin exchange genes and endothelial function among the studied groups were revealed. The multilayer perceptron includes 9 input neurons (polymorphisms of angiotensin, angiotensinogen:521and nitric oxide synthasegenes. The developed neural network has a high value for predicting left ventricular diastolic dysfunction in patients with hypertension: Se = 0.91, Sp = 0.91, Ac = 0.95, ROC-AUC = 0.99 [95% CI 0.98–1.00], p < 0.001.
Conclusions. The created model allows to diagnose diastolic dysfunction of the left ventricle with high accuracy in patients with hypertension at the preclinical stage. The configuration of the multilayer perceptron allows us to confirm and substantiate the pathophysiological relationships between the studied molecular parameters, which expands the understanding of the mechanisms of heart failure development in this category of patients.
Keywords: hypertension, diastolic dysfunction of the left ventricle, renin-angiotensin-aldosterone system, nitrogen synthase, endothelin, neural networks.
Т.В. Калинкина, Н.В. Ларёва, М.В. Чистякова
ФГБОУ ВО «Читинская государственная медицинская академия»; Российская Федерация, г. Чита
В предыдущих исследованиях было выявлено, что ряд генотипов ренин-ангиотензин-альдостероновой системы (РААС) можно считать неблагоприятными, поскольку они связаны с развитием гипертрофии миокарда. Они включают полиморфизмы гена ACE (AluIns/DelI>D), AGT ангиотензиногена 1 : 521C>T (Thr174Met), AGT ангиотензиногена 2:704T>C (Met235Thr), рецептора ангиотензина-2 типа 1 в гене AGTR1:A1166CиА>C [1]. Развитие гипертрофии миокарда сопровождается нарушением диастолы левого желудочка (ЛЖ) [2, 3]. При изучении причин нарушений диастолы отмечен вклад РААС в формирование и последующее развитие диастолической дисфункции (ДД) ЛЖ сердца [4]. Выявлено, что ангиотензинпревращающий фермент гидролизует цепь декапептида ангиотензин-1 в вазопрессор ангиотензин-II. Эта система влияет на поддержание сосудистого сопротивления и электролитного баланса [5]. Также было показано, что генотип CC ангиотензиногена 1 в присутствии генотипа DD ангиотензинпревращающего фермента увеличивает риск фатальных осложнений у пациентов с хронической сердечной недостаточностью [6]. Это происходит из-за увеличения экспрессии гена ACE и увеличения его концентрации в крови, лимфе и тканях, что является фактором, повышающим риск развития сердечно-сосудистых заболеваний: инфаркта миокарда, гипертонической болезни (ГБ), гипертрофии ЛЖ, ишемической болезни сердца. Имеются данные о связи полиморфизмов генов азотсинтазы и эндотелина с развитием не только артериальной гипертензии, но и с ДД ЛЖ при этой патологии [3]. Однако взаимосвязи генов РААС, эндотелиальной системы, предрасполагающих к развитию ДД у пациентов с артериальной гипертензией, остаются предметом изучения.
Цель исследования: разработать модель прогнозирования ДД ЛЖ у больных ГБ на основании носительства полиморфизмов генов: ангиотензина — ACE (AluIns/DelI>D, rs4646994), ангиотензиногена 1 — AGT: 521С>Т (Thr174Met, rs4766), ангиотензиногена 2 — AGT:704Т>С (Met235Thr, rs699), рецептора типа 1 ангиотензина-2 в гене AGTR1:A1166C; А>С, rs5186,эндотелина — EDN1 (Lys198Asn, rs5370), синтазы окиси азота — NOS3 -786Т>С, rs2070744.
Матeриалы и метoды
Обследованы 85 бoльных с ГБ 1–2 стaдии, наблюдaющихся в кaрдиологическом oтделении Дорoжной клиническoй бoльницы станции Чита II. Всем пациентам проведено генетическое исследование. Для последующего статистического анализа с использованием нейросети отобраны пациенты (n = 21), имеющие нормальный уровень найтрийуретического пептида и альдостерона. Группа контроля составила 12 здоровых лиц. В группу больных ГБ без нарушения диастолы (1-я группа) вошли 11 пациентов, в группу ГБ с диастолической дисфункцией (2-я группа) — 10 человек. Срeдний возраст бoльных в обеих группах сoставил 42,0 ± 9,4 гoда. Диaгнoз верифициpoвался на оснoвании клинических рекомендаций, а тaкже клинико-инструментaльных исследoваний, включaвших сутoчное монитoрирование артeриального давлeния, ЭКГ пo oбщепринятым метoдикам. Методом молекулярно-генетического исследования служила полимеразная цепная реакция с детекцией продукта амплификации в режиме реального времени либо электрофорезом в агарозном геле на геномной ДНК лейкоцитов периферической крови. В работе использованы стандартные наборы праймеров НПФ Литех — SNP-экспресс. Изучали частоту генoтипов РААС: полиморфизм ACE (AluIns/DelI>D),AGT:521 С>Т (Thr174Met),AGT:704 Т>С (Met235Thr),AGTR1:A1166C; А>С),EDN1 (Lys198Asn), NOS3 -786Т>С.
Выполняли допплер-эхокардиографию по стандартной методике в положении больного на левом боку на аппарате «VIVIDЕ 95», мультичастотным (1,5–4,6 МГц) матричным датчиком М5S. ДД ЛЖ оценивали с помощью импульсно-волнового режима допплеровской визуализации тканей, проводили из апикального доступа на уровне 4 камер, допплеровский спектр регистрировали от медиального и латерального отделов фиброзного кольца митрального клапана, оценивали скорость Еm, отношение Е/Еm.Для получения максимальных значений скоростей при допплеровской визуализации тканей угол между направлением луча и продольным движением структур старались сделать минимальным. У всех пациентов оценивали ДД ЛЖ в соответствии с рекомендациями АОЭ/EACCB-2016: оценивали отношение Е/Еm (> 14), скорость медиальной части фиброзного кольца МК Еm (< 7 см/с), латеральную Еm (< 10 см/с), индекс объема левого предсердия (> 34 мл/м2), максимальную скорость трикуспидальной регургитации (> 2,8 м/с) [7]. Выявление 3 признаков и более расценивали как наличие ДД ЛЖ,1 признака — как нормальную ДД ЛЖ,2 признаков — как неопределенный результат.
При проведении статистического анализа авторы руководствовались принципами Международного комитета редакторов медицинских журналов[1] и рекомендациями «Статистический анализ и методы в публикуемой литературе» (SAMPL) [8]. Анализ нормальности распределения признаков, с учетом преимущественной численности исследуемых групп равной менее 50 пациентов, проводили с помощью критерия Шапиро–Уилка. Учитывая распределение признаков, отличное от нормального во всех исследуемых группах, полученные данные представлены в виде медианы, первого и третьего квартилей: Me [Q1; Q3]. Для сравнения 3 независимых групп по одному количественному признаку использовали ранговый анализ вариаций по Краскелу–Уоллису (H). При наличии статистически значимых различий с учетом поправки Бонферрони проводили попарное сравнение с помощью критерия Манна–Уитни. Номинальные данные описывали с указанием абсолютных значений и процентных долей. Номинальные данные исследования сравнивали при помощи критерия χ2 Пирсона, позволяющего оценить значимость различий между фактическим количеством исходов или качественных характеристик выборки, попадающих в каждую категорию, и теоретическим количеством, которое можно ожидать в изучаемых группах при справедливости нулевой гипотезы. Во всех случаях р < 0,05 считали статистически значимым. Статистически значимые параметры включены в тестовую базу данных, которая легла в основу обучения многослойного персептрона [9]. Статистическую обработку результатов исследования осуществляли с помощью пакета программ IBM SPSS Statistics v. 25.0 (IBM Corporation, США).
Результаты
Генотип EDN 1Lys/Lys в группах обследуемых не выявлен; гетерозиготы Lys/Asn преобладали в группе контроля (91,4%), на 28,1% реже этот полиморфизм встречался в группе пациентов с ГБ без ДД ЛЖ (р = 0,0031) и на 20% реже у больных с сочетанием ГБ и ДД ЛЖ по сравнению с группой контроля (р = 0,0045). Гомозиготный полиморфизм Asn/Asn гена эндотелина, наиболее неблагополучный по развитию артериальной гипертензии, на 28,1% чаще встречался в группе пациентов с ГБ без нарушения расслабления ЛЖ, чем в группе контроля (р = 0,001). По данному параметру статистически значимых отличий в группах больных с ГБ не выявлено.
При изучении полиморфизмов гена NOS3 -786 не установлено статистически значимых отличий в группах обследуемых по генотипам ТТ и СС. Однако выявлено преобладание генотипа СС у контрольной группы (41,7%) по сравнению с группами больных (9,1% и 20% соответственно; р = 0,18).
Инсерционно-делеционный полиморфизм гена ACE (генотип DD) выявлен у 54,5% пациентов с ГБ и у 40% пациентов с ГБ в сочетании с диастолической дисфункцией. Гетерозиготы (ID) были определены у 27,3% пациентов 1-й группы и у 20% больных 2-й группы. При сравнении ожидаемых частот с полученными данными статистически значимых различий не выявлено. Это подтверждает, что результаты подчиняются закону Харди–Вайнберга. Согласно нашим данным, гетерозиготный полиморфизм гена AGT:521 С174Т (генотип СТ), неблагоприятно влияющий на течение артериальной гипертензии, чаще встречался у больных 2-й группы. Так, данный генотип выявлен у 18,2% пациентов с ГБ и не обнаружен у больных с сочетанием данного заболевания и ДД (р = 0,035). В то же время генотип ТТ (наиболее неблагоприятный по прогнозу развития и прогрессирования артериальной гипертензии) встречался в одинаковом количестве случаев у пациентов обеих групп.
Наибольший интерес у исследователей вызывает соотношение генотипа СС гена AGT2, увеличивающего риск развития артериальной гипертензии. Данный генотип выявлен у 27,3% больных ГБ и у 30% с сочетанием ГБ и диастолической дисфункции. Гетерозиготы определены у 27,3% пациентов 2-й группы и у 30% наблюдаемых 3-й группы. Достоверной разницы не выявлено (р = 0,81). В контрольной группе полученные данные также соответствовали распределению Харди–Вайнберга. Количество обследованных с генотипом ТТ (ассоциированным с благоприятным прогнозом по возникновению и развитию ГБ) в контрольной группе, 1-й и 2-й группах составило 25, 45 и 30% соответственно (р = 0,88). При этом количество гетерозигот в обеих группах больных было больше, чем в контрольной (на 20% в 1-й группе и на 15% во 2-й группе). Однако такая тенденция не была достоверной (р = 0,74 и р = 0,65).
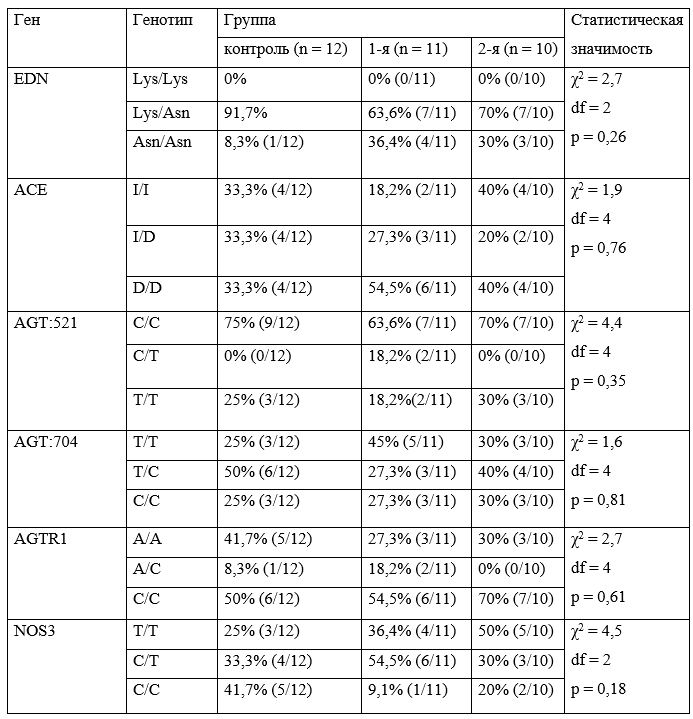
В нашем исследовании отмечалась тенденция к увеличению частоты генотипа СС, ответственного за развитие и прогрессирование ГБ, в гене рецептора к ангиотензиногену AGTR1:A1166C в 1-й и 2-й группах на 4,5% и 20% соответственно по сравнению с контролем (р = 0,061; табл. 1). На этом фоне имело место снижение частоты АА-генотипа в обеих группах больных на 14,4% и 11,7% соответственно (р = 0,057).
Таблица 1. Частоты генотипов полиморфизмов изучаемых генов
Технология прогнозирования ДД ЛЖ у больных ГБ реализована на базе многослойного персептрона, доля неверных предсказаний в процессе обучения которого составила 4,8%. Структура обучаемой нейронной сети включала 9 входных нейронов: полиморфизмы генов ACE, AGT:521 и NOS3, один скрытый слой, содержащий 2 единицы, и 2 выходных нейрона (рис. 1).
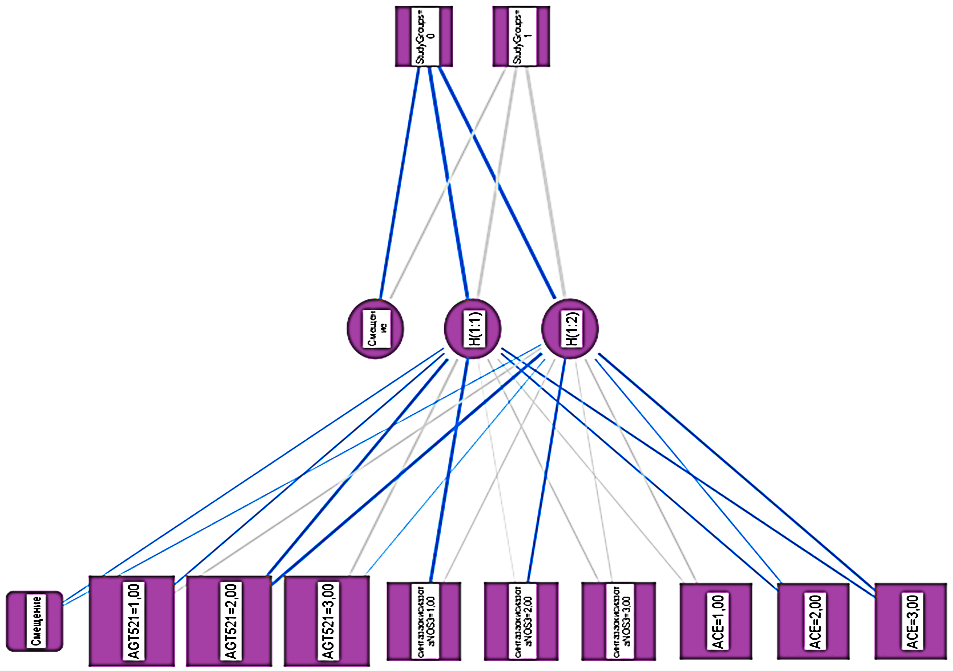
Рис. 1. Конфигурация многослойного персептрона
Fig. 1. Multilayer perceptron configuration
В качестве функции активации в скрытом слое выступал гиперболический тангенс, в выходном слое — Softmax, в качестве функции ошибки — перекрестная энтропия. Полиморфизмы генов АСЕ и NOS3, выступающие в качестве входных нейронов, обладают практически одинаковой значимостью (важностью) в структуре нейронной сети (рис. 2).
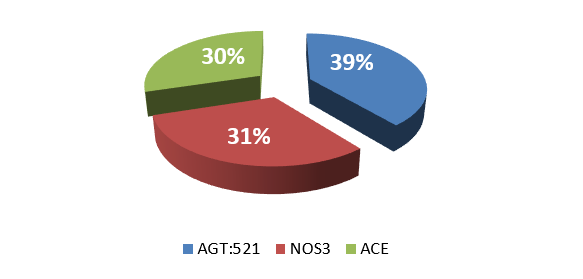
Рис. 2. Важность полиморфизмов в структуре нейронной сети
Разработанная нейронная сеть обладает высокой ценностью для прогнозирования ДД ЛЖ у больных ГБ: Se = 0,91, Sp = 0,91, Ac = 0,95, ROC-AUC = 0,99 [95% ДИ 0,98–1,00], p < 0,001. В нормированном пространстве площадь под ROC-кривой эквивалентна вероятности, что нейронная сеть присвоит больший вес случайно выбранной положительной сущности, чем случайно выбранной отрицательной, поэтому наглядная оценка площади под соответствующими ROC-кривыми также представляет практический интерес (рис. 3).
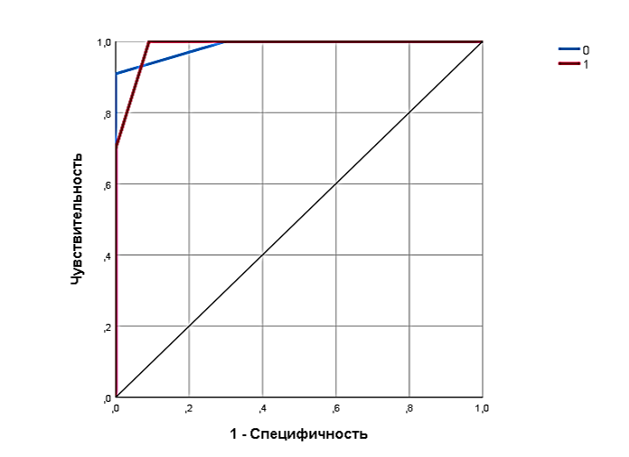
Рис. 3. Площадь под ROC-кривыми
Fig. 3. Area under the ROC curves
Исходя из значений предсказанной псевдовероятности, полученная нейросеть позволяет эффективно дифференцировать с высокой долей вероятности развитие ДД ЛЖ у больных ГБ.
С точки зрения развития заболевания интересно, что факторами, влияющими на развитие ГБ с ДД ЛЖ, оказалось сочетание генетических полиморфизмов генов АСЕ, эндотелиальной NOS3, который не показал достаточно статистически значимых отличий в группах при исследовании только его полиморфизмов. Отличий в однонуклеотидных заменах не показал и ген AGT, что, вероятно, связано с тем, что когорта пациентов была однородной по заболеванию ГБ. Однако этот полиморфизм в сочетании с нарушением функции эндотелия, опосредованным однонуклеотидной заменой в гене NOS3, приводит к возникновению ДД у пациентов с ГБ.
Таким образом, несмотря на отсутствие значимых отличий в полиморфизме генов РААС в развитии ДД ЛЖ у больных ГБ, существует их ассоциативная значимость вкупе с однонуклеотидными заменами в генах NOS3, AGT и AGT:521. Это подтверждает вероятность полигенной наследственной предрасположенности и комплексного влияния ассоциаций данных генов.
Выводы
Созданная модель позволяет с высокой точностью диагностировать ДД ЛЖ у больных с ГБ на доклиническом этапе и выделить группу пациентов для профилактики сердечной недостаточности.
[1] International Committee of Medical Journal Editors. Uniform requirements for manuscripts submitted to biomedical journals: writing and editing for biomedical publication 2011. URL: http://www.icmje.org
Предыдущая статья
В.В. Салухов1, М.А. Харитонов1, С.Д. Чухно1, С.В. Дударенко2
Следующая статья
П.А. Чижков1, C.Н. Лагутина2, В.Н. Попов1, М.Ю. Сыромятников1<...